名校
1 . 已知:①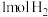 分子中化学键断裂时需要吸收436kJ的能量,②
分子中化学键断裂时需要吸收436kJ的能量,② 蒸气中化学键断裂时需要吸收151kJ的能量,③由H原子和I原子形成
蒸气中化学键断裂时需要吸收151kJ的能量,③由H原子和I原子形成 分子时释放299kJ的能量。下列判断不正确的是
分子时释放299kJ的能量。下列判断不正确的是
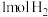 分子中化学键断裂时需要吸收436kJ的能量,②
分子中化学键断裂时需要吸收436kJ的能量,② 蒸气中化学键断裂时需要吸收151kJ的能量,③由H原子和I原子形成
蒸气中化学键断裂时需要吸收151kJ的能量,③由H原子和I原子形成 分子时释放299kJ的能量。下列判断不正确的是
分子时释放299kJ的能量。下列判断不正确的是A. 蒸气比 蒸气比 分子稳定 分子稳定 |
B. 发生分解生成 发生分解生成 蒸气和 蒸气和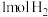 吸收11kJ热量 吸收11kJ热量 |
| C.HI溶液与NaOH溶液反应属于放热反应 |
| D.上述HI的生成过程中有非极性键的断裂和极性键的生成 |
您最近一年使用:0次
名校
2 . 臭氧( )在
)在 催化下能将烟气中的
催化下能将烟气中的 、
、 分别氧化为
分别氧化为 和
和 。下列关于N、O、S、Fe元素及其化合物的说法正确的是
。下列关于N、O、S、Fe元素及其化合物的说法正确的是
 )在
)在 催化下能将烟气中的
催化下能将烟气中的 、
、 分别氧化为
分别氧化为 和
和 。下列关于N、O、S、Fe元素及其化合物的说法正确的是
。下列关于N、O、S、Fe元素及其化合物的说法正确的是A. 是含有极性键的非极性分子 是含有极性键的非极性分子 |
B.由于O、N、S非金属性依次递减,所以沸点: |
C. 的VSEPR模型: 的VSEPR模型: |
D.1mol  含有σ键12mol 含有σ键12mol |
您最近一年使用:0次
名校
解题方法
3 . 某化合物具漂白性,主要用于染色工艺,其结构如图所示,其中W、X、Y、M、Z是原子序数依次递增的短周期主族元素,且Y和 同主族,下列说法错误的是
同主族,下列说法错误的是
 同主族,下列说法错误的是
同主族,下列说法错误的是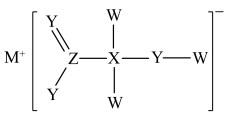
A.电负性: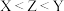 | B. 和 和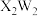 均为极性分子 均为极性分子 |
| C.MW与水反应后的溶液呈碱性 | D. 利 利 的VSEPR模型名称均为平面三角形 的VSEPR模型名称均为平面三角形 |
您最近一年使用:0次
2024-05-27更新
|
395次组卷
|
5卷引用:天津市耀华中学2024届高三下学期第二次模拟化学试题
4 . 下列陈述Ⅰ和陈述Ⅱ具有对应关系的是
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | 电负性: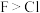 | 酸性: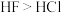 |
B | 第一电离能: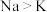 | 与水反应剧烈程度: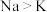 |
C | 分子极性: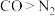 | 范德华力: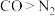 |
D | 分子间作用力: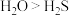 | 热稳定性: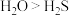 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 已知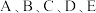 是原子序数依次增大的前四周期元素,其元素性质或原子结构如表:
是原子序数依次增大的前四周期元素,其元素性质或原子结构如表:
(1)A的最高价氧化物是___________ 分子。(填“极性”或“非极性”)
(2)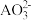 的空间结构为
的空间结构为___________ ,其中心原子的杂化方式为___________ 杂化。
(3)C的气态氢化物沸点是同族元素氢化物沸点中最高的,其原因是___________ 。
(4) 属于
属于___________ 区的元素,其基态原子的价层电子轨道表示式为___________ 。
(5) 的基态原子的电子排布式为
的基态原子的电子排布式为___________ ,在周期表中位置___________ 。
 是原子序数依次增大的前四周期元素,其元素性质或原子结构如表:
是原子序数依次增大的前四周期元素,其元素性质或原子结构如表: | 原子核外电子分占3个不同能级,且每个能级上排布的电子数相同 |
 | 原子最高能级的不同轨道都有电子,且自旋方向相同 |
 | 在周期表所有元素中电负性最大 |
 | 位于周期表中第4纵列 |
 | 基态原子 层全充满, 层全充满, 层只有一个电子 层只有一个电子 |
(2)
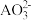 的空间结构为
的空间结构为(3)C的气态氢化物沸点是同族元素氢化物沸点中最高的,其原因是
(4)
 属于
属于(5)
 的基态原子的电子排布式为
的基态原子的电子排布式为
您最近一年使用:0次
6 . 下列说法错误的是
| A.水很稳定是因为水中含有大量氢键 |
| B.在同一能级上运动的电子,其运动状态不可能相同 |
| C.碘易溶于四氯化碳、甲烷难溶于水,二者都可用相似相溶原理解释 |
| D.M能层最多含3个能级 |
您最近一年使用:0次
7 . 下列陈述Ⅰ和Ⅱ均正确,且二者具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A |  可用作葡萄酒的保鲜 可用作葡萄酒的保鲜 |  有漂白性 有漂白性 |
| B |  易溶于 易溶于 |  和 和 都是非极性分子 都是非极性分子 |
| C | HF的沸点高于HCl | H-F键键能比H-Cl键的大 |
| D | 铁罐车可用于装运浓硝酸 | 常温下Fe与浓硝酸不反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 下列叙述不正确 的是
A.酸性: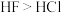 | B.键角: |
C. 中的溶解度: 中的溶解度: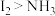 | D.晶体硬度:金刚石>晶体硅 |
您最近一年使用:0次
名校
解题方法
9 . 下列对一些实验事实的理论解释正确的是
| 选项 | 实验事实 | 理论解释 |
| A | 1体积水可以溶解700体积氨气 | 氨是极性分子且有氢键的影响 |
| B | 白磷为正四面体分子 | 白磷分子中P-P键间的夹角是109.5° |
| C | SO2、H2O分子空间结构均为V形 | SO2、H2O中心原子均为sp3杂化 |
| D | HF的沸点高于HCl | H-F的键长比H-Cl的键长短 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 研究人员发现在某种含钒催化剂的作用下,NO可被 还原为
还原为 ,从而降低含氮气体造成的空气污染,反应机理如图所示,下列说法错误的是
,从而降低含氮气体造成的空气污染,反应机理如图所示,下列说法错误的是
 还原为
还原为 ,从而降低含氮气体造成的空气污染,反应机理如图所示,下列说法错误的是
,从而降低含氮气体造成的空气污染,反应机理如图所示,下列说法错误的是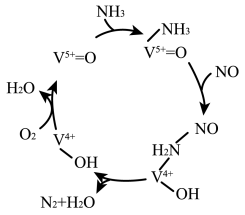
A. 价电子排布式为 价电子排布式为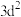 ,核外电子有11种空间运动状态 ,核外电子有11种空间运动状态 |
B. 和NO分子是极性分子, 和NO分子是极性分子, 为该反应的中间体 为该反应的中间体 |
| C.该转化过程中,氧化剂只有NO |
D. 可加快反应速率,却不能提高总反应的平衡转化率 可加快反应速率,却不能提高总反应的平衡转化率 |
您最近一年使用:0次



