名校
1 . 下列对分子性质的解释中,正确的是
| A.NH3极易溶于水而CH4难溶于水只是因为NH3是极性分子,CH4是非极性分子 |
B.乳酸( )具有光学活性,因为其分子中含有一个手性碳原子 )具有光学活性,因为其分子中含有一个手性碳原子 |
| C.水很稳定(1000℃以上才会部分分解)是因为水分子间存在大量的氢键 |
| D.PH3分子与NH3分子的键角相同 |
您最近一年使用:0次
名校
2 . 使用铜基催化剂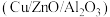 ,以
,以 和
和 合成
合成 是大规模实现低碳减排和清洁能源再生产的有效路径。回答下列问题:
是大规模实现低碳减排和清洁能源再生产的有效路径。回答下列问题:
(1) 的
的 模型名称是
模型名称是___________ , 分子中O的杂化轨道类型是
分子中O的杂化轨道类型是___________ 。
(2)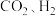 和
和 中,属于极性分子的是
中,属于极性分子的是___________ ,由非极性键结合成的非极性分子是___________ 。
(3) 的沸点
的沸点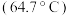 介于
介于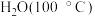 和
和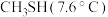 之间,其原因是
之间,其原因是___________ 。
(4) 属于
属于___________ 晶体, 属于
属于___________ 晶体。
(5) 的一种立方晶胞结构如图所示,每个
的一种立方晶胞结构如图所示,每个 周围与它最近且相等距离的
周围与它最近且相等距离的 有
有___________ 个。若该立方晶胞参数为 ,则正负离子的核间距最小为
,则正负离子的核间距最小为___________  ,晶体密度
,晶体密度
___________  (列出算式,阿伏加德罗常数的值为
(列出算式,阿伏加德罗常数的值为 )。
)。
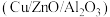 ,以
,以 和
和 合成
合成 是大规模实现低碳减排和清洁能源再生产的有效路径。回答下列问题:
是大规模实现低碳减排和清洁能源再生产的有效路径。回答下列问题:(1)
 的
的 模型名称是
模型名称是 分子中O的杂化轨道类型是
分子中O的杂化轨道类型是(2)
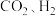 和
和 中,属于极性分子的是
中,属于极性分子的是(3)
 的沸点
的沸点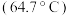 介于
介于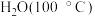 和
和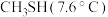 之间,其原因是
之间,其原因是(4)
 属于
属于 属于
属于(5)
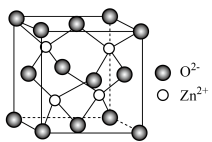
 的一种立方晶胞结构如图所示,每个
的一种立方晶胞结构如图所示,每个 周围与它最近且相等距离的
周围与它最近且相等距离的 有
有 ,则正负离子的核间距最小为
,则正负离子的核间距最小为 ,晶体密度
,晶体密度
 (列出算式,阿伏加德罗常数的值为
(列出算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
名校
3 . 家庭药箱常备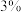 的过氧化氢消毒液。过氧化氢的分子结构如下图所示,两个氢原子犹如分布在半展开的书的两面上。下列关于
的过氧化氢消毒液。过氧化氢的分子结构如下图所示,两个氢原子犹如分布在半展开的书的两面上。下列关于 的说法中正确的是
的说法中正确的是
 的过氧化氢消毒液。过氧化氢的分子结构如下图所示,两个氢原子犹如分布在半展开的书的两面上。下列关于
的过氧化氢消毒液。过氧化氢的分子结构如下图所示,两个氢原子犹如分布在半展开的书的两面上。下列关于 的说法中正确的是
的说法中正确的是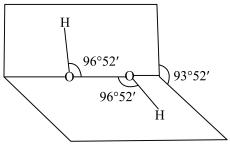
| A.分子中既有极性键又有非极性键 | B.属于非极性分子,易溶于 |
C.两个氧原子均采用 杂化 杂化 | D.分子中既有 键又有 键又有 键 键 |
您最近一年使用:0次
名校
解题方法
4 . 根据下列证据,所得推理错误的是
| 选项 | 证据 | 推理 |
| A | 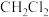 不存在同分异构体 不存在同分异构体 | 碳的4个价键指向四面体的顶点 |
| B | 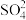 的键长、键角均相等 的键长、键角均相等 |  的空间结构为正四面体,S采用 的空间结构为正四面体,S采用 杂化 杂化 |
| C |  在水中的溶解度比 在水中的溶解度比 大得多 大得多 |  是极性分子, 是极性分子, 是非极性分子 是非极性分子 |
| D |  的键角为 的键角为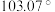 |  为极性分子,O采用 为极性分子,O采用 杂化 杂化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 一种能增强人体免疫力的化合物,其结构如图,其中X、Y、Z、W、R为原子序数依次增大的短周期主族非金属元素,W、R同族。下列说法正确的是
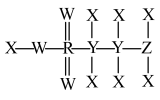
| A.R的常见氧化物均属于非极性分子 |
| B.氢化物的沸点:W>Z>Y |
| C.原子半径:Z>Y>X |
| D.X、Z、W三种元素既可形成共价化合物又可形成离子化合物 |
您最近一年使用:0次
6 . 短周期主族元素X、Y、Z、W的原子序数依次增大,W的最外层电子数比X的最外层电子数少1个,X、Y、Z为同一周期元素,X、Y、Z组成一种化合物 的结构式如图所示。下列说法错误的是
的结构式如图所示。下列说法错误的是
 的结构式如图所示。下列说法错误的是
的结构式如图所示。下列说法错误的是
| A.W位于元素周期表的p区 |
| B.第一电离能:Y>Z>X |
| C.Z形成的单质一定是非极性分子 |
| D.Y、W可形成共价晶体 |
您最近一年使用:0次
7 . 六氟化硫( ,结构如图所示)是一种惰性温室气体,因其具有良好的绝缘性能和灭弧性能被广泛应用于电器工业。下列关于该物质的说法不正确的是
,结构如图所示)是一种惰性温室气体,因其具有良好的绝缘性能和灭弧性能被广泛应用于电器工业。下列关于该物质的说法不正确的是
 ,结构如图所示)是一种惰性温室气体,因其具有良好的绝缘性能和灭弧性能被广泛应用于电器工业。下列关于该物质的说法不正确的是
,结构如图所示)是一种惰性温室气体,因其具有良好的绝缘性能和灭弧性能被广泛应用于电器工业。下列关于该物质的说法不正确的是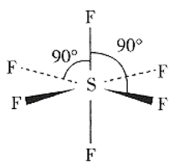
| A.分子中所有原子最外层均满足8电子稳定结构 |
B. 不易溶于水 不易溶于水 |
| C.电负性:S<F |
| D.能用作金属冶炼工业的保护剂 |
您最近一年使用:0次
名校
解题方法
8 . 下列对分子性质的解释中,不正确 的是
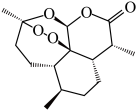
A.青蒿素的分子式为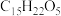 ,结构如图所示,该分子中包含7个手性碳原子 ,结构如图所示,该分子中包含7个手性碳原子 |
| B.碘易溶于四氯化碳、甲烷难溶于水都可用“相似相溶”规律解释 |
| C.过氧化氢是含有极性键和非极性键的极性分子 |
| D.水很稳定(1000℃以上才会部分分解)是因为水中含有大量的氢键 |
您最近一年使用:0次
名校
9 . 碳族元素的物质是化学世界中最庞大的家族,“天问一号”轨道飞行器近距离拍摄了火星北极,看到大量白色冰冻区域, 主要是二氧化碳低温凝结形成的干冰,虽然看起来和地球两极很像,但实际温度却比地球两极冷多了!
(1)已知 25℃时,H2CO3的Ka1=4.2×10-7、Ka2=4.8×10- 11,HCN的Ka=4.0×10-10,若向NaCN 溶液中通入少量 CO2,发生反应的离子方程式为___________ 。
(2)下列关于二氧化碳的说法正确的是___________。
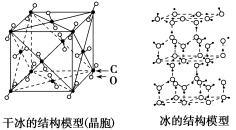
(3)干冰和冰的晶体模型如下图存在差别的本质原因___________ 。___________ 。
(5)金刚石晶体中,每个C被___________ 个六元环共用。
(6)晶体硅和碳化硅熔点较高的是___________ (填化学式)。
(7)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为___________ 。
(1)已知 25℃时,H2CO3的Ka1=4.2×10-7、Ka2=4.8×10- 11,HCN的Ka=4.0×10-10,若向NaCN 溶液中通入少量 CO2,发生反应的离子方程式为
(2)下列关于二氧化碳的说法正确的是___________。
A.电子式为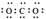 | B.空间填充模型为  |
| C.CO2 是极性分子, 能溶于水 | D.CO2 的水溶液能够导电,但 CO2是非电解质 |
(5)金刚石晶体中,每个C被
(6)晶体硅和碳化硅熔点较高的是
(7)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为
您最近一年使用:0次
名校
10 . 下列关于物质的结构或性质及解释都正确的是
| 选项 | 物质的结构或性质 | 解释 |
| A | 第一电离能:Zn>Cu | 元素金属性:Zn大于Cu |
| B | 熔点:SiO2>CO2 | 相对分子质量:SiO2大于CO2 |
| C | O2与O3分子极性相同 | 二者都是由非极性键构成的非极性分子 |
| D | 沸点:对羟基苯甲醛>邻羟基苯甲醛 | 对羟基苯甲醛形成分子间氢键,邻羟基苯甲醛形成分子内氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



