2024·上海·模拟预测
1 .  与环氧丙烷(
与环氧丙烷( )在一定条件下反应制得碳酸丙烯酯。
)在一定条件下反应制得碳酸丙烯酯。
 是
是(2)环氧丙烷中,O原子的杂化轨道类型是
(3)沸点:环氧丙烷
 (填“>”或“<”),解释其原因:
(填“>”或“<”),解释其原因:
您最近一年使用:0次
名校
解题方法
2 . 氮可形成多种化合物,其中三氯化氮NCl3)常温下是一种淡黄色液体,其分子星三角锥形,关于NCl3的叙述不正确的是
| A.NCl3晶体为共价晶体 | B.分子中N-Cl键是极性共价键 |
| C.NCl3晶体融化时破坏共价键 | D.NCl3中的原子都满足8电子的稳定结构 |
您最近一年使用:0次
名校
解题方法
3 . 硫及其化合物有许多用途,相关物质的物理常数如下表所示:
回答下列问题:
(1)SO2分子构型为“折线型”,则SO2是___________ (选填“极性”、“非极性”)分子,从结构的角度解释原因:___________ ;其在水中的溶解度比氯气___________ (选填“大”、“小”、“一样”)。
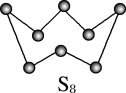
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是___________ ;下图为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因是___________ 。
| H2S | S8 | MnS | SO2 | SO3 | H2SO4 | |
| 熔点/℃ | -85.5 | 115.2 | >1600(分解) | -75.5 | 16.8 | 10.3 |
| 沸点/℃ | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
(1)SO2分子构型为“折线型”,则SO2是
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是
您最近一年使用:0次
2024-04-23更新
|
78次组卷
|
2卷引用:上海市华东师范大学第三附属中学2023-2024学年高二下学期期中考试 化学试题(等级考)
解题方法
4 . 下列关于肼的说法正确的是
A.电子式为 | B.既含极性键,又含非极性键 |
| C.属于极性分子 | D.N原子为sp2杂化 |
您最近一年使用:0次
解题方法
5 . SO2分子的空间结构和分子的极性分别为
| A.直线形,非极性 | B.直线形,极性 |
| C.角形,非极性 | D.角形,极性 |
您最近一年使用:0次
6 . 从硝酸工业中排放的氮氧化物NOx是一种大气污染物。最常见的吸收法是利用NaOH溶液吸收,发生以下方程:
①NO+NO2=N2O3
②N2O3+2NaOH=2NaNO2+H2O
③2NO2+2NaOH=NaNO2+___________+___________
实验表明,反应②发生的速率大于反应③发生的速率。
(1)补全方程式③并标出电子转移数目:___________ 。
2NO2+2NaOH=NaNO2+___________+___________
(2)NO2的分子构型和分子的极性分别为___________。
(3)C、N、O的第一电离能大小为___________ ,其原因是___________ 。
①NO+NO2=N2O3
②N2O3+2NaOH=2NaNO2+H2O
③2NO2+2NaOH=NaNO2+___________+___________
实验表明,反应②发生的速率大于反应③发生的速率。
(1)补全方程式③并标出电子转移数目:
2NO2+2NaOH=NaNO2+___________+___________
(2)NO2的分子构型和分子的极性分别为___________。
| A.直线形,非极性 | B.角形,极性 | C.平面三角形,非极性 | D.三角锥形,极性 |
您最近一年使用:0次
名校
解题方法
7 . 一定条件下(H2O)2•BF3可发生如图的转化:_______ ,属于_____ 分子(选填“极性”或“非极性”)。
(2) 中B原子采用杂化形式为
中B原子采用杂化形式为_______ 杂化。
(3)F-B-F键角大小:BF3_______  (选填>、=或<)。
(选填>、=或<)。
(4)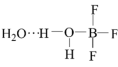 中不存在的微粒间相互作用是
中不存在的微粒间相互作用是_______ 。
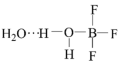


(2)
 中B原子采用杂化形式为
中B原子采用杂化形式为(3)F-B-F键角大小:BF3
 (选填>、=或<)。
(选填>、=或<)。(4)
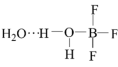 中不存在的微粒间相互作用是
中不存在的微粒间相互作用是| A.配位键 | B.氢键 | C.极性键 | D.非极性键 |
您最近一年使用:0次
名校
8 . 无机物可根据其组成和性质进行分类。现有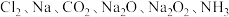 六种物质,完成下列填空:
六种物质,完成下列填空:
(1)由分子构成的单质是
(2)既有离子键又有共价键的物质的电子式为
(3)上述化合物中组成元素的原子半径由大到小的顺序是
(4)
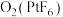 是离子化合物,其中
是离子化合物,其中 为
为 价。正确判断是___________。
价。正确判断是___________。| A.常温下为固体 | B.不存在共价键 | C.属于极性分子 | D.由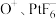 构成 构成 |
您最近一年使用:0次
9 . 火法冶炼是以黄铜矿(CuFeS2)为主要原料,下图是一种火法制备高纯度铜的工艺。

(1)黄铜矿熔炼过程中会发生反应:2CuFeS2+O2=Cu2S+2FeS+SO2.若2 mol CuFeS2参与反应,转移电子数目为_______ 。在上述反应中,SO2是_______ 。
A.氧化剂 B.还原剂 C.还原产物 D.氧化产物
(2)吹炼过程中,向熔融的冰铜中加入SiO2的目的是_______ 。
(3)粗铜经电解精炼可获得高纯度铜,下列说法正确的是
(4)关于SO2的说法正确的是
(5)煤中掺入一定量的生石灰,能减少煤燃烧排放的SO2,体现SO2具有
(6)冶铜烟气可以作为工业制硫酸为原料。下列的说法正确的是
(7)蔗糖遇浓硫酸会变成“黑面包”状,下列说法正确的是

(1)黄铜矿熔炼过程中会发生反应:2CuFeS2+O2=Cu2S+2FeS+SO2.若2 mol CuFeS2参与反应,转移电子数目为
A.氧化剂 B.还原剂 C.还原产物 D.氧化产物
(2)吹炼过程中,向熔融的冰铜中加入SiO2的目的是
(3)粗铜经电解精炼可获得高纯度铜,下列说法正确的是
| A.粗铜做阴极,发生氧化反应 |
| B.电解质溶液中铜离子向阴极移动 |
| C.利用阳极泥可回收Ag、Zn、Au等金属 |
| D.当电路中通过的电子数为NA时,阳极的质量变化一定是32 g |
(4)关于SO2的说法正确的是
| A.中心原子的杂化类型为sp2 | B.电负性:O<S |
| C.属于非极性分子 | D.价层电子对的空间结构为平面三角形 |
(5)煤中掺入一定量的生石灰,能减少煤燃烧排放的SO2,体现SO2具有
| A.漂白性 | B.酸性氧化物的性质 |
| C.氧化性 | D.还原性 |
(6)冶铜烟气可以作为工业制硫酸为原料。下列的说法正确的是
| A.500℃左右,转化器中反应的平衡转化率最大 |
| B.使用以铁为主的催化剂 |
| C.冶炼烟气在进入转化器之前,必须进行除尘、干燥等净化操作,防止催化剂中毒 |
| D.压强一般采用20~50MPa |
(7)蔗糖遇浓硫酸会变成“黑面包”状,下列说法正确的是
| A.蔗糖属于多糖 |
| B.在水浴条件下,蔗糖能与银氨溶液反应产生“银镜” |
| C.浓硫酸表现出脱水性、氧化性 |
| D.产生的气体通入品红溶液,溶液会褪色 |
您最近一年使用:0次
名校
10 . 科学家正在研究温室气体 和
和 的转化和利用。在
的转化和利用。在 基催化剂作用下,
基催化剂作用下, 和
和 反应可获得合成气
反应可获得合成气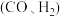 。
。
(1)基态 原子的电子排布式可简要表示为
原子的电子排布式可简要表示为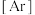
_____ 。
(2) 能与
能与 形成正四面体形的配位分子
形成正四面体形的配位分子 ,该分子属于
,该分子属于_____ 。
A.极性分子 B.非极性分子, 中含有
中含有_____  键。
键。
(3)已知 的燃烧热为
的燃烧热为 的燃烧热为
的燃烧热为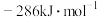 。用
。用 和
和 反应所得的合成气的热值(单位:
反应所得的合成气的热值(单位: )为多少?
)为多少?_____ (写出计算过程,体积按标准状况计算, )。
)。
一定条件下, 和
和 都能与
都能与 形成笼状结构的水合物晶体(如图),相关参数如表所示。
形成笼状结构的水合物晶体(如图),相关参数如表所示。

已知可燃冰形成过程可以表示为: 。
。
(4)“可燃冰”中分子间存在的作用有_____ 。
(5)目前已探明的可燃冰都分布在深海海底或永久冻土层深处,结合平衡原理解释这一现象_____ 。
(6)为开采深海海底的“可燃冰”,有科学家提出用 置换
置换 的设想。已知上图中笼状结构的空腔直径为
的设想。已知上图中笼状结构的空腔直径为 ,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
,根据上述图表,从物质结构及性质的角度分析,该设想的依据是_____ 。
 的晶胞呈立方体结构(如图),图中每一个小球代表一个
的晶胞呈立方体结构(如图),图中每一个小球代表一个 分子。
分子。

(7)甲烷晶体中,离一个甲烷分子最近的甲烷分子有_____。
(8)已知甲烷晶体密度为 ,晶胞的棱长为
,晶胞的棱长为 。则阿伏加德罗常数可以用含
。则阿伏加德罗常数可以用含 、a的代数式表示为
、a的代数式表示为
_____  。
。
 和
和 的转化和利用。在
的转化和利用。在 基催化剂作用下,
基催化剂作用下, 和
和 反应可获得合成气
反应可获得合成气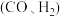 。
。(1)基态
 原子的电子排布式可简要表示为
原子的电子排布式可简要表示为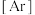
(2)
 能与
能与 形成正四面体形的配位分子
形成正四面体形的配位分子 ,该分子属于
,该分子属于A.极性分子 B.非极性分子,
 中含有
中含有 键。
键。(3)已知
 的燃烧热为
的燃烧热为 的燃烧热为
的燃烧热为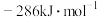 。用
。用 和
和 反应所得的合成气的热值(单位:
反应所得的合成气的热值(单位: )为多少?
)为多少? )。
)。一定条件下,
 和
和 都能与
都能与 形成笼状结构的水合物晶体(如图),相关参数如表所示。
形成笼状结构的水合物晶体(如图),相关参数如表所示。
分子直径/ | 分子与 的结合能 的结合能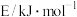 | |
 | 0.436 | 16.40 |
 | 0.512 | 29.91 |
 。
。(4)“可燃冰”中分子间存在的作用有
(5)目前已探明的可燃冰都分布在深海海底或永久冻土层深处,结合平衡原理解释这一现象
(6)为开采深海海底的“可燃冰”,有科学家提出用
 置换
置换 的设想。已知上图中笼状结构的空腔直径为
的设想。已知上图中笼状结构的空腔直径为 ,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
,根据上述图表,从物质结构及性质的角度分析,该设想的依据是 的晶胞呈立方体结构(如图),图中每一个小球代表一个
的晶胞呈立方体结构(如图),图中每一个小球代表一个 分子。
分子。
(7)甲烷晶体中,离一个甲烷分子最近的甲烷分子有_____。
| A.4个 | B.6个 | C.8个 | D.12个 |
(8)已知甲烷晶体密度为
 ,晶胞的棱长为
,晶胞的棱长为 。则阿伏加德罗常数可以用含
。则阿伏加德罗常数可以用含 、a的代数式表示为
、a的代数式表示为
 。
。
您最近一年使用:0次



