名校
1 . 关于 性质的解释合理的是
性质的解释合理的是
 性质的解释合理的是
性质的解释合理的是| 选项 | 性质 | 解释 |
| A | 比 容易液化 容易液化 |  分子间的范德华力更大 分子间的范德华力更大 |
| B | 熔点高于 |  键的键能比 键的键能比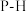 大 大 |
| C | 具有还原性 | 氮元素的化合价处于最低价 |
| D | 氨水中存在 |  是离子化合物 是离子化合物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 德国科学家发现新配方:他使用了远古地球上存在的 、
、 、
、 、
、 、
、 和HCN,再使用硫醇和铁盐等物质合成RNA的四种基本碱基。下列说法不正确的是
和HCN,再使用硫醇和铁盐等物质合成RNA的四种基本碱基。下列说法不正确的是
 、
、 、
、 、
、 、
、 和HCN,再使用硫醇和铁盐等物质合成RNA的四种基本碱基。下列说法不正确的是
和HCN,再使用硫醇和铁盐等物质合成RNA的四种基本碱基。下列说法不正确的是A.基态 价电子排布为 价电子排布为 | B. 、 、 、 、 分子间均存在氢键 分子间均存在氢键 |
C. 、 、 、HCN中均存在σ键和π键 、HCN中均存在σ键和π键 | D.沸点: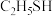 (乙硫醇) (乙硫醇) |
您最近一年使用:0次
2024-05-03更新
|
110次组卷
|
2卷引用:海南省文昌中学2023-2024学年高二下学期期中段考化学试题
名校
3 . 请用所学知识简单解释下列现象。
(1)四种晶体的熔点数据如表:
CF4和SiF4熔点相差较小,BF3和AlF3熔点相差较大,主要原因是_______ 。
(2)实验证明,金刚石、硅、锗的熔点和硬度依次下降,主要原因是_______ 。
(3)实验证明,接近水的沸点的水蒸气的相对分子质量测定值比按化学式H2O计算出来的相对分子质量大一些,主要原因是______ 。
(1)四种晶体的熔点数据如表:
| 物质 | CF4 | SiF4 | BF3 | AlF3 |
| 熔点/℃ | -183 | -90 | -127 | >1000 |
(2)实验证明,金刚石、硅、锗的熔点和硬度依次下降,主要原因是
(3)实验证明,接近水的沸点的水蒸气的相对分子质量测定值比按化学式H2O计算出来的相对分子质量大一些,主要原因是
您最近一年使用:0次
名校
4 . 下列对有关事实的解释错误的是
| 事 实 | 解 释 | |
| A. | BF3与NH3形成配合物[H3N→BF3] | BF3中的B有空轨道接受NH3中N的孤电子对 |
| B. | 邻羟基苯甲醛比对羟基苯甲醛的沸点低 | 前者形成分子内氢键,后者形成分子间氢键 |
| C. | 壁虎在天花板上爬行自如 | 壁虎足与墙体之间存在范德华力 |
| D. | DNA是超分子 | DNA中两条分子链之间通过化学键的作用而组合在一起 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 下列关于分子间作用力的说法正确的是
| A.范德华力是短程作用力,分子之间距离太远可忽略 |
B. 比 比 稳定是因为水分子间存在氢键 稳定是因为水分子间存在氢键 |
| C.氢键具有方向性和饱和性,属于化学键的一种 |
| D.卤素单质、卤素氢化物的熔、沸点均随着相对分子质量的增大而增大 |
您最近一年使用:0次
名校
解题方法
6 . 青霉胺可以用于医学上误食铜盐的解毒,解毒原理: 形成环状配合物,其结构如图所示。该配合物无毒、易溶于水,可经尿液排出。下列说法正确的是
形成环状配合物,其结构如图所示。该配合物无毒、易溶于水,可经尿液排出。下列说法正确的是
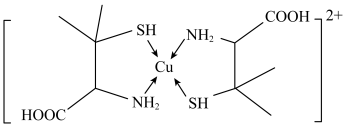
 形成环状配合物,其结构如图所示。该配合物无毒、易溶于水,可经尿液排出。下列说法正确的是
形成环状配合物,其结构如图所示。该配合物无毒、易溶于水,可经尿液排出。下列说法正确的是
A.共价键键角的大小关系为: |
B.电负性大小关系为: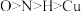 |
| C.该配合物易溶于水的主要原因是其与水可形成分子间氢键 |
D.与铜离子形成配位键强弱的大小关系为: |
您最近一年使用:0次
名校
7 . 下列事实与相应的物质的化学键键能大小无关的是
A.沸点: | B.活泼性: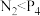 |
C.热稳定性: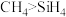 | D.硬度:金刚石>晶体硅 |
您最近一年使用:0次
名校
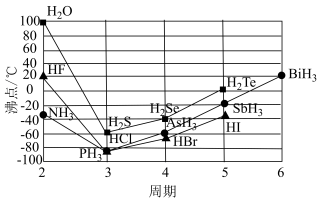
8 . 下图为第ⅤA族、ⅥA、ⅦA族元素简单氢化物沸点随周期数的递变趋势图。
(1)解释第ⅤA族元素氢化物沸点变化的趋势:___________ ,推测ⅣA族 与
与 的沸点大小为
的沸点大小为
___________  (填“>”或“<”)。
(填“>”或“<”)。
(2)接近水的沸点的水蒸气的相对分子质量测定值比按化学式 计算出的相对分子质量大一些,原因为
计算出的相对分子质量大一些,原因为___________ 。
(3) 常用于制备半导体材料,
常用于制备半导体材料, 与足量的
与足量的 加热可反应得到
加热可反应得到 ,写出该反应的化学方程式
,写出该反应的化学方程式___________ 。通过___________ 的实验分析方法可测出 的键长键角信息,下列关于
的键长键角信息,下列关于 分子的说法正确的是
分子的说法正确的是___________ 。
A.中心原子价层电子对数为5对
B.分子的空间构型为正四面体
C.中心原子的杂化方式为 杂化
杂化
(1)解释第ⅤA族元素氢化物沸点变化的趋势:
 与
与 的沸点大小为
的沸点大小为
 (填“>”或“<”)。
(填“>”或“<”)。(2)接近水的沸点的水蒸气的相对分子质量测定值比按化学式
 计算出的相对分子质量大一些,原因为
计算出的相对分子质量大一些,原因为(3)
 常用于制备半导体材料,
常用于制备半导体材料, 与足量的
与足量的 加热可反应得到
加热可反应得到 ,写出该反应的化学方程式
,写出该反应的化学方程式 的键长键角信息,下列关于
的键长键角信息,下列关于 分子的说法正确的是
分子的说法正确的是A.中心原子价层电子对数为5对
B.分子的空间构型为正四面体
C.中心原子的杂化方式为
 杂化
杂化
您最近一年使用:0次
2023-12-27更新
|
227次组卷
|
2卷引用:海南省海口市海南中学2023-2024学年高二上学期期中考试化学试题
名校
9 . 下图是三种结构相似的有机物。

(1)推测有机物沸点:对羟基苯乙酰胺___________ 邻羟基苯乙酰胺(填“>”或“<”),推测有机物水溶性:邻羟基苯乙酰胺___________ 邻羟基苯乙酰氯(填“>”或“<”)。
(2)推测键长
___________  (填“>”或“<”),
(填“>”或“<”), 对羟基苯乙酰胺分子中所含的σ键的物质的量为
对羟基苯乙酰胺分子中所含的σ键的物质的量为___________ 。
(3)邻羟基苯乙酰胺中除氢原子外的其他原子是否一定共平面:___________ (填“是”或“否”)
(4)现有分别装有上述三种物质的三个试剂瓶失去了标签,哪种仪器分析方法可以鉴别出三种物质中的邻羟基苯乙酰氯___________
A.红外光谱法 B.质谱法 C.X射线衍射实验
(5)抗坏血酸结构如图所示,推测抗坏血酸在水中的溶解性:___________ (填“难溶”或“易溶”于水;坏血酸分子有___________ 个手性碳原子。


(1)推测有机物沸点:对羟基苯乙酰胺
(2)推测键长

 (填“>”或“<”),
(填“>”或“<”), 对羟基苯乙酰胺分子中所含的σ键的物质的量为
对羟基苯乙酰胺分子中所含的σ键的物质的量为(3)邻羟基苯乙酰胺中除氢原子外的其他原子是否一定共平面:
(4)现有分别装有上述三种物质的三个试剂瓶失去了标签,哪种仪器分析方法可以鉴别出三种物质中的邻羟基苯乙酰氯
A.红外光谱法 B.质谱法 C.X射线衍射实验
(5)抗坏血酸结构如图所示,推测抗坏血酸在水中的溶解性:

您最近一年使用:0次
名校
解题方法
10 . 硼(B)及其化合物在化学中有重要的地位。请回答下列问题:
(1)硼酸( )是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
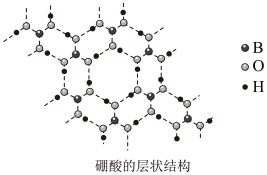
①硼酸中B原子的杂化轨道类型为______ 。
②硼酸晶体中存在的作用力有范德华力和______ 。
③加热时,硼酸的溶解度增大,主要原因是______ 。
④硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的OH而呈酸性。写出硼酸的电离方程式:____________ 。
(2)硼氢化钠( )是有机化学中的一种常用还原剂,
)是有机化学中的一种常用还原剂,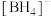 的空间构型是
的空间构型是______ 。
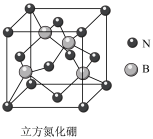
(3)立方氮化硼的晶胞如图,与金刚石相似,已知晶胞边长为361.5pm,则立方氮化硼的密度是______ g·cm 。(只要求列计算式,不必计算出数值,阿伏加德罗常数用
。(只要求列计算式,不必计算出数值,阿伏加德罗常数用 表示)。
表示)。
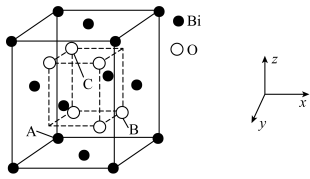
(4) 的立方晶胞结构如图3所示,以A点为原点建立分数坐标,已知A点坐标为
的立方晶胞结构如图3所示,以A点为原点建立分数坐标,已知A点坐标为 ,B点坐标为
,B点坐标为 ,则C点坐标为
,则C点坐标为______ 。
(1)硼酸(
 )是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
①硼酸中B原子的杂化轨道类型为
②硼酸晶体中存在的作用力有范德华力和
③加热时,硼酸的溶解度增大,主要原因是
④硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的OH而呈酸性。写出硼酸的电离方程式:
(2)硼氢化钠(
 )是有机化学中的一种常用还原剂,
)是有机化学中的一种常用还原剂,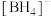 的空间构型是
的空间构型是(3)立方氮化硼的晶胞如图,与金刚石相似,已知晶胞边长为361.5pm,则立方氮化硼的密度是
 。(只要求列计算式,不必计算出数值,阿伏加德罗常数用
。(只要求列计算式,不必计算出数值,阿伏加德罗常数用 表示)。
表示)。
(4)
 的立方晶胞结构如图3所示,以A点为原点建立分数坐标,已知A点坐标为
的立方晶胞结构如图3所示,以A点为原点建立分数坐标,已知A点坐标为 ,B点坐标为
,B点坐标为 ,则C点坐标为
,则C点坐标为
您最近一年使用:0次



