名校
解题方法
1 . 对下列事实的解释不正确 的是
| 选项 | 事实 | 解释 |
| A | 稳定性:HF>HI | HF分子间存在氢键,HI分子间不存在氢键 |
| B | 键角:NH >H2O >H2O | 中心原子均采取sp3杂化,孤电子对有较大的斥力 |
| C | 熔点:石英>干冰 | 石英是共价晶体,干冰是分子晶体;共价键比分子间作用力强 |
| D | 酸性:CF3COOH>CCl3COOH | F的电负性大于Cl,F-C的极性大于Cl-C,使F3C-的极性大于Cl3C-的极性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-01更新
|
1839次组卷
|
13卷引用:天津经济技术开发区第一中学2023-2024学年高三上学期开学检测化学试题
天津经济技术开发区第一中学2023-2024学年高三上学期开学检测化学试题天津市第二十中学2022-2023学年高二下学期期中考试化学试题天津市滨海新区2023届普通高考第三次模拟检测化学试题北京市东城区2023届一模考试化学试题河南省实验中学2022-2023学年高二下学期期中考试化学试题安徽省颍上第一中学2022-2023学年高二下学期5月月考化学试题北京市第二十中学2023-2024学年高三上学期10月月考化学试题海南省海口市第一中学2023-2024学年高二上学期第一次月考化学试题北京市铁路第二中学2023-2024学年高三上学期期中考试化学试题北京市第八中学2023-2024学年高三上学期12月月考化学试题(已下线)热点07 分子晶体与共价晶体河南省济源一中2022-2023学年高二下学期5月月考化学试题浙江省杭州地区(含周边)重点高中2023-2024学年高二下学期4月期中考试化学试题
名校
2 . 化学家屠呦呦团队在确认青蒿素分子结构之后实现了青蒿素的全合成,如图所示。已知:Bn-即为C6H5CH2-;部分条件和步骤已省略。
(1)A的分子式为____ ,其所含含氧官能团名称为____ 。E→F的反应类型为___ 。
(2)A的同系物中含碳原子数目最少的物质的结构式为____ 。
(3)B的同分异构体X含有醚键和碳碳双键,其中核磁共振氢谱有2组峰,则符合该条件的X的所有结构有____ 种,写出其中一种X的结构简式:____ 。
(4)写出A与新制氢氧化铜加热反应的化学方程式:___ 。
(5)通过H→I的反应,分子中引入了硫醚基团,而J→K的反应,分子中硫醚基团又被脱去,这样做的目的是____ 。
(6)科学家将青蒿素还原转化为疗效更好的双氢青蒿素,如图所示,从结构视角解释双氢青蒿素的水溶性比青蒿素的强的原因是____ 。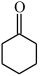 为主要原料,经四步反应制备
为主要原料,经四步反应制备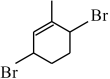 的流程:
的流程:___ 。

(1)A的分子式为
(2)A的同系物中含碳原子数目最少的物质的结构式为
(3)B的同分异构体X含有醚键和碳碳双键,其中核磁共振氢谱有2组峰,则符合该条件的X的所有结构有
(4)写出A与新制氢氧化铜加热反应的化学方程式:
(5)通过H→I的反应,分子中引入了硫醚基团,而J→K的反应,分子中硫醚基团又被脱去,这样做的目的是
(6)科学家将青蒿素还原转化为疗效更好的双氢青蒿素,如图所示,从结构视角解释双氢青蒿素的水溶性比青蒿素的强的原因是

 为主要原料,经四步反应制备
为主要原料,经四步反应制备 的流程:
的流程:
您最近一年使用:0次
2022-06-01更新
|
339次组卷
|
2卷引用:天津经济技术开发区第一中学2023-2024学年高三上学期开学检测化学试题
名校
解题方法
3 . 教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
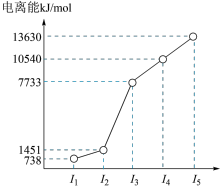
(1)第三周期的某主族元素,其第一至第五电离能数据如图所示,则该元素对应的原子有________ 种不同运动状态的电子。
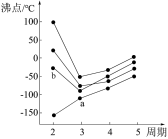
(2)如图所示,每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a代表的是________ (写化学式)。
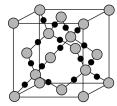
(3) 在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于
在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于________ 晶体。
(4)第一电离能介于Al、P之间的第三周期元素有________ 种。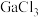 中中心原子的杂化方式为
中中心原子的杂化方式为________ 。
(5) 的一种配离子
的一种配离子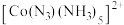 中,
中, 的配位数是
的配位数是________ ,配体的空间结构分别为________ 。
(6)金属磷化物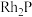 (化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图所示,已知晶胞参数为
(化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图所示,已知晶胞参数为 ,则晶体的密度为
,则晶体的密度为________ (列式即可)。

(1)第三周期的某主族元素,其第一至第五电离能数据如图所示,则该元素对应的原子有

(2)如图所示,每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a代表的是

(3)
 在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于
在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于
(4)第一电离能介于Al、P之间的第三周期元素有
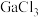 中中心原子的杂化方式为
中中心原子的杂化方式为(5)
 的一种配离子
的一种配离子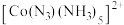 中,
中, 的配位数是
的配位数是(6)金属磷化物
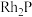 (化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图所示,已知晶胞参数为
(化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图所示,已知晶胞参数为 ,则晶体的密度为
,则晶体的密度为
您最近一年使用:0次
名校
4 . 下列说法不正确 的是
| A.通过X射线衍射可测定青蒿素晶体的结构 |
| B.利用盐析的方法可将蛋白质从溶液中分离 |
| C.邻羟基苯甲醛在水中的溶解度高于对羟基苯甲醛在水中的溶解度 |
| D.可用新制氢氧化铜悬浊液鉴别苯、乙醇、乙醛、甲酸和醋酸溶液 |
您最近一年使用:0次
名校
5 . A、B、C、D、E是中学化学中的常见物质,A、B是短周期元素组成的单质。其转化关系如下:

若C是能使湿润的红色石蕊试纸变蓝的气体,D是黄绿色气体。下列说法正确的是

若C是能使湿润的红色石蕊试纸变蓝的气体,D是黄绿色气体。下列说法正确的是
| A.组成C的分子中心原子杂化轨道类型为sp2杂化,分子为三角锥形 |
| B.E物质中可能是含有离子键和共价键 |
| C.C、D均极易溶于水,是由于氢键的原因 |
| D.反应中D得到1.2 mol电子时,在标准状况下生成B气体2.24 L |
您最近一年使用:0次
2021-03-06更新
|
189次组卷
|
2卷引用:天津市杨村第一中学2020-2021学年高三下学期开学开学考试化学试题
名校
解题方法
6 . 下列叙述正确的是
| A.所有的σ键的强度都比π键的大 |
| B.常规晶胞的顶角原子是 8 个晶胞共用的 |
| C.H2O、H2S、H2Se 的相对分子质量依次增大,熔点依次增大 |
| D.基态原子的核外电子填充在 6 个轨道中的元素有 3 种 |
您最近一年使用:0次
名校
7 . 原子结构与性质
(1)元素As与N同族。As的氢化物沸点比NH3的___ (填“高”或“低”),其判断理由是______ 。
(2)铜原子在基态时的价电子排布式为______ 。
(3)Fe是人体需要补充的元素之一,试写出Fe2+的核外电子排布式:_____ 。与Al同一周期的Na、Mg元素也是人体所需元素,Na、Mg、Al基态原子第一电离能的大小关系____ 。某同学所画基态镁原子的核外电子排布图如图 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了______ 。
(4)K元素处于元素周期表的____ 区,其基态原子中,核外电子占据的电子云轮廓图为球形的能级有____ 个。
(1)元素As与N同族。As的氢化物沸点比NH3的
(2)铜原子在基态时的价电子排布式为
(3)Fe是人体需要补充的元素之一,试写出Fe2+的核外电子排布式:
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(4)K元素处于元素周期表的
您最近一年使用:0次
2019-09-27更新
|
204次组卷
|
2卷引用:天津市六校(天津中学、南开中学、实验中学等)2020届高三上学期期初检测化学试题
名校
解题方法
8 . 甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应的水化物为强酸。下列说法不正确 的是
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A.原子半径:丁>戊>乙 |
| B.乙的简单氢化物的沸点一定高于戊的简单氢化物的沸点 |
| C.甲的简单氢化物遇氯化氢一定有白烟产生 |
| D.丙的最高价氧化物对应的水化物一定能与强碱反应 |
您最近一年使用:0次



