名校
1 . 用 表示阿伏加德罗常数。下列说法不正确的是
表示阿伏加德罗常数。下列说法不正确的是
 表示阿伏加德罗常数。下列说法不正确的是
表示阿伏加德罗常数。下列说法不正确的是A.常温常压下相同体积的 和 和 所含的分子数相同 所含的分子数相同 |
B.物质的量相同的 和 和 所含的质子数相同 所含的质子数相同 |
C. 金刚石中 金刚石中 键数和 键数和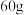 石英晶体中 石英晶体中 键数均为 键数均为 |
D.标准状况下, 丙烯中 丙烯中 键数为 键数为 , , 键数为 键数为 |
您最近一年使用:0次
名校
2 . 有关晶体的结构如图所示,下列说法中不正确的是

A.在NaCl晶体中,距 最近的 最近的 有6个,距 有6个,距 最近且相等的 最近且相等的 共12个 共12个 |
B.在 晶体中,每个晶胞平均占有4个 晶体中,每个晶胞平均占有4个 , , 的配位数是8 的配位数是8 |
| C.在金刚石晶体中,每个碳原子以共价键与4个碳原子相连,金刚石内部碳原子和共价键的比例为1∶2 |
| D.该气态团簇分子的分子式为EF或FE,其晶体不导电 |
您最近一年使用:0次
名校
解题方法
3 . 下表给出了几种物质的熔点和沸点:
下列说法中,错误的是
 |  |  | 单质B | |
| 熔点/℃ | 801 | 710 | -68 | 2300 |
| 沸点/℃ | 1465 | 1418 | 57 | 2500 |
A. 是分子晶体 是分子晶体 | B.单质B可能是共价晶体 |
C. 时, 时, 呈气态 呈气态 | D. 水溶液不能导电 水溶液不能导电 |
您最近一年使用:0次
2022-08-22更新
|
1009次组卷
|
6卷引用:北京教育学院附属中学2022-2023学高三上学期10月测试 化学试题
北京教育学院附属中学2022-2023学高三上学期10月测试 化学试题专题3 微粒间作用力与物质性质 专题强化练3 微粒间作用力的判断及对物质性质的影响专题强化练7 晶体熔、沸点高低的比较(已下线)3.2.2 共价晶体-同步学习必备知识新疆乌鲁木齐市第101中学2022-2023学年高二下学期4月期中化学试题(已下线)热点08 金属晶体和离子晶体
4 . 下列说法正确的是
| A.HF和Br2分子中均含有s-pσ键 |
| B.沸点:H2O<H2S<H2Se<H2Te |
| C.硬度:晶体硅>碳化硅>金刚石 |
| D.酸性:CF3COOH>CCl3COOH>CH3COOH |
您最近一年使用:0次
2022-07-10更新
|
680次组卷
|
3卷引用:北京市首都师范大学附属中学2021-2022学年高二下学期期末考试化学试题
5 . 硅烷SiH4可用于制造高纯硅。采用硅化镁法制备SiH4的化学方程式如下:Mg2Si+4NH4Cl+8NH3=SiH4+2MgCl2·6NH3
(1)硅在元素周期表中的位置是___________ ,基态硅原子占据的最高能级的符号是___________ 。
(2)①SiH4的电子式是___________ 。
②SiH4的沸点比CH4的___________ 。(填“高”或“低”),原因是___________ 。
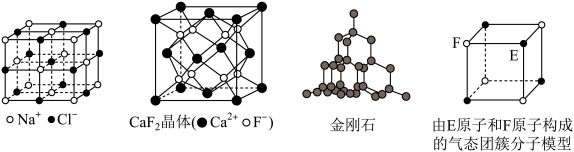
(3)Mg2Si可由Mg和SiO2反应制得。晶体SiO2属于___________ 晶体(填晶体类型),一种SiO2晶体的结构中有顶角相连的硅氧四面体形成螺旋上升的长链(如图)。其中Si原子的杂化轨道类型是___________ 。
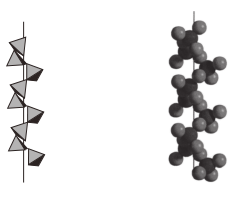
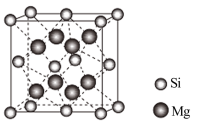
(4)Mg2Si晶体的晶胞示意图如下。每个Mg原子位于Si原子组成的四面体的中心。则1个Si原子周围有___________ 个紧邻的Mg原子。已知Mg2Si的晶胞边长为acm,阿伏加德罗常数的值为NA,则Mg2Si晶体的密度为___________ g·cm-3。
(1)硅在元素周期表中的位置是
(2)①SiH4的电子式是
②SiH4的沸点比CH4的
(3)Mg2Si可由Mg和SiO2反应制得。晶体SiO2属于

(4)Mg2Si晶体的晶胞示意图如下。每个Mg原子位于Si原子组成的四面体的中心。则1个Si原子周围有

您最近一年使用:0次
2022-01-14更新
|
635次组卷
|
7卷引用:北京市西城区2021~2022学年高三上学期期末考试化学试题
名校
解题方法
6 . 碳族中的碳、硅、锗及其化合物在多领域有重要用途。
(1)基态 的电子排布式为
的电子排布式为___________ 。
(2)我国科学家研发的“液态阳光”计划是通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。 分子中存在
分子中存在___________ 个 键和
键和___________ 个 键,
键, 分子是
分子是___________ 分子(填“极性”或“非极性”)。
(3)关于 、
、 及其化合物的结构与性质,下列论述
及其化合物的结构与性质,下列论述不正确 的是___________。
(4) 与
与 -甲基咪唑(
-甲基咪唑(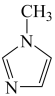 )反应可以得到
)反应可以得到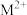 ,其结构如下图所示:
,其结构如下图所示:

 -甲基咪唑中碳原子的杂化轨道类型有
-甲基咪唑中碳原子的杂化轨道类型有___________ 。
(5)汞( )、锗(
)、锗( )、锑(
)、锑( )形成的一种新物质
)形成的一种新物质 为潜在的拓扑绝缘体材料。
为潜在的拓扑绝缘体材料。 的晶体(晶胞为下图
的晶体(晶胞为下图 )可视为
)可视为 晶体(晶胞为下图
晶体(晶胞为下图 )中部分
)中部分 原子被
原子被 和
和 取代后形成。
取代后形成。
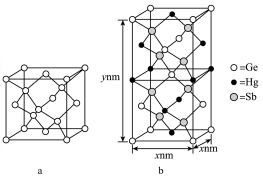
 的最简式的相对分子质量为
的最简式的相对分子质量为 ,阿伏加德罗常数的数值为
,阿伏加德罗常数的数值为 ,则
,则 晶体的密度为
晶体的密度为___________  (列出计算式)。注:
(列出计算式)。注:
(1)基态
 的电子排布式为
的电子排布式为(2)我国科学家研发的“液态阳光”计划是通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。
 分子中存在
分子中存在 键和
键和 键,
键, 分子是
分子是(3)关于
 、
、 及其化合物的结构与性质,下列论述
及其化合物的结构与性质,下列论述A.键能 、 、 ,因此 ,因此 稳定性小于 稳定性小于 |
B. 是与金刚石结构相似的共价晶体,因此 是与金刚石结构相似的共价晶体,因此 具有较高的硬度 具有较高的硬度 |
C. 中 中 的化合价为 的化合价为 , , 中 中 的化合价为 的化合价为 ,因此 ,因此 还原性小于 还原性小于 |
D. 原子间难形成双键和三键而 原子间难形成双键和三键而 原子间可以,是因为 原子间可以,是因为 的原子半径大于 的原子半径大于 ,因此难以形成 ,因此难以形成 键 键 |
 与
与 -甲基咪唑(
-甲基咪唑( )反应可以得到
)反应可以得到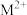 ,其结构如下图所示:
,其结构如下图所示:
 -甲基咪唑中碳原子的杂化轨道类型有
-甲基咪唑中碳原子的杂化轨道类型有(5)汞(
 )、锗(
)、锗( )、锑(
)、锑( )形成的一种新物质
)形成的一种新物质 为潜在的拓扑绝缘体材料。
为潜在的拓扑绝缘体材料。 的晶体(晶胞为下图
的晶体(晶胞为下图 )可视为
)可视为 晶体(晶胞为下图
晶体(晶胞为下图 )中部分
)中部分 原子被
原子被 和
和 取代后形成。
取代后形成。
 的最简式的相对分子质量为
的最简式的相对分子质量为 ,阿伏加德罗常数的数值为
,阿伏加德罗常数的数值为 ,则
,则 晶体的密度为
晶体的密度为 (列出计算式)。注:
(列出计算式)。注:
您最近一年使用:0次
7 . 下列各组晶体物质中,化学键类型相同,晶体类型也相同的是
①SiO2和SO3 ②金刚石和白磷 ③CO2和SO2 ④晶体硅和金刚石⑤晶体氖和晶体氮 ⑥硫黄和单质碘
①SiO2和SO3 ②金刚石和白磷 ③CO2和SO2 ④晶体硅和金刚石⑤晶体氖和晶体氮 ⑥硫黄和单质碘
| A.③④⑥ | B.④⑤⑥ | C.①②③ | D.①③⑤ |
您最近一年使用:0次
2021-05-11更新
|
493次组卷
|
9卷引用:北京市房山区2021-2022学年高二下学期期中考试化学试题
北京市房山区2021-2022学年高二下学期期中考试化学试题辽宁省锦州市黑山县黑山中学2019-2020学年高二6月月考化学试题(已下线)第三章 晶体结构与性质【过关测试提高卷】-2020-2021学年高二化学单元复习(人教版选择性必修2)宁夏吴忠中学2020-2021学年高二下学期期中考试化学试题四川省资阳中学校2021-2022学年高二上学期期中考试化学试题(已下线)第3.2.1讲 分子晶体-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)新疆巴楚县第一中学2021-2022学年高二下学期 3月月考化学试题陕西省宝鸡市金台区2022-2023学年高二下学期期末考试化学试题新疆伊犁州霍城县江苏中学2023-2024学年高二下学期3月月考化学试题
8 . 金刚石和石墨的物理性质存在着较大差异,原因是( )
| A.它们是由不同种元素构成的 | B.他们各自的原子排列方式不同 |
| C.它们具有不同的几何外形 | D.石墨能导电而金刚石不能 |
您最近一年使用:0次
2020-11-18更新
|
388次组卷
|
4卷引用:北京市第四十三中学2020-2021学年高二下学期第一次月考化学试题
9 . 下列物质的熔点均按由高到低的次序排列,其原因是由于键能由大到小排列的是
| A.铝、钠、干冰 | B.金刚石、碳化硅、晶体硅 |
| C.碘化氢、溴化氢、氯化氢 | D.二氧化硅、二氧化碳、一氧化碳 |
您最近一年使用:0次
2020-08-05更新
|
333次组卷
|
10卷引用:北京市汇文中学2021-2022学年高二下学期期中考试化学试题
北京市汇文中学2021-2022学年高二下学期期中考试化学试题(已下线)2011-2012学年福建省上杭一中高二下学期期末考试化学试卷(已下线)2012年鲁科版高中化学选修3 3.2金属晶体与离子晶体练习卷【全国百强校】福建省莆田第一中学2017-2018学年高二下学期期中考试化学试题【全国百强校】河南省林州市第一中学2018-2019学年高二下学期5月月考化学试题云南省盈江县第一高级中学2019-2020学年高二上学期期末考试化学试题辽宁省丹东市第四中学2019-2020学年高二 4 月线上月考化学试题辽宁省六校协作体2019-2020高二下学期期初考试化学试卷黑龙江省鸡西市鸡东县第二中学2019-2020 学年高二下学期期末考试化学试题高二选择性必修2(人教版2019)第三章 晶体结构与性质 专题2 晶体类型的判断与晶胞结构的有关计算
10 . 下列关于C、Si及其化合物结构与性质的论述错误的是
A.键能 、 、 ,因此C2H6稳定性大于Si2H6 ,因此C2H6稳定性大于Si2H6 |
| B.立方型SiC是与金刚石成键、结构均相似的共价晶体,因此具有很高的硬度 |
| C.SiH4中Si的化合价为+4,CH4中C的化合价为-4,因此SiH4还原性小于CH4 |
D.Si原子间难形成双键而C原子间可以,是因为Si的原子半径大于C,难形成 键 键 |
您最近一年使用:0次
2020-07-11更新
|
7455次组卷
|
37卷引用:北京市第八十中学2023届高三下学期二模适应考试化学试题
北京市第八十中学2023届高三下学期二模适应考试化学试题2020年山东省高考化学试卷(新高考)(已下线)专题17 物质结构与性质(选修)-2020年高考真题和模拟题化学分项汇编河南省长葛市第一高级中学2021届高三上学期10月阶段性测试化学试题山东省淄博市般阳中学2020-2021学年高二上学期期中考试化学试题四川省乐山十校2020-2021学年高二上学期半期联考化学试题(已下线)小题必刷22 元素周期表(律)及其应用——2021年高考化学一轮复习小题必刷(通用版)河北省石家庄市第二十四中学2021届高三上学期月考化学试卷(人教版2019)选择性必修2 第三章 晶体结构与性质 C 高考挑战区(已下线)热点4 物质结构与性质(选择题)-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)专题11 物质结构与性质——备战2021年高考化学纠错笔记(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练山东省夏津第一中学2020-2021学年高二下学期3月月考化学试题(已下线)押山东卷第04题 物质结构与性质选择题-备战2021年高考化学临考题号押题(山东卷)福建省福州第一中学2020-2021学年高二下学期期中考试化学试题(已下线)考点35 晶体结构与性质-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)专题13 物质结构与性质基础-备战2022年高考化学真题及地市好题专项集训【山东专用】(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)福建省厦门集美中学2021-2022学年高二下学期第一次月考化学试题(已下线)卷14 物质结构与性质选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)押新高考卷08题 物质结构与性质-备战2022年高考化学临考题号押题(新高考通版)(已下线)卷03 小题素养卷-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)2020年山东卷化学高考真题变式题1-10抚顺市第一中学2021-2022学年高二下学期开学考试化学试题河南省南阳市第六完全学校高级中学2021-2022学年高二下学期4月月考化学试题四川省安岳县兴隆中学2021-2022学年高二上学期期中测试化学试题江苏省苏州市2022-2023学年高二上学期期中调研化学试卷江西省景德镇一中2022-2023学年高二上学期期中考试化学试题四川省乐山沫若中学2022-2023学年高二上学期第二次月考(期中考试)化学试题福建省厦门市湖滨中学2022-2023学年高三上学期期中考试化学试题山东省菏泽市单县二中2021-2022学年高二下学期开学考试 化学试题(已下线)专题33 物质结构与性质基础-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第五章 物质结构与性质 元素周期律 第31讲 晶体结构与性质广东广雅中学2022-2023学年高二下学期期中考试化学试题广东省湛江市第二中学2021-2022学年高二下学期第17周(6.11)周练化学试题(已下线)第3讲 化学键 共价键的类型及键参数宁夏回族自治区银川市贺兰县第一中学2023-2024学年高三第三阶段化学考试



