1 . 设  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是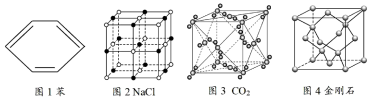
A.每摩尔苯中含有碳碳双键的数目为  |
B. 晶体中含有 晶体中含有  分子的数目为 分子的数目为  |
C. (干冰) 晶胞中含有的共用电子对的数目为 (干冰) 晶胞中含有的共用电子对的数目为  |
D. 金刚石含有的碳碳单键的数目为 金刚石含有的碳碳单键的数目为  |
您最近一年使用:0次
2 . 下列各组物质性质的比较,结论正确的是
A.在水中的溶解度: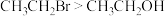 |
B.晶体熔点:碳化硅 晶体硅 晶体硅 |
C.酸性: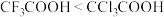 |
D.沸点:正戊烷 新戊烷 新戊烷 |
您最近一年使用:0次
名校
3 . 化学与能源、材料和环境密切相关。下列有关说法错误的是
| A.中国空间站使用的推进器燃料为氙气(Xe),Xe是第五周期元素 |
| B.水结冰体积膨胀有利于水生生物,是因为水分子间存在氢键 |
| C.我国自主研发的“深地一号”为进军万米深度提供核心装备而制造钻头用的金刚石为共价晶体 |
| D.BaSO4俗称“钡餐”,常用作X射线透视肠胃造影剂,Ba元素位于周期表d区 |
您最近一年使用:0次
名校
解题方法
4 . 元素周期表中第ⅢA族元素的单质及其化合物应用广泛,下列说法不正确的是
A. 属于原子晶体 属于原子晶体 |
B. 中存在配位键 中存在配位键 |
C. 分子间能形成氢键 分子间能形成氢键 |
D.基态Tl原子的价电子排布式为 |
您最近一年使用:0次
名校
解题方法
5 .  表示阿伏加德罗常数,下列说法不正确的是
表示阿伏加德罗常数,下列说法不正确的是
 表示阿伏加德罗常数,下列说法不正确的是
表示阿伏加德罗常数,下列说法不正确的是A.31g白磷中,含有 个磷磷键 个磷磷键 | B.12g金刚石中,含有 个碳碳键 个碳碳键 |
C.12g石墨中,含有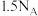 个碳碳键 个碳碳键 | D.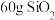 晶体中,含有 晶体中,含有 个硅氧键 个硅氧键 |
您最近一年使用:0次
名校
解题方法
6 . 下列有关晶体的叙述中,正确的是
| A.晶体中只要有阳离子就一定有阴离子 |
B.金刚石、SiC、NaF、NaCl、 、 、 晶体的熔点依次降低 晶体的熔点依次降低 |
| C.金刚石的三维骨架结构中,由共价键形成的最小碳环上有4个碳原子 |
D.氯化钠晶体中,每个 周围紧邻且距离相等的 周围紧邻且距离相等的 所形成的结构为正四面体形 所形成的结构为正四面体形 |
您最近一年使用:0次
2022-04-28更新
|
163次组卷
|
3卷引用:重庆市万州纯阳中学校2021-2022学年高二下学期5月月考化学试题
解题方法
7 . A、B、C、D、E、F六种元素均位于元素周期表的前四周期,且原子序数依次增大。元素A是原子半径最小的元素;B元素基态原子的核外电子占据四个原子轨道;D元素原子的成对电子总数是未成对电子总数的3倍;E与D位于同一主族;F位于第Ⅷ族,在地壳中含量排金属中第二位。
(1)F2+的价电子排布图为_______ 。
(2)B、C、D元素的第一电离能由大到小的顺序是_______ (用元素符号表示)。
(3)B、C、D的某些氢化物的分子中都含有18个电子,B的这种氢化物的中心原子杂化方式为_______ ,等物质的量B、C、D的这种氢化物的分子中含有σ键的个数之比为_______ 。
(4)D常见的两种单质D2和D3,其中_______ (填化学式)在水中的溶解度更大。
(5)B、E可形成分子式为BE2的化合物,其电子式为_______ 。
(6)实验室合成一种由B和C两种元素形成的化合物,该化合物具有三维骨架结构,其中每个B原子与4个C原子形成共价键,每个C原子与3个B原子形成共价键。其化学式为_______ , 预测该化合物熔点_______ 金刚石(填“高于”或“低于”)。
(1)F2+的价电子排布图为
(2)B、C、D元素的第一电离能由大到小的顺序是
(3)B、C、D的某些氢化物的分子中都含有18个电子,B的这种氢化物的中心原子杂化方式为
(4)D常见的两种单质D2和D3,其中
(5)B、E可形成分子式为BE2的化合物,其电子式为
(6)实验室合成一种由B和C两种元素形成的化合物,该化合物具有三维骨架结构,其中每个B原子与4个C原子形成共价键,每个C原子与3个B原子形成共价键。其化学式为
您最近一年使用:0次
8 . 晶体的结构和性质是人们研究晶体的重要方向。
(1)硅元素可形成多种晶体。
①硅与氯、溴结合能形成SiCl4、SiBr4,二者沸点高低顺序为_______ ,原因是_______ 。
②晶体Si和晶体SiC结构相似,二者熔点高低顺序为_______ ,原因是_______ 。
(2)晶胞结构的认识可帮助我们认识微粒间的空间位置关系及作用力。
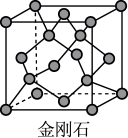
①金刚石的晶胞结构如图所示,则1个金刚石晶胞中含有_______ 个碳原子。
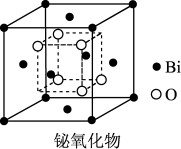
②铋的某种氧化物的立方晶胞结构如图所示,该铋的氧化物的化学式为_______ 。
③已知FeP的晶胞结构如图所示:

A、B点的原子坐标如图所示,则C点的原子坐标为_______ 。
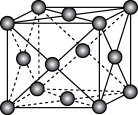
④铁形成的某种晶体的晶胞如图所示,该晶胞中Fe原子的配位数为_______ ,若该晶胞的边长为apm,则其密度为_______ g/cm3(NA表示阿伏加德罗常数的值,列出计算式即可)。
(1)硅元素可形成多种晶体。
①硅与氯、溴结合能形成SiCl4、SiBr4,二者沸点高低顺序为
②晶体Si和晶体SiC结构相似,二者熔点高低顺序为
(2)晶胞结构的认识可帮助我们认识微粒间的空间位置关系及作用力。
①金刚石的晶胞结构如图所示,则1个金刚石晶胞中含有

②铋的某种氧化物的立方晶胞结构如图所示,该铋的氧化物的化学式为

③已知FeP的晶胞结构如图所示:

A、B点的原子坐标如图所示,则C点的原子坐标为
④铁形成的某种晶体的晶胞如图所示,该晶胞中Fe原子的配位数为

您最近一年使用:0次
名校
解题方法
9 . 碳族元素(Carbongroup)是位于元素周期表IVA族的元素,包括碳(C)、硅(Si)、锗(Ge),锡(Sn)、铅(Pb)、鈇(Fl)六种。请回答:
(1)鈇(Fl),其命名是为了纪念苏联原子物理学家乔治弗洛伊洛夫,是一种人工合成的放射性化学元素,它的化学符号是Uuq,它的原子序数是_______ , 属于弱金属之一。
(2)基态锡原子价电子的轨道表示式为_______ ;与Ge同周期且未成对电子数相同的元素还有_______ 种。
(3)碱金属元素是位于元素周期表第IA族(除氢外)的元素。第一电离能(I1)的变化趋势是自上而下依次减小,其原因是_______ 。
(4)石英玻璃(非晶态二氧化硅)和水晶(晶态二氧化硅)外观很相似,可通过_______ 法进行科学区分。
(5)金刚石和石墨是碳元素形成的常见单质,下列关于这两种单质的对比叙述中正确的有_______ 。
a.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化
b.晶体中共价键的键长:金刚石中C-C<石墨中C-C
c.晶体的熔点:金刚石>石墨
d. 晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力
f. 金刚石和石墨的熔点都很高,所以金刚石和石墨都是共价晶体
g. 在金刚石和石墨的结构中, 由共价键形成的最小碳环均是六元环
(6)三氯甲烷(CHCl3)常温下为无色透明液体。有特殊气味,味甜,低毒,有麻醉性,有致癌可能性。三氯甲烷的是_______ 分子(选填“极性”或“非极性”), 碳元素的化合价是_______ 。
(1)鈇(Fl),其命名是为了纪念苏联原子物理学家乔治弗洛伊洛夫,是一种人工合成的放射性化学元素,它的化学符号是Uuq,它的原子序数是
(2)基态锡原子价电子的轨道表示式为
(3)碱金属元素是位于元素周期表第IA族(除氢外)的元素。第一电离能(I1)的变化趋势是自上而下依次减小,其原因是
(4)石英玻璃(非晶态二氧化硅)和水晶(晶态二氧化硅)外观很相似,可通过
(5)金刚石和石墨是碳元素形成的常见单质,下列关于这两种单质的对比叙述中正确的有
a.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化
b.晶体中共价键的键长:金刚石中C-C<石墨中C-C
c.晶体的熔点:金刚石>石墨
d. 晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力
f. 金刚石和石墨的熔点都很高,所以金刚石和石墨都是共价晶体
g. 在金刚石和石墨的结构中, 由共价键形成的最小碳环均是六元环
(6)三氯甲烷(CHCl3)常温下为无色透明液体。有特殊气味,味甜,低毒,有麻醉性,有致癌可能性。三氯甲烷的是
您最近一年使用:0次
名校
10 . 设NA为阿伏加德罗常数的值。下列说法不正确的是
| A.12g金刚石中含有C-C的个数为2NA |
| B.124g白磷(P4)晶体中含有P-P的个数为6NA |
| C.18g冰中含有氢键的个数为4NA |
| D.SiO2晶体中1mol硅原子可与氧原子形成4NA个共价键(Si-O) |
您最近一年使用:0次
2022-03-19更新
|
363次组卷
|
5卷引用:重庆市万州第二高级中学2021-2022学年高二下学期3月考试化学试题



