解题方法
1 . 过渡金属在生产、生活、科技等方面有着广泛的应用。例如仿生簇化合物Mn4XO4(X=Ca2+/Y3+/Gd3+)有望为实现利用太阳能和水获取清洁能源(氢能)开辟新途径,MnOx·Na2WO4·SiO2、钴(Co)的合金及其化合物材料等广泛应用于化工催化剂等领域。
请回答下列问题:
(1)基态钇(39Y)的价层电子排布式为_______ 。
(2)基态Co原子核外有_______ 种运动状态不同的电子,其3d能级上有_______ 对成对电子。
(3)[Co(NO2)6]3-中三种元素的第一电离能由大到小的顺序是_______ (填元素符号)。已知:[Co(CN)6]4-是强还原剂,与水反应能生成[Co(CN)6]3-。[Co(CN)6]4-中含有σ键与π键的数目之比为_______ ,[Co(CN)6]3-中C的杂化方式为_______ 。
(4)[Mn(NH3)2]2+中配体分子的立体构型是_______ 。[Mn(NH3)2]2+中键角∠HNH_______ (填“大于” 、“小于”或“等于”)NH3中键角∠HNH。
(5)MnF2、MnCl2晶体的熔点分别为856 °C、650 °C,二者熔点存在明显差异的主要原因是_______ 。
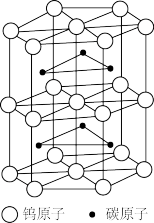
(6)碳化钨是一种由钨(W)和碳组成的晶体,其晶体结构如图所示,晶体的熔点为2870° C,硬度与金刚石相当。碳化钨的晶体类型是_______ ;已知:碳化钨晶体的密度为ρg·cm-3,NA为阿伏加德罗常数的值,六棱柱高为a cm,则底边长为_______ (用含ρ、a、N的表达式表示)nm。
请回答下列问题:
(1)基态钇(39Y)的价层电子排布式为
(2)基态Co原子核外有
(3)[Co(NO2)6]3-中三种元素的第一电离能由大到小的顺序是
(4)[Mn(NH3)2]2+中配体分子的立体构型是
(5)MnF2、MnCl2晶体的熔点分别为856 °C、650 °C,二者熔点存在明显差异的主要原因是
(6)碳化钨是一种由钨(W)和碳组成的晶体,其晶体结构如图所示,晶体的熔点为2870° C,硬度与金刚石相当。碳化钨的晶体类型是

您最近一年使用:0次
2022-05-27更新
|
409次组卷
|
5卷引用:河北省秦皇岛市2022届高三三模化学试题
河北省秦皇岛市2022届高三三模化学试题河南省2022届高三下学期仿真模拟大联考理科综合化学试题(已下线)新疆博乐高级中学2022届高三第一次诊断性测试理科综合化学试卷广东省部分学校2022届高三下学期高考冲刺化学试题(已下线)专题17 物质结构与性质(综合题)-2022年高考真题模拟题分项汇编
2022·河北·模拟预测
解题方法
2 . 叠氮化物是一类重要化合物,在炸药、磁性化合物研究、微量元素测定等方面越来越引起人们的重视,其中氢叠氮酸( )是一种弱酸,分子结构示意图可表示为
)是一种弱酸,分子结构示意图可表示为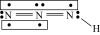 ,联氨被亚硝酸氧化时便可生成氢叠氮酸(
,联氨被亚硝酸氧化时便可生成氢叠氮酸( ):
): ,它的酸性类似于醋酸,微弱电离出
,它的酸性类似于醋酸,微弱电离出 和
和 。试回答下列问题:
。试回答下列问题:
(1)下列有关说法正确的是___________(填序号)。
(2)叠氮化物能与部分金属离子形成配合物,如 ,在该配合物中钴显
,在该配合物中钴显___________ 价,根据价层电子对互斥理论可知 的空间构型为
的空间构型为___________ ,写出钴原子在基态时的核外电子排布式:___________ 。
(3)与 互为等电子体的分子有
互为等电子体的分子有___________ (举2例)。
(4)人造立方氮化硼的硬度仅次于金刚石而远远高于其他材料,因它与金刚石统称为超硬材料。立方氮化硼晶胞如图所示,试分析:

①该晶体的类别为___________ 晶体。
②晶体中每个N原子同时吸引___________ 个B原子。
③设该晶体的摩尔质量为Mg/mol,晶体的密度为 ,阿伏加德罗常数的值为NA,则晶体中两个距离最近的B原子之间的距离为
,阿伏加德罗常数的值为NA,则晶体中两个距离最近的B原子之间的距离为___________ cm。
 )是一种弱酸,分子结构示意图可表示为
)是一种弱酸,分子结构示意图可表示为 ,联氨被亚硝酸氧化时便可生成氢叠氮酸(
,联氨被亚硝酸氧化时便可生成氢叠氮酸( ):
): ,它的酸性类似于醋酸,微弱电离出
,它的酸性类似于醋酸,微弱电离出 和
和 。试回答下列问题:
。试回答下列问题:(1)下列有关说法正确的是___________(填序号)。
A. 中含有5个σ键 中含有5个σ键 |
B. 中三个氮原子采用的都是sp2杂化 中三个氮原子采用的都是sp2杂化 |
C. 、 、 、 、 , , 都是极性分子 都是极性分子 |
D.肼( )沸点高达113.5℃,说明肼分子间可形成氢键 )沸点高达113.5℃,说明肼分子间可形成氢键 |
 ,在该配合物中钴显
,在该配合物中钴显 的空间构型为
的空间构型为(3)与
 互为等电子体的分子有
互为等电子体的分子有(4)人造立方氮化硼的硬度仅次于金刚石而远远高于其他材料,因它与金刚石统称为超硬材料。立方氮化硼晶胞如图所示,试分析:

①该晶体的类别为
②晶体中每个N原子同时吸引
③设该晶体的摩尔质量为Mg/mol,晶体的密度为
 ,阿伏加德罗常数的值为NA,则晶体中两个距离最近的B原子之间的距离为
,阿伏加德罗常数的值为NA,则晶体中两个距离最近的B原子之间的距离为
您最近一年使用:0次
3 . 据古籍《燕闲清赏笺》记载:“宣窑之青,乃苏勃泥青”,说明宣德时期青花瓷使用的颜料是“苏勃泥青”,它是从一种钻毒砂[主要成分:( ,
, )
) ]中提取出来的。回答下列问题:
]中提取出来的。回答下列问题:
(1)基态S原子的价层电子排布图为_______ ,其原子核外电子共有_______ 种空间运动状态。
(2)比较元素第一电离能:S_______ P(填“>”、“<”或=)。
(3) 位于周期表的第
位于周期表的第_______ 周期 _______ 族,_______ (填“d”或“ds”)区。
(4)区分晶体与非晶体最可靠的科学方法是_______ 。
(5)砷化镓晶胞结构如图所示。晶胞中 与周围最近且等距的
与周围最近且等距的 形成的空间结构为
形成的空间结构为_______ 。已知 晶胞棱长为apm,其密度
晶胞棱长为apm,其密度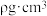 ,则阿伏加德罗常数的数值为
,则阿伏加德罗常数的数值为_______ (列出计算式即可, 的摩尔质量为
的摩尔质量为 )。
)。

(6) 的熔点为
的熔点为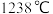 ,
, 与
与 晶体类型相同,
晶体类型相同, 的熔点
的熔点_______ (填“>”、“<”或“=”)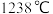 。
。
 ,
, )
) ]中提取出来的。回答下列问题:
]中提取出来的。回答下列问题:(1)基态S原子的价层电子排布图为
(2)比较元素第一电离能:S
(3)
 位于周期表的第
位于周期表的第(4)区分晶体与非晶体最可靠的科学方法是
(5)砷化镓晶胞结构如图所示。晶胞中
 与周围最近且等距的
与周围最近且等距的 形成的空间结构为
形成的空间结构为 晶胞棱长为apm,其密度
晶胞棱长为apm,其密度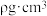 ,则阿伏加德罗常数的数值为
,则阿伏加德罗常数的数值为 的摩尔质量为
的摩尔质量为 )。
)。
(6)
 的熔点为
的熔点为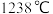 ,
, 与
与 晶体类型相同,
晶体类型相同, 的熔点
的熔点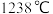 。
。
您最近一年使用:0次
名校
解题方法
4 . 生命起源假说认为,在地球生命形成初期(约36亿年前),由NH3、CO、H2O、H2、H2S等小分子在放电条件下形成了多种氨基酸,继而合成了蛋白质而形成单细胞。
(1)写出基态S原子的价电子排布式____ ,其基态原子具有____ 种不同能量的电子。
(2)H2S的沸点低于H2O的沸点,其原因是____ 。
(3)NH3的VSEPR模型名称为____ ,H2O分子中孤对电子占据2个____ 杂化轨道。
(4)太阳能电池种类繁多,如铜铟镓硒镍薄膜太阳能电池等。1molNi(CO)4中π键与σ键的个数比为____ 。高温下CuO容易转化为Cu2O,试从原子结构角度解释原因:____ 。
(5)①金刚石的晶胞如图,其中C原子的配位数是____ ;晶体硅、金刚砂(SiC)的结构与之相似,则金刚石、晶体硅、金刚砂的熔点由高到低的排列顺序是____ (用化学式表示);

②金刚石的晶胞参数为a pm。 1cm3晶体的平均质量为___ g(只要求列出算式,阿伏加德罗常数值为NA)
(1)写出基态S原子的价电子排布式
(2)H2S的沸点低于H2O的沸点,其原因是
(3)NH3的VSEPR模型名称为
(4)太阳能电池种类繁多,如铜铟镓硒镍薄膜太阳能电池等。1molNi(CO)4中π键与σ键的个数比为
(5)①金刚石的晶胞如图,其中C原子的配位数是

②金刚石的晶胞参数为a pm。 1cm3晶体的平均质量为
您最近一年使用:0次
2020-11-20更新
|
543次组卷
|
2卷引用:四川省遂宁市2021届高三零诊考试理综化学试题



