解题方法
1 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.标况下, 己烯中含有的 己烯中含有的 数为0.2NA 数为0.2NA | B.5.85g氯化钠晶体中含有的氯化钠分子数为0.1NA |
| C.1mol乙醇中含有的极性键数为8NA | D.60gSiO2中含有的Si-O键数为4NA |
您最近一年使用:0次
2022-07-14更新
|
156次组卷
|
2卷引用:福建省三明市2021-2022学年高二下学期期末质量检测化学试题
解题方法
2 . 科学家成功将 转化为类似
转化为类似 结构的共价晶体,下列说法正确的是
结构的共价晶体,下列说法正确的是
 转化为类似
转化为类似 结构的共价晶体,下列说法正确的是
结构的共价晶体,下列说法正确的是A. 共价晶体易升华 共价晶体易升华 |
B. 共价晶体硬度小于 共价晶体硬度小于 |
C. 共价晶体中C原子的杂化方式为sp 共价晶体中C原子的杂化方式为sp |
D. 由分子晶体转化为共价晶体是化学变化 由分子晶体转化为共价晶体是化学变化 |
您最近一年使用:0次
3 . 下列说法正确的是
| A | B | C | D |
 |  |  |  |
| 一个NaCl晶胞中含有6个Na+和6个Cl- | CaF2晶胞中F-配位数为8,Ca2+配位数为4 | 二氧化硅晶体中,硅原子与硅氧键个数比为1:2 | 石墨晶体是层状结构,图中7个六元环完全占有的碳原子数为14 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 灰锡是金刚石型立方晶体,其结构如下图。下列说法不正确的是


| A.灰锡是分子晶体 | B.Sn原子间以共价键相结合 |
| C.灰锡中Sn原子的配位数是4 | D.Sn原子围成的最小环上有6个Sn原子 |
您最近一年使用:0次
2022-07-06更新
|
142次组卷
|
3卷引用:福建省宁德市2021-2022学年高二下学期期末质量检测化学试题
名校
解题方法
5 . 下列对一些实验事实的理论解释正确的是
| 选项 | 实验事实 | 理论解释 |
| A | CsCl晶体中阳离子和阴离子都有确定的配位数 | 离子键具有饱和性 |
| B | 环状 分子结构如图 分子结构如图 | 原子采取的杂化方式为 |
| C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
| D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-06-30更新
|
182次组卷
|
2卷引用:福建省福州第一中学2021-2022学年高二下学期期中考试化学试题
名校
6 . NA表示阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,2.24L苯中含有的分子数为0.1NA |
| B.14g乙烯和环丁烷(C4H8)的混合气体含有的碳氢共价键数为2NA |
| C.18g冰中含有的氢键的数目为4NA |
| D.1molSiO2晶体中所含的Si-O键的数目为2NA |
您最近一年使用:0次
7 . 下列我国科研成果所涉及材料中,是共价晶体的是
 |  |  |  |
| A.4.03米大口径碳化硅反射镜 | B.2022年冬奥会聚氨酯速滑服 | C.能屏蔽电磁波的碳包覆银纳米线 | D.“玉兔二号”钛合金筛网轮 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-05-04更新
|
159次组卷
|
2卷引用:福建省三明第一中学2021-2022学年高二下学期第二次月考化学试题
解题方法
8 . 观察下列模型并结合有关信息,判断下列说法正确的是
| 干冰 | BN | SiO2 | NaCl | |
| 结构模型示意图 | 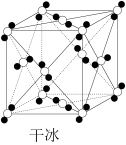 | 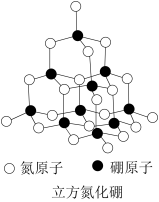 |  | 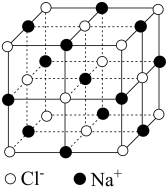 |
| A.44g干冰中含有NA个晶胞结构单元 |
| B.立方氮化硼含有σ键和π键,所以硬度大 |
| C.SiO2晶体和NaCl晶体中微粒的排列方式均为紧密堆积形式 |
| D.NaCl晶体中每个Na+周围距离相等且最近的Na+有12个 |
您最近一年使用:0次
9 . 下列关于晶体结构和性质的叙述错误的是


A.在 晶体中,Cs+的配位数为8 晶体中,Cs+的配位数为8 |
B.在 晶体中,距Na+最近的Cl-形成正八面体 晶体中,距Na+最近的Cl-形成正八面体 |
| C.干冰晶体中,每个CO2分子周围紧邻6个CO2分子 |
D.在二氧化硅晶体中,平均每个 原子形成4个 原子形成4个 键,且每个Si被12个环共用 键,且每个Si被12个环共用 |
您最近一年使用:0次
2022-04-25更新
|
161次组卷
|
2卷引用:福建省南安市侨光中学、昌财实验中学2021-2022学年高二下学期第4次联考(期中)化学试题
名校
解题方法
10 . 下列各物质中,按熔点由高到低的顺序排列正确的是
| A.CH4>SiH4>GeH4>SnH4 | B.KCl>NaCl>MgCl2>MgO |
| C.SiCl4>MgBr2>BN | D.金刚石>晶体硅>钠 |
您最近一年使用:0次
2022-04-25更新
|
119次组卷
|
3卷引用:福建省南安市侨光中学、昌财实验中学2021-2022学年高二下学期第4次联考(期中)化学试题



