1 . 中国科学院物理研究所合成了基于铁基超导体系掺杂调控的新型稀磁半导体LiZnqMnpAs(图乙),该材料是LiZnAs晶体(如图甲所示立方晶胞)中部分Zn原子被Mn原子代替后制成的。已知a点原子的分数坐标为(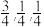 ),图甲晶体的密度为dg·cm-3,晶胞参数为cpm。下列说法错误的是
),图甲晶体的密度为dg·cm-3,晶胞参数为cpm。下列说法错误的是
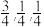 ),图甲晶体的密度为dg·cm-3,晶胞参数为cpm。下列说法错误的是
),图甲晶体的密度为dg·cm-3,晶胞参数为cpm。下列说法错误的是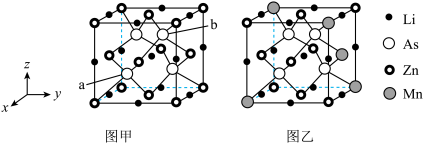
A.b点As原子的分数坐标为(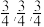 ) ) |
| B.图乙晶体的最简化学式为LiZn0.75Mn0.25As |
| C.图乙晶胞结构中的As位于Zn、Mn形成的正四面体空隙中 |
D.阿伏加德罗常数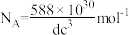 |
您最近一年使用:0次
2023-08-31更新
|
496次组卷
|
4卷引用:湖南省张家界市慈利县第一中学2023-2024学年高三上学期第二次月考化学试卷
2 . 金是一种贵重金属,抗腐蚀,是延展性最好的金属之一。负载型金纳米材料在催化动态催化理论、光学、电子学等方面有重要作用。
Ⅰ.金的结构
(1)金元素位于元素周期表第6周期ⅠB族,金的价电子排布式为_______ 。
(2)金晶体的晶胞为面心立方晶胞,Au在晶胞中的配位数是_______ 。
Ⅱ.金的提取
硫脲(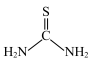 )液相提金原理:
)液相提金原理:
(3)硫脲易溶于水,原因是_______ 。
Ⅲ.金的应用
一种最稳定的负载型纳米金团簇,具有最完美的对称性,其结构如图所示:
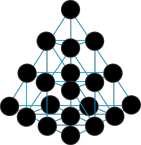
(4)该金团簇的化学式为_______ (填字母)。
a.Au b.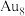 c.
c.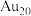
(5)该金团簇中有_______ 种不同化学环境的金原子。
Ⅰ.金的结构
(1)金元素位于元素周期表第6周期ⅠB族,金的价电子排布式为
(2)金晶体的晶胞为面心立方晶胞,Au在晶胞中的配位数是
Ⅱ.金的提取
硫脲(
 )液相提金原理:
)液相提金原理:
(3)硫脲易溶于水,原因是
Ⅲ.金的应用
一种最稳定的负载型纳米金团簇,具有最完美的对称性,其结构如图所示:

(4)该金团簇的化学式为
a.Au b.
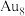 c.
c.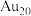
(5)该金团簇中有
您最近一年使用:0次
3 . 某纳米钛铝合金晶胞结构如图甲(Al、Ti各有1个原子在晶胞内部),金属铬的晶胞如图乙所示,已知铬的密度为ρg•cm-3,阿伏加德罗常数为NA。下列说法中正确的是


| A.甲中Al与Ti原子个数比为11∶5 |
| B.1个基态Ti原子中含有4个未成对电子 |
| C.乙中与铬原子距离最近的铬原子共有12个 |
D.铬原子的半径r= × ×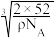 ×1010pm ×1010pm |
您最近一年使用:0次
名校
解题方法
4 . 下列有关晶体堆积模型和晶胞的说法错误的是


| A.图①、图②和图③都是最密堆积,图④的空间占有率是图中最小的 |
| B.从左至右的配位数依次为12、12、12、6、8 |
| C.图①可以表示氯化钠晶胞中氯离子的堆积方式 |
| D.铜晶体、碳化硅晶体中的硅原子、硫化锌晶体中的硫离子都采用图③中的最密堆积 |
您最近一年使用:0次
名校
解题方法
5 . “愚人金”因在野外很容易被误认为黄金而得名,其中一种主要成分是 ,可用于炼铜,流程如图:
,可用于炼铜,流程如图:

以下说法正确的是
 ,可用于炼铜,流程如图:
,可用于炼铜,流程如图:
以下说法正确的是
| A.铜元素在元素周期表中位于第四周期IB族 |
| B.冰铜中主要金属元素的化合价都是+2 |
| C.基态S原子核外电子的运动状态有5种 |
| D.铜晶胞类型为面心立方晶胞,晶胞中Cu的配位数是8 |
您最近一年使用:0次
名校
解题方法
6 . 几种离子晶体的晶胞如图所示,下列说法正确的是
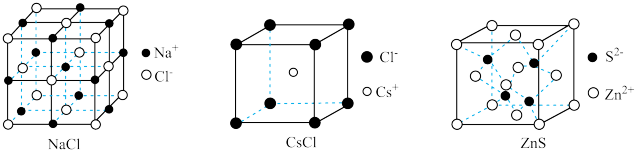

| A.熔沸点:NaCl<CsCl |
B.NaCl晶胞中, 做面心立方最密堆积, 做面心立方最密堆积, 填充正四面体空隙 填充正四面体空隙 |
C.若ZnS的晶胞边长为a pm,则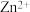 与 与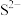 之间的最近距离为 之间的最近距离为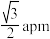 |
| D.上述三种晶胞中,阳离子的配位数:ZnS<NaCl<CsCl |
您最近一年使用:0次
名校
7 . 在照相底片定影时,Na2S2O3溶液能溶解未起反应的AgBr,这是因为Ag+与S2O 生成配离子,Ag+的配位数为2。下列说法不正确的是
生成配离子,Ag+的配位数为2。下列说法不正确的是

 生成配离子,Ag+的配位数为2。下列说法不正确的是
生成配离子,Ag+的配位数为2。下列说法不正确的是
A.Ag+与S2O 结合成配离子,使反应AgBr(s) 结合成配离子,使反应AgBr(s) Ag+(aq)+Br-(aq)平衡向右移动 Ag+(aq)+Br-(aq)平衡向右移动 |
| B.上述反应生成配合物的化学方程式为AgBr+2Na2S2O3=Na3[Ag(S2O3)2]+NaBr |
C.Ag+与S2O 反应时,Ag+提供空轨道,S2O 反应时,Ag+提供空轨道,S2O 提供孤电子对,二者通过配位键结合 提供孤电子对,二者通过配位键结合 |
| D.如图为单质银的晶胞(面心立方最密堆积),银原子的配位数为6 |
您最近一年使用:0次
名校
8 . 已知X、Y、Z、W、Q是原子序数依次增大的前四周期元素。X原子核外有6种不同运动状态的电子;Y基态原子中s电子总数与p电子总数相等;Z最高价氧化物对应水化物的碱性在同周期元素中最强;W基态原子的最外层p轨道有2个电子的自旋状态与其他电子的自旋状态相反。
(1)基态X原子中电子占据的最高能级的原子轨道形状为_______ 。原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态X原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态X原子,其核外电子自旋磁量子数的代数和为_______ 。
(2)Y、Z、W的简单离子半径由大到小的顺序为_______ 。(用离子符号表示)
(3)Q是生活中使用最广泛的一种金属。
①Q的原子结构示意图为_______ 。
②检验溶液中是否含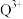 离子的试剂是
离子的试剂是_______ (填化学式),现象为_______ 。
③Q的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的截面图是_______ (填字母序号)。
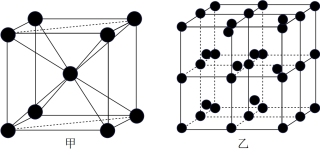
A.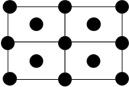 B.
B.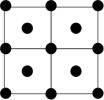 C.
C.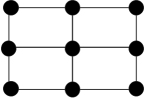 D.
D.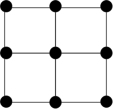
(1)基态X原子中电子占据的最高能级的原子轨道形状为
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态X原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态X原子,其核外电子自旋磁量子数的代数和为(2)Y、Z、W的简单离子半径由大到小的顺序为
(3)Q是生活中使用最广泛的一种金属。
①Q的原子结构示意图为
②检验溶液中是否含
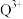 离子的试剂是
离子的试剂是③Q的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的截面图是

A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
9 . 硼、铝、镓、铟、铊位于元素周期表第ⅢA族,统称为硼族元素,它们的单质及化合物在工农业生产中有着重要的应用。
(1)基态镓原子的外围电子排布式为_______ 。
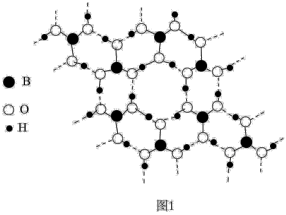
(2)硼酸晶体具有层状结构,每一层的平面层状结构如图1所示。硼酸分子中B原子采取_______ 杂化;晶体平面层内所含有作用力类型有_______ 。
(3)工业上通常用电解法冶炼铝。已知Al2O3熔点为2054℃、AlCl3熔点为194℃,冶炼铝时应选择电解熔融_______ (填化学式),理由是_______ 。
(4)冰晶石(Na3AlF6)是炼铝的助熔剂,由两种离子构成,其中阴离子具有正八面体结构,写出该阴离子的化学式_______ ,与该阴离子互为等电子体的分子有_______ 。
(5)铊具有三种晶体结构:低于230℃时为六方最密堆积(α-Tl),230℃以上转化为体心立方堆积(β-Tl),在高压下形成面心立方最密堆积(γ-Tl),晶胞结构如图2所示。
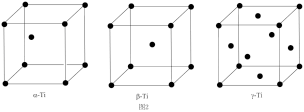
三种铊的晶体中,铊的配位数之比(α:β:γ)为_______ .若铊原子半径为a pm,则β-Tl中铊原子间最短距离为_______ pm (用含a的式子表示,下同),γ-Tl晶体的密度计算式为ρ=_______ g/cm3(设NA为阿伏加德罗常数的值)。
(1)基态镓原子的外围电子排布式为
(2)硼酸晶体具有层状结构,每一层的平面层状结构如图1所示。硼酸分子中B原子采取

(3)工业上通常用电解法冶炼铝。已知Al2O3熔点为2054℃、AlCl3熔点为194℃,冶炼铝时应选择电解熔融
(4)冰晶石(Na3AlF6)是炼铝的助熔剂,由两种离子构成,其中阴离子具有正八面体结构,写出该阴离子的化学式
(5)铊具有三种晶体结构:低于230℃时为六方最密堆积(α-Tl),230℃以上转化为体心立方堆积(β-Tl),在高压下形成面心立方最密堆积(γ-Tl),晶胞结构如图2所示。

三种铊的晶体中,铊的配位数之比(α:β:γ)为
您最近一年使用:0次
名校
解题方法
10 . X、Y、Z、M为原子序数依次增大的四种短周期主族元素,Y与M同主族,X的一种1∶2型氢化物分子中既有 键又有π键,且所有原子共平面;Y的基态原子L层上有2个未成对电子;Z元素的原子在同周期原子中半径最大。下列说法正确的是
键又有π键,且所有原子共平面;Y的基态原子L层上有2个未成对电子;Z元素的原子在同周期原子中半径最大。下列说法正确的是
 键又有π键,且所有原子共平面;Y的基态原子L层上有2个未成对电子;Z元素的原子在同周期原子中半径最大。下列说法正确的是
键又有π键,且所有原子共平面;Y的基态原子L层上有2个未成对电子;Z元素的原子在同周期原子中半径最大。下列说法正确的是A.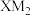 中心原子的杂化方式为sp 中心原子的杂化方式为sp | B.晶体Z的堆积方式为简单立方堆积 |
C.与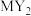 互为等电子体的分子有 互为等电子体的分子有 | D.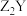 和 和 中化学键类型完全相同 中化学键类型完全相同 |
您最近一年使用:0次
2021-07-09更新
|
546次组卷
|
2卷引用:云南省曲靖市第一中学2023-2024学年高二下学期3月月考化学试题



