名校
解题方法
1 . 回答下列问题。
(1)蒸馏操作实验仪器:铁架台、酒精灯、石棉网、___________ 、温度计、___________ 、牛角管(尾接管)、锥形瓶。
(2)实验装置与注意事项___________ ,不少于___________ ;
②加入沸石或碎瓷片,防止___________ ;
③温度计水银球应与蒸馏烧瓶的___________ ;
④冷凝水应___________ 进入,___________ 流出;
⑤实验开始时,先___________ ,后___________ ;
实验结束时,先停止加热,后停止通冷凝水;
(1)蒸馏操作实验仪器:铁架台、酒精灯、石棉网、
(2)实验装置与注意事项
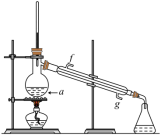
②加入沸石或碎瓷片,防止
③温度计水银球应与蒸馏烧瓶的
④冷凝水应
⑤实验开始时,先
实验结束时,先停止加热,后停止通冷凝水;
您最近一年使用:0次
名校
解题方法
2 . 完成下列问题。
(1)下列做法中,符合“低碳”理念的是________ (填字母序号)
A.开发使用新能源汽车 B.“焚烧法”处理垃圾 C.大力发展火力发电
D.使用太阳能热水器 E.大力发展风力发电
(2)幼儿和青少年缺___________ 会患佝偻病和发育不良。
(3)如图是A、B、C三种物质的溶解度曲线图。请回答:

①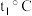 时,溶解度相等的两种物质是
时,溶解度相等的两种物质是________ 。
②B的饱和溶液中混有少量的物质A,要除去A得到较纯的B物质,可采用的结晶方法是___________ 。
③如图所示,在大烧杯中加入一定量的硝酸铵固体后,甲试管内出现的现象是___________ ,乙试管内的溶液为___________ (填“饱和”或“不饱和”)溶液。

(1)下列做法中,符合“低碳”理念的是
A.开发使用新能源汽车 B.“焚烧法”处理垃圾 C.大力发展火力发电
D.使用太阳能热水器 E.大力发展风力发电
(2)幼儿和青少年缺
(3)如图是A、B、C三种物质的溶解度曲线图。请回答:

①
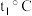 时,溶解度相等的两种物质是
时,溶解度相等的两种物质是②B的饱和溶液中混有少量的物质A,要除去A得到较纯的B物质,可采用的结晶方法是
③如图所示,在大烧杯中加入一定量的硝酸铵固体后,甲试管内出现的现象是

您最近一年使用:0次
解题方法
3 . 回答下列小题
(1)中国科学院天津工业生物技术研究所在《科学》杂志发表论文,表示其研究团队首次在实验室实现了二氧化碳到淀粉〔(C6H10O5)n〕的人工合成。
①人工合成淀粉过程为:在催化剂的作用下,将二氧化碳和氢气转化为甲醇(CH3OH)和水,再经过铰复杂的变化将甲醇转化为淀粉。请写出该过程中,二氧化碳和氢气反应生成甲醇的化学方程式:___________ 。
②甲醇常温下是一种无色液体,易溶于水,沸点64.7℃。要将甲醇从其水溶液中分离出来,可以采用___________ (选填“过滤”“蒸馏”之一)的方法。
③根据质量守恒定律,用以上方法生产32g甲醇,至少需要CO2的质量为___________ g。
④绿色植物通过光合作用也可以合成淀粉,该过程是绿色植物将光能转化为___________ 能。
⑤生活中检验淀粉可以选用___________ (选填“碘酒”“食醋”“酒精”之一)。
(2)1926年我国化学家侯德榜创立了“侯氏制减法”,使原料NaC1的利用率从70%提高到96%,也使原来的副产物CaCl2转化成化肥NH4Cl。Na2CO3和NaCl的溶解度曲线如右图所示,请回答下列问题:

①以NaCl为原料制取纯碱(Na2CO3),从元素守恒的观点来看,还需要补充___________ 元素(填元素名称)。
②将t2℃时相同质量的Na2CO3饱和溶液和NaC1饱和溶液均降温至t1℃,此时所得两溶液的溶质质量分数相比较为___________ (选填“前者大”“后者大”“相等”之一)。
③t1℃时,一小试管内盛有Na2CO3的饱和溶液,试管底部还存有少许Na2CO3固体,将小试管放入盛有水的烧杯中,将较多量的NaOH固体加入烧杯内的水中,观察到小试管内的固体物质逐渐溶解,原因是___________ 。

(1)中国科学院天津工业生物技术研究所在《科学》杂志发表论文,表示其研究团队首次在实验室实现了二氧化碳到淀粉〔(C6H10O5)n〕的人工合成。
①人工合成淀粉过程为:在催化剂的作用下,将二氧化碳和氢气转化为甲醇(CH3OH)和水,再经过铰复杂的变化将甲醇转化为淀粉。请写出该过程中,二氧化碳和氢气反应生成甲醇的化学方程式:
②甲醇常温下是一种无色液体,易溶于水,沸点64.7℃。要将甲醇从其水溶液中分离出来,可以采用
③根据质量守恒定律,用以上方法生产32g甲醇,至少需要CO2的质量为
④绿色植物通过光合作用也可以合成淀粉,该过程是绿色植物将光能转化为
⑤生活中检验淀粉可以选用
(2)1926年我国化学家侯德榜创立了“侯氏制减法”,使原料NaC1的利用率从70%提高到96%,也使原来的副产物CaCl2转化成化肥NH4Cl。Na2CO3和NaCl的溶解度曲线如右图所示,请回答下列问题:

①以NaCl为原料制取纯碱(Na2CO3),从元素守恒的观点来看,还需要补充
②将t2℃时相同质量的Na2CO3饱和溶液和NaC1饱和溶液均降温至t1℃,此时所得两溶液的溶质质量分数相比较为
③t1℃时,一小试管内盛有Na2CO3的饱和溶液,试管底部还存有少许Na2CO3固体,将小试管放入盛有水的烧杯中,将较多量的NaOH固体加入烧杯内的水中,观察到小试管内的固体物质逐渐溶解,原因是

您最近一年使用:0次
名校
4 . 填空
(1)胆矾的化学式为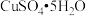 。
。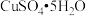 属于
属于___________ 。 (选填“纯净物”或“混合物”); 1mol 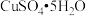 中约含有
中约含有___________ 个S原子
(2)湿法炼铜产生酸性废水,含有的H2SO4、CuSO4、 ZnSO4, 可用铁炭混合物(铁粉和活性炭的混合物)除去。其他条件不变,废水pH对Cu2+、Zn2+去除率的影响如图所示。
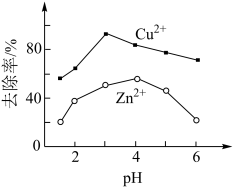
①pH<3时,铁炭混合物表面有大量气泡产生,产生该现象的化学方程式为___________ 。
②相同pH条件下,Cu2+的去除率远高于Zn2+的原因可能是___________ 。
(3)如图是某输液瓶标签上的部分内容。由此可知,葡萄糖由___________ 种元素组成,其中碳元素的质量分数为___________ 。要把 10 g 这种葡萄糖溶液稀释为 2%的溶液,需要加水的质量为___________ g。
(1)胆矾的化学式为
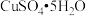 。
。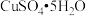 属于
属于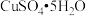 中约含有
中约含有(2)湿法炼铜产生酸性废水,含有的H2SO4、CuSO4、 ZnSO4, 可用铁炭混合物(铁粉和活性炭的混合物)除去。其他条件不变,废水pH对Cu2+、Zn2+去除率的影响如图所示。

①pH<3时,铁炭混合物表面有大量气泡产生,产生该现象的化学方程式为
②相同pH条件下,Cu2+的去除率远高于Zn2+的原因可能是
(3)如图是某输液瓶标签上的部分内容。由此可知,葡萄糖由
| 葡萄糖注射液 (C6H12O6) 【成分】葡萄糖,水 【规格】500mL 质量分数为 5% 【性状】液体,味甜 【贮藏】密闭保存 |
您最近一年使用:0次
5 . 根据如图所示的实验回答问题。

(1)甲是蒸发食盐水的实验。当观察到蒸发皿中出现_______ 时,停止加热。
(2)乙是探究可燃物燃烧条件的实验。实验中热水的作用是_______ ;写出一组对照实验:_______ 。
(3)丙是用稀盐酸、氢氧化钠溶液、酚酞溶液进行酸碱中和反应的实验,试剂Ⅱ是_______ ,试剂Ⅰ的作用是_______ 。

(1)甲是蒸发食盐水的实验。当观察到蒸发皿中出现
(2)乙是探究可燃物燃烧条件的实验。实验中热水的作用是
(3)丙是用稀盐酸、氢氧化钠溶液、酚酞溶液进行酸碱中和反应的实验,试剂Ⅱ是
您最近一年使用:0次
名校
6 . 选择下列实验方法分离提纯物质,将分离提纯方法的字母序号填在横线上。
A.萃取分液 B.升华 C.重结晶 D.分液 E.蒸馏 F.过滤 G.洗气
(1)____ 分离氯化钾与固体碘的混合物。
(2)____ 提纯含有泥沙的苯甲酸固体。
(3)____ 分离水和CCl4的混合物。
(4)____ 分离石油中的各组分。
(5)____ 除去混在甲烷中的乙烯。
(6)____ 提取溴水中的溴。
A.萃取分液 B.升华 C.重结晶 D.分液 E.蒸馏 F.过滤 G.洗气
(1)
(2)
(3)
(4)
(5)
(6)
您最近一年使用:0次
名校
7 . 化学就在我们身边,它与我们的日常生活生产密切相关,按要求回答以下问题
(1)煎中药时用水在煮沸条件下提取中药中的有效成分相当于化学实验中的_______ 操作(填操作名称)
(2)维生素C又称“抗坏血酸”,在人体内有重要功能,具有还原性,能帮助人体将食物中摄取的不易吸收的 转化为
转化为_______ 。
(3)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,常用FeCl3作“腐蚀液”,生成 和
和 ,其反应的离子方程式为
,其反应的离子方程式为_______ 。
(4)洪水过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂,工业上将氯气通入石灰乳中制取漂白粉,其化学方程式为_______ ;漂白粉敞放在空气中会变质,其发生的化学方程式为_______ 。
(5)某同学需帮助水质检测站配制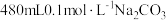 溶液以备使用。
溶液以备使用。
①该同学选择托盘天平、药匙、量筒、烧杯、玻璃棒、胶头滴管、_______ 。
②该同学应称取 固体
固体_______ g
③在转移完溶液后未洗涤玻璃棒和烧杯,会使浓度_______ (填“偏大”、“偏小”或“不变”)。
(1)煎中药时用水在煮沸条件下提取中药中的有效成分相当于化学实验中的
(2)维生素C又称“抗坏血酸”,在人体内有重要功能,具有还原性,能帮助人体将食物中摄取的不易吸收的
 转化为
转化为(3)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,常用FeCl3作“腐蚀液”,生成
 和
和 ,其反应的离子方程式为
,其反应的离子方程式为(4)洪水过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂,工业上将氯气通入石灰乳中制取漂白粉,其化学方程式为
(5)某同学需帮助水质检测站配制
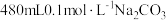 溶液以备使用。
溶液以备使用。①该同学选择托盘天平、药匙、量筒、烧杯、玻璃棒、胶头滴管、
②该同学应称取
 固体
固体③在转移完溶液后未洗涤玻璃棒和烧杯,会使浓度
您最近一年使用:0次
8 . 用于分离或提纯物质的方法有:A.蒸馏(分馏) B.萃取C.过滤 D.重结晶 E.分液。下列各组混合物的分离或提纯应选用上述哪一种方法最合适?(填方法的标号 )
(1)除去Ca(OH)2溶液中悬浮的CaCO3微粒___ ;
(2)分离四氯化碳与水的混合物____ ;
(3)分离汽油和煤油____ ;
(4)分离碘水中的碘单质____ ;
(5)提纯氯化钠和硝酸钾混合物中的硝酸钾____ 。
(1)除去Ca(OH)2溶液中悬浮的CaCO3微粒
(2)分离四氯化碳与水的混合物
(3)分离汽油和煤油
(4)分离碘水中的碘单质
(5)提纯氯化钠和硝酸钾混合物中的硝酸钾
您最近一年使用:0次
2021-03-25更新
|
78次组卷
|
2卷引用:新疆维吾尔自治区呼图壁县第一中学2020-2021学年高二下学期期初考试化学试题
名校
解题方法
9 . 某铝合金中含有元素铝、镁、铜、硅,为了测定该合金中铝的含量,设计了如下实验,请回答有关问题:
(1)称取样品ag(精确到0.1g),称量时通常使用的主要仪器的名称是_______ 。
(2)样品溶解于足量的稀盐酸,过滤并洗涤滤渣。滤渣为_______ ,溶解、过滤用到的玻璃仪器是_______ 。
(3)向滤液中加过量的氢氧化钠溶液,过滤并洗涤滤渣。有关的离子方程式是_______ 、_______ 、_______ 。
(4)向步骤(3)的滤液中通入足量的二氧化碳气体,过滤并洗涤滤渣。有关的离子方程式是_______ 、_______ 。
(5)将步骤(4)中所得的滤渣烘干并灼烧至恒重、冷却后称量,其质量为bg。有关反应的化学方程式是_______ 。原样品中铝的质量分数是_______ 。
(1)称取样品ag(精确到0.1g),称量时通常使用的主要仪器的名称是
(2)样品溶解于足量的稀盐酸,过滤并洗涤滤渣。滤渣为
(3)向滤液中加过量的氢氧化钠溶液,过滤并洗涤滤渣。有关的离子方程式是
(4)向步骤(3)的滤液中通入足量的二氧化碳气体,过滤并洗涤滤渣。有关的离子方程式是
(5)将步骤(4)中所得的滤渣烘干并灼烧至恒重、冷却后称量,其质量为bg。有关反应的化学方程式是
您最近一年使用:0次
名校
10 . (1)当光束通过下列物质时,会出现丁达尔效应的是_______ 。
①Fe(OH)3胶体,②水,③蔗糖溶液,④Ca(OH)2悬浊液
(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有_______ (填“氧化性”或“还原性”)。
(3)下列各组混合物的分离或提纯选用哪种方法最合适?(把选用的标号填入括号内)
A.萃取 B.分液 C.过滤 D.加热分解 E.蒸发 F.蒸馏 H.升华
①把溴水中的溴提取出来_______
②分离柴油和水的混合物_______
③分离四氯化碳(沸点为 76.75℃)和甲苯(沸点为 110.6℃)的混合物_______
(4)现有以下物质:①Ba(OH)2晶体,②盐酸,③冰醋酸(固态醋酸),④石墨,⑤酒精(C2H5OH),请回答下列问题(填序号):
Ⅰ、以上物质中属于电解质的是_______ 。
Ⅱ、以上物质中属于非电解质的是_______ 。
Ⅲ、请写出①在水溶液中的电离方程式_______ 。
(5)某学校实验室有一瓶浓硫酸试剂,标签上标有密度1.84g·cm-3,质量分数98%,现用该浓硫酸配制480 mL 1mol·L﹣1的稀硫酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒。请回答下列问题:
a.配制稀硫酸时,除了上述仪器,还缺少的仪器有_______ (写仪器名称)。
b.经计算,配制480mL 1mol·L-1的稀硫酸,需要用量筒量取上述浓硫酸的体积为_______ mL。
①Fe(OH)3胶体,②水,③蔗糖溶液,④Ca(OH)2悬浊液
(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
(3)下列各组混合物的分离或提纯选用哪种方法最合适?(把选用的标号填入括号内)
A.萃取 B.分液 C.过滤 D.加热分解 E.蒸发 F.蒸馏 H.升华
①把溴水中的溴提取出来
②分离柴油和水的混合物
③分离四氯化碳(沸点为 76.75℃)和甲苯(沸点为 110.6℃)的混合物
(4)现有以下物质:①Ba(OH)2晶体,②盐酸,③冰醋酸(固态醋酸),④石墨,⑤酒精(C2H5OH),请回答下列问题(填序号):
Ⅰ、以上物质中属于电解质的是
Ⅱ、以上物质中属于非电解质的是
Ⅲ、请写出①在水溶液中的电离方程式
(5)某学校实验室有一瓶浓硫酸试剂,标签上标有密度1.84g·cm-3,质量分数98%,现用该浓硫酸配制480 mL 1mol·L﹣1的稀硫酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒。请回答下列问题:
a.配制稀硫酸时,除了上述仪器,还缺少的仪器有
b.经计算,配制480mL 1mol·L-1的稀硫酸,需要用量筒量取上述浓硫酸的体积为
您最近一年使用:0次



