解题方法
1 . 某实验小组用0.50 NaOH溶液和0.50
NaOH溶液和0.50 硫酸溶液进行中和热的测定。
硫酸溶液进行中和热的测定。
(一)配制0.50 NaOH溶液。
NaOH溶液。
(1)若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体_______ g。
(2)从下图中选择称量NaOH固体所需要的仪器_______ (填字母)。
(二)测定稀硫酸和稀氢氧化钠反应的中和热的实验装置如图所示。
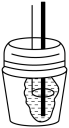
(3)写出该反应的热化学方程式(中和热 ):
):_______ 。
(4)取50mLNaOH溶液和30mL硫酸溶液进行实验,实验数据如下表。
①请填写表中的空白:
②近似认为0.50 NaOH溶液和0.50
NaOH溶液和0.50 硫酸溶液的密度都是1
硫酸溶液的密度都是1 ,中和后生成溶液的比热容
,中和后生成溶液的比热容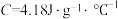 。则测得中和热
。则测得中和热 =
=_______  (取小数点后一位)。
(取小数点后一位)。
③上述实验数值结果与57.3 有偏差,产生偏差的原因可能是
有偏差,产生偏差的原因可能是_______ (填字母)。
A.实验装置保温、隔热效果差
B.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
C.用温度计测定NaOH溶液起始温度后直接测定 溶液的温度
溶液的温度
 NaOH溶液和0.50
NaOH溶液和0.50 硫酸溶液进行中和热的测定。
硫酸溶液进行中和热的测定。(一)配制0.50
 NaOH溶液。
NaOH溶液。(1)若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体
(2)从下图中选择称量NaOH固体所需要的仪器
| 序号 | a | b | c | d | e | f |
| 仪器 | 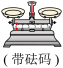 |  |  |  |  |  |
(二)测定稀硫酸和稀氢氧化钠反应的中和热的实验装置如图所示。

(3)写出该反应的热化学方程式(中和热
 ):
):(4)取50mLNaOH溶液和30mL硫酸溶液进行实验,实验数据如下表。
①请填写表中的空白:
| 实验次数 | 起始温度 /℃ /℃ | 终止温度 /℃ /℃ | 温度差平均值 (  - - )/℃ )/℃ | ||
 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
 NaOH溶液和0.50
NaOH溶液和0.50 硫酸溶液的密度都是1
硫酸溶液的密度都是1 ,中和后生成溶液的比热容
,中和后生成溶液的比热容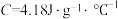 。则测得中和热
。则测得中和热 =
= (取小数点后一位)。
(取小数点后一位)。③上述实验数值结果与57.3
 有偏差,产生偏差的原因可能是
有偏差,产生偏差的原因可能是A.实验装置保温、隔热效果差
B.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
C.用温度计测定NaOH溶液起始温度后直接测定
 溶液的温度
溶液的温度
您最近一年使用:0次
2022-12-31更新
|
211次组卷
|
3卷引用:河南省鹤壁市第一中学2022-2023学年高二上学期期末检测化学试题
2 . 某同学用硫铁矿焙烧后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取绿矾FeSO4·7H2O,设计了如下流程(部分物质已略去,加入的试剂均过量):回答下列问题:
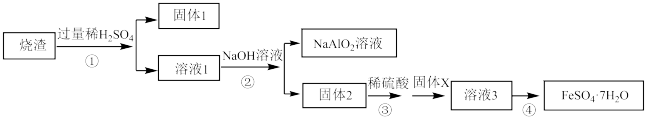
(1)固体1的主要成分为___________ (填化学式,下同),固体X为_____________ 。
(2)写出步骤②中生成固体2和NaAlO2溶液的离子方程式为_____________ 、__________
(3)某学生的过滤操作中,其操作不规范的是__________ (填标号)。
a.玻璃棒用作引流
b.滤纸边缘高出漏斗
c.漏斗末端颈尖未紧靠烧杯壁
d.将滤纸湿润,使其紧贴漏斗壁
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(4)步骤①中用到的稀硫酸浓度为2mol/L,体积为1L,此稀硫酸是由18.0 mol/L的浓硫酸稀释得到,该用量筒量取__________ ml 18.0 mol/L的浓硫酸。下列操作使所配稀硫酸浓度偏大的有________ (填写字母)。
A、在烧杯中稀释浓硫酸后,未冷却就立即转移到容量瓶中
B、往容量瓶转移时,有少量液体溅出;
C、定容时俯视刻度线;
D、容量瓶未干燥即用来配制溶液;
E、定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。

(1)固体1的主要成分为
(2)写出步骤②中生成固体2和NaAlO2溶液的离子方程式为
(3)某学生的过滤操作中,其操作不规范的是
a.玻璃棒用作引流
b.滤纸边缘高出漏斗
c.漏斗末端颈尖未紧靠烧杯壁
d.将滤纸湿润,使其紧贴漏斗壁
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(4)步骤①中用到的稀硫酸浓度为2mol/L,体积为1L,此稀硫酸是由18.0 mol/L的浓硫酸稀释得到,该用量筒量取
A、在烧杯中稀释浓硫酸后,未冷却就立即转移到容量瓶中
B、往容量瓶转移时,有少量液体溅出;
C、定容时俯视刻度线;
D、容量瓶未干燥即用来配制溶液;
E、定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。
您最近一年使用:0次
解题方法
3 . 实验室配制500mL 0.1 mol/L Na2CO3溶液,实验操作步骤如下:
①用电子天平称出相应质量的Na2CO3固体。把它放入烧杯中,加入适量的蒸馏水,使它完全溶解。
②把制得的溶液,小心地注入___________中。
③继续向容量瓶中加蒸馏水至液面距离刻度1-2cm处,改用________小心滴加蒸馏水至液面凹液面最低处与刻度线相切。
④用少量蒸馏水洗涤玻璃棒和烧杯2-3次,每次洗涤的液体都要小心的转入容量瓶中。
⑤将瓶塞塞紧,充分摇匀。
(1)请填写②和③处仪器名称___________ 、___________ 。
(2)需要称取碳酸钠固体______________ 。
(3)操作步骤正确的顺序为______________ (填写序号)。
(4)溶液注入容量瓶先需恢复到室温,这是因为______________ 。
(5)下列操作对配置溶液的浓度大小有何影响?
I.若没有进行步骤④,则所配溶液的浓度将会______________ 。
A.偏大 B.偏小 C.无影响
Ⅱ.俯视刻度线,则所配制的溶液浓度将会______________ 。
A.偏大 B.偏小 C.无影响
(6)定容时,取上述溶液100mL稀释至1000mL,所得溶液中钠离子的物质的量浓度为_____________ 。
(7)若实验过程中,加入蒸馏水时,不慎超过了刻度线,应如何处理?____________ 。
①用电子天平称出相应质量的Na2CO3固体。把它放入烧杯中,加入适量的蒸馏水,使它完全溶解。
②把制得的溶液,小心地注入___________中。
③继续向容量瓶中加蒸馏水至液面距离刻度1-2cm处,改用________小心滴加蒸馏水至液面凹液面最低处与刻度线相切。
④用少量蒸馏水洗涤玻璃棒和烧杯2-3次,每次洗涤的液体都要小心的转入容量瓶中。
⑤将瓶塞塞紧,充分摇匀。
(1)请填写②和③处仪器名称
(2)需要称取碳酸钠固体
(3)操作步骤正确的顺序为
(4)溶液注入容量瓶先需恢复到室温,这是因为
(5)下列操作对配置溶液的浓度大小有何影响?
I.若没有进行步骤④,则所配溶液的浓度将会
A.偏大 B.偏小 C.无影响
Ⅱ.俯视刻度线,则所配制的溶液浓度将会
A.偏大 B.偏小 C.无影响
(6)定容时,取上述溶液100mL稀释至1000mL,所得溶液中钠离子的物质的量浓度为
(7)若实验过程中,加入蒸馏水时,不慎超过了刻度线,应如何处理?
您最近一年使用:0次
名校
解题方法
4 . 掌握仪器的名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置。
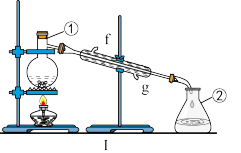
(1)写出仪器的名称:①_______ 。
(2)若利用装置Ⅰ分离四氯化碳和酒精的混合物,还缺少的仪器有_______ 。
(3)某校环保兴趣小组在处理污水样品时,需用质量分数为37%、密度为1.19 g/cm3的浓盐酸配制成250 mL 0.1 mol/L的稀盐酸。装置Ⅱ是某同学转移溶液的示意图,图Ⅱ中的错误是_______ 。
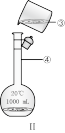
①盛放浓盐酸的试剂瓶标签上应印有图中警示标识中的_______ 。(填序号)。
A. B.
B.  C.
C. D.
D.
②在如图所示仪器中,配制上述溶液不需要的是_______ (填图中相应仪器的序号)。
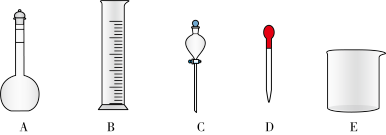
③根据计算,本实验需要量取浓盐酸的体积为_______ mL,本实验应使用的量筒_______ (填序号)。
A.10ml B.100ml C.250ml D.500ml
④在容量瓶的使用方法中,下列操作正确的是_____ (填序号)。
A.使用容量瓶前检查是否漏水
B.容量瓶用水洗净后,再用配好的稀HCl溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线
D.配制溶液时,若试样是液体,用量筒取试样后直接倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住容量瓶底部,反复倒转多次,摇匀
⑤假设配制时其他操作均正确,只出现以下某一情况,试判断对所配制的溶液浓度的影响(相比于要求的值,即0.1 mol/L,填“偏高”“偏低”或“无影响”)。
A.容量瓶中有少量蒸馏水:_______ ;
B.稀释浓盐酸时,没有冷却就立即转移到容量瓶中:_______ ;
C.配制的溶液装入洁净的但有少量蒸馏水的试剂瓶中:_______ ;
D.定容时俯视:_______ 。

(1)写出仪器的名称:①
(2)若利用装置Ⅰ分离四氯化碳和酒精的混合物,还缺少的仪器有
(3)某校环保兴趣小组在处理污水样品时,需用质量分数为37%、密度为1.19 g/cm3的浓盐酸配制成250 mL 0.1 mol/L的稀盐酸。装置Ⅱ是某同学转移溶液的示意图,图Ⅱ中的错误是

①盛放浓盐酸的试剂瓶标签上应印有图中警示标识中的
A.
 B.
B.  C.
C. D.
D.
②在如图所示仪器中,配制上述溶液不需要的是

③根据计算,本实验需要量取浓盐酸的体积为
A.10ml B.100ml C.250ml D.500ml
④在容量瓶的使用方法中,下列操作正确的是
A.使用容量瓶前检查是否漏水
B.容量瓶用水洗净后,再用配好的稀HCl溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线
D.配制溶液时,若试样是液体,用量筒取试样后直接倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住容量瓶底部,反复倒转多次,摇匀
⑤假设配制时其他操作均正确,只出现以下某一情况,试判断对所配制的溶液浓度的影响(相比于要求的值,即0.1 mol/L,填“偏高”“偏低”或“无影响”)。
A.容量瓶中有少量蒸馏水:
B.稀释浓盐酸时,没有冷却就立即转移到容量瓶中:
C.配制的溶液装入洁净的但有少量蒸馏水的试剂瓶中:
D.定容时俯视:
您最近一年使用:0次
2022-07-20更新
|
106次组卷
|
2卷引用:内蒙古包头市第四中学2021-2022学年高一上学期期中考试化学试题
解题方法
5 . 将 19.5 g锌粒投入250 mL 2mol/L的硫酸溶液中,试计算:(写出计算过程)
(1)产生的氢气在标准状况下的体积;
(2)忽略溶液体积变化体积,反应后溶液中氢离子浓度是多少?
(3)要配制250 mL 2mol/L的硫酸溶液,需用质量百分数为98%,密度为1.84 g/cm3浓硫酸多少毫升?(保留三位有效数字)
(1)产生的氢气在标准状况下的体积;
(2)忽略溶液体积变化体积,反应后溶液中氢离子浓度是多少?
(3)要配制250 mL 2mol/L的硫酸溶液,需用质量百分数为98%,密度为1.84 g/cm3浓硫酸多少毫升?(保留三位有效数字)
您最近一年使用:0次
6 . (一)(1)用胆矾(CuSO4·5H2O)配制0.200mol/L CuSO4溶液240mL,所需要的玻璃仪器为:烧杯、量筒、________________________ (要填全),应称取胆矾的质量为____________ 。
(2)下列操作使所配CuSO4溶液浓度偏低的是____________ 。
A.观察刻度线时仰视
B.观察刻度线时俯视
C.定容后倒转容量瓶几次,发现液面最低点低于标线,再补几滴水至标线
D.配制溶液前,容量瓶中有少量蒸馏水
(二)(1)用单线桥标出该反应的电子转移方向和数目,并回答相关问题:
KClO4+8HCl(浓)=KCl+4Cl2↑+4H2O____________ ,氧化剂与还原剂的物质的量之比为____________ 。
(2)配平化学方程式(将化学计量数填于空白处)
_____ KMnO4+___FeSO4+___H2SO4=___K2SO4+__MnSO4+__Fe2(SO4)3+__H2O
氧化产物与还原产物的物质的量比为________ 。
(2)下列操作使所配CuSO4溶液浓度偏低的是
A.观察刻度线时仰视
B.观察刻度线时俯视
C.定容后倒转容量瓶几次,发现液面最低点低于标线,再补几滴水至标线
D.配制溶液前,容量瓶中有少量蒸馏水
(二)(1)用单线桥标出该反应的电子转移方向和数目,并回答相关问题:
KClO4+8HCl(浓)=KCl+4Cl2↑+4H2O
(2)配平化学方程式(将化学计量数填于空白处)
氧化产物与还原产物的物质的量比为
您最近一年使用:0次
名校
解题方法
7 . (1)某同学欲配制100 mL 0.10 mol·L-1的CuSO4溶液。以下操作1~5是其配制的过程及示意图:
操作1:准确称取一定质量的胆矾晶体并用适量蒸馏水溶解。
操作2:将所得溶液转移到仪器X中,用蒸馏水冲洗烧杯和玻璃棒2~3次,将洗涤液也转移到X中。
操作3:继续向X中加蒸馏水至液面离X的刻度线1~2 cm处。
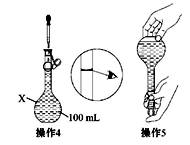
①仪器X的名称是________ 。称量过程中主要用到的仪器是_____________ 。在将烧杯中的溶液转移至容量瓶中,为了防止溶液溅出,应采取什么措施____________________ 。
②关于该配制过程,下列说法正确的是________ 。
A.操作1中,应称取胆矾晶体的质量为2.5 g
B.操作2中,洗涤液不需要转移到仪器X中
C.操作4称为定容,由于该同学的观察方法不正确,将导致所配溶液浓度偏低
D.操作5摇匀后静置,发现液面低于刻度线,应继续加水至凹液面与刻度线相切
(2)为实现金属钠在隔绝空气条件下与水反应并收集生成的气体,某研究性学习小组设计了如图发生装置。
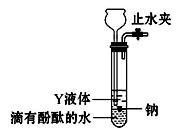
① Y液体可以选用________ 。
A.煤油 B.饱和的食盐水 C.四氯化碳
②实验前检验该装置气密性的方法是____________ 。
操作1:准确称取一定质量的胆矾晶体并用适量蒸馏水溶解。
操作2:将所得溶液转移到仪器X中,用蒸馏水冲洗烧杯和玻璃棒2~3次,将洗涤液也转移到X中。
操作3:继续向X中加蒸馏水至液面离X的刻度线1~2 cm处。

①仪器X的名称是
②关于该配制过程,下列说法正确的是
A.操作1中,应称取胆矾晶体的质量为2.5 g
B.操作2中,洗涤液不需要转移到仪器X中
C.操作4称为定容,由于该同学的观察方法不正确,将导致所配溶液浓度偏低
D.操作5摇匀后静置,发现液面低于刻度线,应继续加水至凹液面与刻度线相切
(2)为实现金属钠在隔绝空气条件下与水反应并收集生成的气体,某研究性学习小组设计了如图发生装置。

① Y液体可以选用
A.煤油 B.饱和的食盐水 C.四氯化碳
②实验前检验该装置气密性的方法是
您最近一年使用:0次



