名校
1 . 下列实验有关操作不正确 的是
| 被提纯物(杂质) | 除杂方法 | |
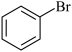
| A | 苯甲酸( ) ) | 加热溶解,冷却结晶,过滤、洗涤、干燥 |
| B |  | 加入生石灰,蒸馏 |
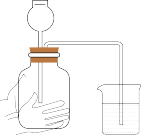
| C | 乙炔( ) ) | 酸性高锰酸钾溶液,洗气 |
| D | 乙酸乙酯(乙酸) | 加入饱和碳酸钠溶液,分液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 实验室提纯以下物质(括号内为杂质),所选用的除杂试剂和分离方法都正确的是
| 被提纯的物质 | 除杂试剂 | 分离方法 | |
| A | 乙炔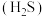 | 酸性高锰酸钾溶液 | 洗气 |
| B | 苯(己烯) | 溴水 | 洗涤,分液 |
| C | 丙烷(丙烯) | 酸性高锰酸钾溶液 | 洗气 |
| D |
|  溶液 溶液 | 分液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 下列实验装置、目的均正确的是
选项 | 实验装置 | 实验目的 |
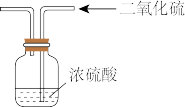
A |
| 干燥 |
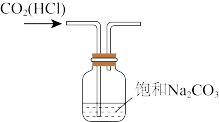
B |
| 除去 |
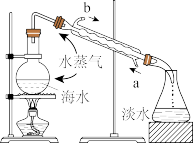
C |
| 蒸馏海水获取蒸馏水 |
D |
| 检验装置的气密性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 下列实验过程可以达到实验目的的是
| 实验目的 | 实验过程 | |
| A | 配制氯化铁溶液 | 将氯化铁溶解在较浓的盐酸中再加水稀释 |
| B | 证明酸性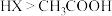 | 用 计测定 计测定 溶液、 溶液、 溶液的 溶液的 , , 前者小 前者小 |
| C | 除去 中的 中的 | 将混合气体通过饱和食盐水 |
| D | 探究浓度对反应速率的影响 | 向2支盛有5 不同浓度 不同浓度 溶液的试管中同时加入2 溶液的试管中同时加入2 5% 5% 溶液,观察实验现象 溶液,观察实验现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-11-12更新
|
171次组卷
|
2卷引用:重庆市三峡名校联盟2022-2023学年高二上学期秋季联考化学试题
5 . 电子工业常用FeCl3溶液腐蚀印刷电路板上不需要的铜箔,最后得到含FeCl3、FeCl2杂质的CuCl2溶液。某化学兴趣小组设计下列方案,从该废液中 除去FeCl3、FeCl2杂质,制取纯净的CuCl2。
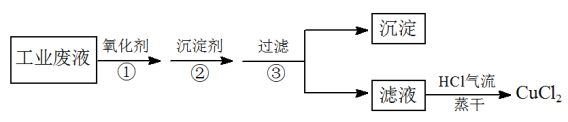
请回答下列问题:
(1)在①步操作中使用了氧化剂,下列氧化剂中一定不能使用的是_______ 。
A.Cl2 B.NaClO C.H2O2 D.KMnO4 E.O3
(2)②步操作中的“沉淀剂”可以是下列中的_______ 。
A.NaOH B.NH3·H2O C.CuO D.Cu2(OH)2CO3 E.Fe2O3
用一种你选择的沉淀剂,分步写出除去杂质的离子方程式:_______ 。
(3)最后将滤液在HCl气流中蒸干,其目的是_______ ,如果将滤液直接加热蒸干,最后得到的固体可能是_______ 。
(4)设常温下各沉淀的溶度积近似为:Ksp[Cu(OH)2]=10-20、Ksp[Fe(OH)3]=10-38、Ksp[Fe(OH)2]=10-16;通常,人们把浓度小于10-5mol/L的离子视为“不存在”。根据所给条件,完成下列问题:
①如果该废液中CuCl2的浓度为1 mol/L,在加沉淀剂时应调节溶液的pH值范围为:_______ 。
②如果对废液不先用氧化剂,而是直接加入沉淀剂,带来的后果是:_______ 。

请回答下列问题:
(1)在①步操作中使用了氧化剂,下列氧化剂中一定不能使用的是
A.Cl2 B.NaClO C.H2O2 D.KMnO4 E.O3
(2)②步操作中的“沉淀剂”可以是下列中的
A.NaOH B.NH3·H2O C.CuO D.Cu2(OH)2CO3 E.Fe2O3
用一种你选择的沉淀剂,分步写出除去杂质的离子方程式:
(3)最后将滤液在HCl气流中蒸干,其目的是
(4)设常温下各沉淀的溶度积近似为:Ksp[Cu(OH)2]=10-20、Ksp[Fe(OH)3]=10-38、Ksp[Fe(OH)2]=10-16;通常,人们把浓度小于10-5mol/L的离子视为“不存在”。根据所给条件,完成下列问题:
①如果该废液中CuCl2的浓度为1 mol/L,在加沉淀剂时应调节溶液的pH值范围为:
②如果对废液不先用氧化剂,而是直接加入沉淀剂,带来的后果是:
您最近一年使用:0次
6 . 用括号内的试剂和方法除去下列各物质中的少量杂质,正确的是
| A.乙烯中混有乙烷(溴水、洗气) | B.乙酸乙酯中混有乙酸(NaOH溶液、蒸馏) |
| C.硬脂酸钠中混有甘油(水、过滤) | D.溴苯中含有液溴(NaOH溶液、分液) |
您最近一年使用:0次
7 . 下列除去杂质的实验方法正确的是
A.除去溴乙烷中的少量 ,加入过量氢氧化钠溶液,加热充分反应,分液 ,加入过量氢氧化钠溶液,加热充分反应,分液 |
| B.除去乙醛中少量的乙醇:加入过量酸性高锰酸钾溶液,充分反应后,蒸馏 |
| C.除去苯中少量的苯酚:加入过量氢氧化钠溶液、充分反应,分液 |
| D.除去乙烷中少量的乙烯;将气体通入过量酸性高锰酸钾溶液洗气 |
您最近一年使用:0次
8 . 下列由实验得出的结论正确的是
| 实验 | 结论 | |
| A | 甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红 | 生成的有机物具有酸性 |
| B | 将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明 | 生成的 1,2-二溴乙烷无色、可溶于四氯化碳 |
| C | 乙烷中混有杂质乙烯,可将混合气体通入溴水溶液中,除去杂质乙烯 | 乙烯被溴水氧化 |
| D | 乙醇和水都可与金属钠反应产生可燃性气体 | 乙醇分子中的氢与水分子中的氢具有相同的活性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 提纯下列物质(括号内为少量杂质),能达到目的的是
| 选项 | 混合物 | 除杂试剂 | 分离方法 |
| A | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| B | 苯(苯酚) | 浓溴水 | 过滤 |
| C | 溴苯(溴) | Na2SO3溶液 | 分液 |
| D | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-31更新
|
602次组卷
|
5卷引用:重庆市主城区六校2020-2021学年高二下学期期末联考化学试题
名校
10 . 已知硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O,其摩尔质量为392g·mol-1]可用作净水剂、颜料、媒染剂、鞣革、防腐剂等,它在空气中不及硫酸亚铁容易被氧化,易溶于水,不溶于乙醇。回答下列问题:
I.制备过程
步骤1:制备硫酸亚铁溶液:将5.6g铁粉和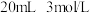 硫酸置于锥形瓶中,水浴加热至几乎不产生气泡,趁热过滤掉残余的少量铁粉。
硫酸置于锥形瓶中,水浴加热至几乎不产生气泡,趁热过滤掉残余的少量铁粉。
步骤2:获得硫酸亚铁铵晶体:向滤液中加入一定量的硫酸铵溶液,然后蒸发浓缩、冷却结晶、过滤、洗涤、晾干。
(1)步骤1中,加入过量铁粉的目的是___________ ;由于加入的铁粉不纯,反应过程中会产生少量H2S,可以用CuSO4溶液进行吸收处理,发生的反应化学方程式为:___________ 。
(2)步骤2中,所用到的硫酸铵溶液呈酸性,原因是___________ (用离子方程式表示),过滤后的硫酸亚铁铵晶体最好用___________ 洗涤;
II.定量分析——氧化还原滴定法
称取20.00g制得的硫酸亚铁铵晶体溶于稀硫酸,加水配制成100mL溶液,取25.00mL于锥形瓶中,然后用 的酸性高锰酸钾溶液进行滴定。
的酸性高锰酸钾溶液进行滴定。
(3)滴定过程中高锰酸钾溶液应装在___________ 仪器中(填“A”或“B”);
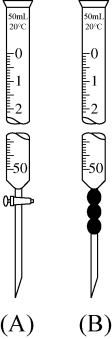
(4)滴定终点的现象是___________ ;
(5)若进行平行滴定三次,消耗 溶液的体积如下表所示:
溶液的体积如下表所示:
则制得的硫酸亚铁铵晶体纯度(质量分数)为___________ (用百分数表示,保留小数点后两位);
(6)上表中第一次的数据明显大于后两次的数据,其原因可能是___________;
I.制备过程
步骤1:制备硫酸亚铁溶液:将5.6g铁粉和
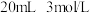 硫酸置于锥形瓶中,水浴加热至几乎不产生气泡,趁热过滤掉残余的少量铁粉。
硫酸置于锥形瓶中,水浴加热至几乎不产生气泡,趁热过滤掉残余的少量铁粉。步骤2:获得硫酸亚铁铵晶体:向滤液中加入一定量的硫酸铵溶液,然后蒸发浓缩、冷却结晶、过滤、洗涤、晾干。
(1)步骤1中,加入过量铁粉的目的是
(2)步骤2中,所用到的硫酸铵溶液呈酸性,原因是
II.定量分析——氧化还原滴定法
称取20.00g制得的硫酸亚铁铵晶体溶于稀硫酸,加水配制成100mL溶液,取25.00mL于锥形瓶中,然后用
 的酸性高锰酸钾溶液进行滴定。
的酸性高锰酸钾溶液进行滴定。(3)滴定过程中高锰酸钾溶液应装在

(4)滴定终点的现象是
(5)若进行平行滴定三次,消耗
 溶液的体积如下表所示:
溶液的体积如下表所示:| 实验次数 | 第一次 | 第二次 | 第三次 |
消耗 溶液的体积/ 溶液的体积/ | 24.54 | 24.01 | 23.99 |
(6)上表中第一次的数据明显大于后两次的数据,其原因可能是___________;
| A.第一次滴定用的锥形瓶用待测液润洗过 |
| B.第一次滴定过程中高锰酸钾溶液滴出锥形瓶外 |
| C.第一次滴定前滴定管尖嘴无气泡,滴定后有气泡 |
| D.第一次滴定结束时,俯视读取酸性高锰酸钾溶液的体积 |
您最近一年使用:0次
2022-03-25更新
|
110次组卷
|
2卷引用:重庆市主城区六校2021-2022学年高二上学期期末联考化学试题