名校
1 . Ⅰ.铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
(1)所含铁元素既有氧化性又有还原性的物质是____ (填字母)。
(2)取一定量氯化亚铁固体,配制成0.1mol·L-1的溶液。检验亚铁离子是否被氧化的方法:____ 。
Ⅱ.工业上用赤铁矿(含Fe2O3、FeO,也含有Al2O3、MnO2、CuO等)制备绿矾FeSO4·7H2O的流程如图:

(3)氢氧化钠溶液加入赤铁矿中发生反应的离子方程式为____ 。
(4)向滤渣Ⅰ中加入过量的试剂a为___ ,过量的试剂b投入到滤液Ⅱ发生的所有反应的离子方程式为____ 。
(5)实验室中操作①②③的名称为____ 。
(6)操作④隔绝空气的目的是____ 。
(1)所含铁元素既有氧化性又有还原性的物质是
| A.Fe | B.FeCl3 | C.FeSO4 | D.Fe2O3 |
Ⅱ.工业上用赤铁矿(含Fe2O3、FeO,也含有Al2O3、MnO2、CuO等)制备绿矾FeSO4·7H2O的流程如图:

(3)氢氧化钠溶液加入赤铁矿中发生反应的离子方程式为
(4)向滤渣Ⅰ中加入过量的试剂a为
(5)实验室中操作①②③的名称为
(6)操作④隔绝空气的目的是
您最近一年使用:0次
名校
解题方法
2 . 某硫酸厂以硫铁矿焙烧后的烧渣(主要成分为Fe2O3、SiO2、Al2O3)为原料制取铵明矾晶体[NH4A1(SO4)2·12H2O]的一种工艺流程如图。

已知:①SiO2是酸性氧化物,难溶于水,酸浸时不发生反应。
②AI(OH)3固体可溶于NaOH等强碱溶液。
请回答下列问题:
(1)写出Fe2O3的一种常见用途:_______ 。
(2)“试剂I”为_______ (填试剂名称),“滤渣b”为_______ (填化学式)。
(3)写出“滤液a”和NaOH溶液反应的离子方程式:_______ 、_______ 。
(4)“滤渣c”的化学式为_______ ,证明铁元素已沉淀完全的实验方法是_______ 。
(5)向NaAlO2溶液中通入足量CO2的离子方程式为_______ 。
(6)从铵明矾溶液中获得铵明矾晶体的实验操作依次为蒸发浓缩、冷却结晶、_______ (填操作名称)、洗涤、干燥。

已知:①SiO2是酸性氧化物,难溶于水,酸浸时不发生反应。
②AI(OH)3固体可溶于NaOH等强碱溶液。
请回答下列问题:
(1)写出Fe2O3的一种常见用途:
(2)“试剂I”为
(3)写出“滤液a”和NaOH溶液反应的离子方程式:
(4)“滤渣c”的化学式为
(5)向NaAlO2溶液中通入足量CO2的离子方程式为
(6)从铵明矾溶液中获得铵明矾晶体的实验操作依次为蒸发浓缩、冷却结晶、
您最近一年使用:0次
名校
解题方法
3 . 某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量 和
和 ,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、胆矾晶体(
,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、胆矾晶体( )和水处理剂高铁酸钾(
)和水处理剂高铁酸钾( )。
)。
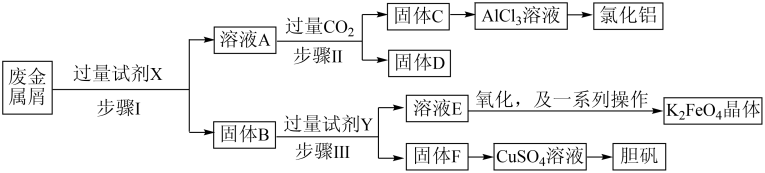
请回答:
(1)利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧胆矾产品时,铜的焰色为___________(填标号)。
(2)试剂X是___________ ;试剂Y是___________ 。步骤Ⅰ涉及到的分离操作是___________ 。
(3)写出溶液A转化为固体C的离子方程式___________ 。
(4)在步骤Ⅱ时,若用大理石与浓盐酸制取 并直接通入溶液A中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是
并直接通入溶液A中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是___________ 。
(5)溶液E在空气中易被氧化,请设计一个简单的实验方案检验溶液E是否被氧化___________ 。由溶液E制取 时,不同的温度下,不同质量浓度的
时,不同的温度下,不同质量浓度的 对
对 生成率有以下影响,由图可知工业生产中最佳条件(温度和
生成率有以下影响,由图可知工业生产中最佳条件(温度和 的质量浓度)为
的质量浓度)为___________ 。

(6)在固体F中加入稀硫酸和 来制备
来制备 溶液是一种环保工艺,该反应的总的化学方程式为
溶液是一种环保工艺,该反应的总的化学方程式为___________ 。
 和
和 ,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、胆矾晶体(
,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、胆矾晶体( )和水处理剂高铁酸钾(
)和水处理剂高铁酸钾( )。
)。
请回答:
(1)利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧胆矾产品时,铜的焰色为___________(填标号)。
| A.黄色 | B.红色 | C.紫色 | D.绿色 |
(3)写出溶液A转化为固体C的离子方程式
(4)在步骤Ⅱ时,若用大理石与浓盐酸制取
 并直接通入溶液A中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是
并直接通入溶液A中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是(5)溶液E在空气中易被氧化,请设计一个简单的实验方案检验溶液E是否被氧化
 时,不同的温度下,不同质量浓度的
时,不同的温度下,不同质量浓度的 对
对 生成率有以下影响,由图可知工业生产中最佳条件(温度和
生成率有以下影响,由图可知工业生产中最佳条件(温度和 的质量浓度)为
的质量浓度)为
(6)在固体F中加入稀硫酸和
 来制备
来制备 溶液是一种环保工艺,该反应的总的化学方程式为
溶液是一种环保工艺,该反应的总的化学方程式为
您最近一年使用:0次
名校
4 . 下列操作不能 达到目的的是
| 实验目的 | 相关操作 | |
| A | 除去KCl固体中少量的MgCl2 | 将固体溶解,向所得溶液中加入过量NaOH溶液,过滤,将滤液蒸发结晶 |
| B | 除去Fe2(SO4)3溶液中混有少量FeSO4 | 向溶液中加入足量双氧水 |
| C | 除去I2中的NaCl | 将混合物加热,收集蒸汽并冷凝 |
| D | 除去MgO中混有的Al2O3 | 向混合物中加足量NaOH溶液,过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-02-28更新
|
163次组卷
|
3卷引用:山东省临沂市沂水县第一中学2021-2022学年高一12月段考化学试题
名校
5 . 中国努力争取2060年前实现碳中和,利用NaOH溶液喷淋捕捉空气中的CO2,反应过程如图所示,下列说法错误的
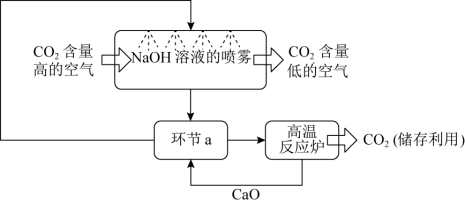

| A.环节a中物质分离的基本操作是过滤 |
| B.捕捉室中NaOH溶液喷成雾状有利于吸收CO2 |
| C.高温反应炉中的物质是Ca(HCO3)2 |
| D.反应过程中只有CaO是可循环的物质 |
您最近一年使用:0次
名校
解题方法
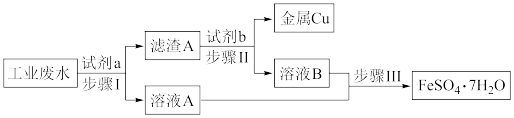
6 . 某工厂的工业废水中含有大量的FeSO4和较多的Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图,回答下列问题:

(1)⑥的操作方法是_______ ,试剂⑦是_______
(2)若取2mL溶液④加入试管中,然后滴加氢气化钠溶液,产生的现象是_______ ;此过程中属于氧化还原反应的化学方程式是_______
(3)溶液②在空气中易被氧化,写出检验溶液②被氧化的具体操作方法_______ ,相应的离子方程式是_______

(1)⑥的操作方法是
(2)若取2mL溶液④加入试管中,然后滴加氢气化钠溶液,产生的现象是
(3)溶液②在空气中易被氧化,写出检验溶液②被氧化的具体操作方法
您最近一年使用:0次
名校
解题方法
7 . 下列除杂试剂及操作方法都正确的是
| A.FeCl3溶液中含有少量的FeCl2,加入铁粉,过滤 |
| B.除去CO2中的少量HCl 气体,通入饱和Na2CO3溶液 |
| C.Cu中含有少量Fe,加入稀硫酸充分反应后,过滤、洗涤、在空气中灼烧干燥 |
| D.Fe中含有少量Al,加入氢氧化钠溶液充分反应后,过滤、洗涤、低温晾干 |
您最近一年使用:0次
名校
8 . 某工业废水中含有大量的Cu2+、Fe3+、Fe2+和 ,拟从该废水中回收金属铜并制得绿矾(FeSO4·7H2O),工艺流程如下图:
,拟从该废水中回收金属铜并制得绿矾(FeSO4·7H2O),工艺流程如下图:
(1)下列叙述正确的是___________。
(2)步骤Ⅰ发生反应的离子方程式为Fe+Cu2+=Fe2++Cu和___________ 。
(3)取2mL溶液A于试管中,滴加少量NaOH溶液,观察到的实验现象是___________ 。
(4)获得的绿矾晶体(FeSO4·7H2O)可能有部分被氧化,请设计检验方案验证(操作、现象、结论)___________ 。
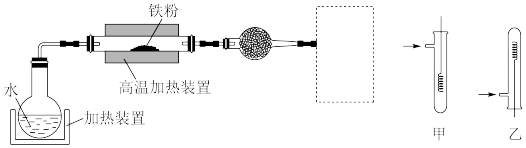
(5)已知:3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g)。虚线框处宜选择的装置是
Fe3O4(s)+4H2(g)。虚线框处宜选择的装置是___________ (填“甲”或“乙”)。
 ,拟从该废水中回收金属铜并制得绿矾(FeSO4·7H2O),工艺流程如下图:
,拟从该废水中回收金属铜并制得绿矾(FeSO4·7H2O),工艺流程如下图:
(1)下列叙述正确的是___________。
| A.滤渣A为Fe和Cu的混合物 |
| B.试剂b为盐酸 |
| C.步骤Ⅱ可以分离出Cu,并能得到FeSO4溶液 |
| D.步骤Ⅲ为蒸发溶液 |
(3)取2mL溶液A于试管中,滴加少量NaOH溶液,观察到的实验现象是
(4)获得的绿矾晶体(FeSO4·7H2O)可能有部分被氧化,请设计检验方案验证(操作、现象、结论)
(5)已知:3Fe(s)+4H2O(g)
 Fe3O4(s)+4H2(g)。虚线框处宜选择的装置是
Fe3O4(s)+4H2(g)。虚线框处宜选择的装置是
您最近一年使用:0次
2022-02-20更新
|
150次组卷
|
2卷引用:浙江省桐乡市高级中学2021-2022学年高一12月阶段教学质量检测化学试题
9 . 对于实验操作和的实验室突发事件应对措施不恰当 的是


| A.上图标志提醒进行化学实验需要佩戴护目镜,以保护眼睛 |
| B.往装有浓硫酸的烧杯中加入适量水稀释,然后用玻璃棒引流转移至容量瓶 |
| C.不慎将碱液沾到皮肤上,应立即用大量水冲洗,然后涂上1%的硼酸溶液 |
D.除去NaCl中的Mg2+、 、Ca2+,可依次加入BaCl2、NaOH、Na2CO3溶液后过滤,再加适量盐酸 、Ca2+,可依次加入BaCl2、NaOH、Na2CO3溶液后过滤,再加适量盐酸 |
您最近一年使用:0次
名校
10 . 图为海水综合利用的部分流程,下列说法正确的是


A.试剂①为过量 ,试剂②为过量的盐酸 ,试剂②为过量的盐酸 |
| B.在实验室完成步骤Ⅰ、Ⅱ、Ⅲ所需实验仪器相同 |
| C.每提取80g液溴,理论上消耗标准状况下的氯气22.4L |
| D.要解决海水提溴过程中对设备的腐蚀,该过程最好在铁制容器中进行 |
您最近一年使用:0次
2022-02-20更新
|
163次组卷
|
2卷引用:江苏省常熟中学2021-2022学年高一12月阶段学习质量检测化学试题



