1 . 已知 晶体在加热条件下发生如下反应:
晶体在加热条件下发生如下反应: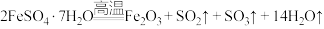 (已知:
(已知: 和
和 的熔点分别为-72.7℃、16.8℃,沸点分别为-10℃、44.8℃);利用下图装置可检验该反应的气体产物。下列说法错误的是
的熔点分别为-72.7℃、16.8℃,沸点分别为-10℃、44.8℃);利用下图装置可检验该反应的气体产物。下列说法错误的是
 晶体在加热条件下发生如下反应:
晶体在加热条件下发生如下反应: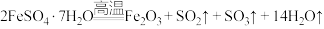 (已知:
(已知: 和
和 的熔点分别为-72.7℃、16.8℃,沸点分别为-10℃、44.8℃);利用下图装置可检验该反应的气体产物。下列说法错误的是
的熔点分别为-72.7℃、16.8℃,沸点分别为-10℃、44.8℃);利用下图装置可检验该反应的气体产物。下列说法错误的是
| A.仪器的连接顺序为a、f(或g)、g(或f)、h、i、d、e、b |
B.装置C中的X溶液为 溶液 溶液 |
| C.装置B的作用为处理尾气 |
D.反应中每生成 ,转移2mol电子 ,转移2mol电子 |
您最近一年使用:0次
解题方法
2 . 某小组探究Na2CO3和NaHCO3的性质。
(1)探究溶解性。在两支试管中,分别加入约1g Na2CO3和NaHCO3固体,分别加入5mL水,充分振荡后,一支试管中固体有剩余,剩余的固体是______ 。
(2)探究稳定性。按照如图所示装置进行实验(部分夹持装置已略去)。
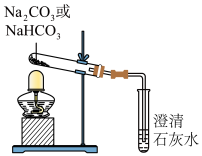
①能够证明Na2CO3的热稳定性强于NaHCO3的证据是______ 。
②NaHCO3受热分解的化学方程式是______ 。
(3)探究与酸的反应。
(4)该小组在探究Na2CO3和NaHCO3的性质时,运用的化学思想方法有______ (填序号)。
a.比较 b.定性与定量相结合
(1)探究溶解性。在两支试管中,分别加入约1g Na2CO3和NaHCO3固体,分别加入5mL水,充分振荡后,一支试管中固体有剩余,剩余的固体是
(2)探究稳定性。按照如图所示装置进行实验(部分夹持装置已略去)。

①能够证明Na2CO3的热稳定性强于NaHCO3的证据是
②NaHCO3受热分解的化学方程式是
(3)探究与酸的反应。
实验步骤 | 实现现象 | 用离子方程式解释现象 |
向盛有Na2CO3溶液的试管中滴加稀盐酸 | 开始无气泡产生,一段时间后产生气泡 | ① ② |
向盛有NaHCO3溶液的试管中滴加稀盐酸 | 立即产生气泡 |
(4)该小组在探究Na2CO3和NaHCO3的性质时,运用的化学思想方法有
a.比较 b.定性与定量相结合
您最近一年使用:0次
3 . 化学兴趣小组课外实验时,取出镁条,发现久置的镁条有一层灰黑色的“外衣”他们把该镁条放入试管中,倒入一定浓度的盐酸,观察到有气泡产生,试管壁发烫。同学们对此气体成分产生了兴趣。
【提出问题】产生的气体是什么?
【查阅资料】i.灰黑色“外衣”中含有
ii.无水 遇水由白色变为蓝色
遇水由白色变为蓝色
【猜想假设】猜想一: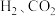
猜想二: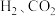 和水蒸气
和水蒸气
猜想三: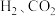 、水蒸气和HCl气体
、水蒸气和HCl气体
(1)猜想三中有HCl气体的理由是___________ 。
【设计实验】为检测产生的气体成分,同学们设计如图所示装置进行实验(部分固定装置略去)
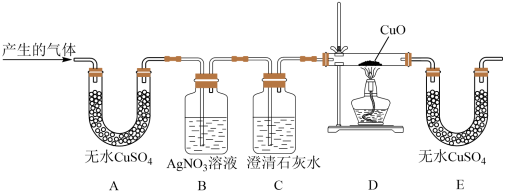
(2)B装置中出现白色沉淀,证明产生的气体中含有___________ ,写出有关的化学方程式___________ 。
(3)C装置的作用是___________ 。
(4)甲同学观察到E装置中无水 由白色变为蓝色,于是得出结论:产生的气体中一定含有H2。乙同学对此提出质疑,理由是
由白色变为蓝色,于是得出结论:产生的气体中一定含有H2。乙同学对此提出质疑,理由是___________ 。
(5)若颠倒B装置和C装置的安装顺序,___________ (填“能”或“不能”)达到实验目的,原因是___________ 。
【反思与评价】
(6)从安全角度考虑,你认为实验时应注意___________ 。
【提出问题】产生的气体是什么?
【查阅资料】i.灰黑色“外衣”中含有

ii.无水
 遇水由白色变为蓝色
遇水由白色变为蓝色【猜想假设】猜想一:
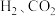
猜想二:
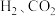 和水蒸气
和水蒸气猜想三:
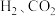 、水蒸气和HCl气体
、水蒸气和HCl气体(1)猜想三中有HCl气体的理由是
【设计实验】为检测产生的气体成分,同学们设计如图所示装置进行实验(部分固定装置略去)

(2)B装置中出现白色沉淀,证明产生的气体中含有
(3)C装置的作用是
(4)甲同学观察到E装置中无水
 由白色变为蓝色,于是得出结论:产生的气体中一定含有H2。乙同学对此提出质疑,理由是
由白色变为蓝色,于是得出结论:产生的气体中一定含有H2。乙同学对此提出质疑,理由是(5)若颠倒B装置和C装置的安装顺序,
【反思与评价】
(6)从安全角度考虑,你认为实验时应注意
您最近一年使用:0次
名校
解题方法
4 . 根据如图所示实验回答问题。

(1)A中,仪器a的名称是___________ ;KMnO4制取O2的化学方程式为___________ ;选择向上排空气法收集氧气的原因是___________ 。
(2)B中,铁丝燃烧生成的黑色固体是___________ 。
(3)C中,能说明木炭在氧气中燃烧的产物为二氧化碳的现象是___________ ;验证产物发生的化学方程式为___________ 。

(1)A中,仪器a的名称是
(2)B中,铁丝燃烧生成的黑色固体是
(3)C中,能说明木炭在氧气中燃烧的产物为二氧化碳的现象是
您最近一年使用:0次
5 . 下列有关常见气体成分检验的结论正确的是
| 选项 | 仪器或试剂 | 实验现象 | 结论 |
| A | 湿润的红色石蕊试纸 | 试纸变蓝 | 一定含 |
| B | 灼热CuO | 黑色固体变为红色 | 一定含 |
| C | 澄清石灰水 | 溶液中出现浑浊 | 一定含 |
| D | 湿润的淀粉-KI试纸 | 试纸变蓝 | 一定含 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-05更新
|
151次组卷
|
2卷引用:2022年夏季山东普通高中学业水平考试化学试题
名校
解题方法
6 . 王老师上课做了“木炭在氧气中燃烧”的实验:将点燃的木炭缓缓地伸入集满氧气的集气瓶中,将木炭取出后向集气瓶中倒入少量澄清石灰水后振荡,让大家观察。
请回答下列问题:
(1)老师“缓慢”地将木炭伸入集气瓶的原因是___________
(2)木炭伸入集气瓶中后所观察到的现象是:___________ ,大家根据___________ 现象,可判断木炭燃烧时生成了二氧化碳。
(3)小华看到老师实验时从集气瓶中取出的木炭已经熄灭,猜想实验时生成的气体中还有___________ 气体。下课后,小华将自己的想法说给老师听,在老师的帮助下,小华对集气瓶中的气体作如下探究:

实验中,当观察到___________ 现象,说明小华的猜想是正确的,请写出直玻璃管中发生反应的化学方程式:___________ 。
(4)从对此实验中生成物的分析可知:反应物的浓度对反应有的影响是___________ 。通过检验,集气瓶中还有氧气剩余,请设计实验进行验证___________ 。
请回答下列问题:
(1)老师“缓慢”地将木炭伸入集气瓶的原因是___________
| A.让同学们观察得更清楚 | B.让木炭与氧气充分反应 |
| C.保证实验时的安全 | D.老师的动作都很慢 |
(3)小华看到老师实验时从集气瓶中取出的木炭已经熄灭,猜想实验时生成的气体中还有

实验中,当观察到
(4)从对此实验中生成物的分析可知:反应物的浓度对反应有的影响是
您最近一年使用:0次
7 . 为探究某液态化合物X(仅含三种短周期元素)的组成和性质,某学习小组进行了如图实验:
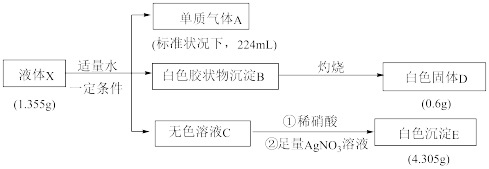
已知:白色固体D是光导纤维的主要成分。请回答:
(1)组成X的三种元素的名称是______ 。
(2)由白色固体D制备的光导纤维作通讯材料时,遇强碱性溶液易造成断路,请用离子方程式解释其原因______ 。
(3)写出液体X与适量水在一定条件下反应的化学方程式______ 。
(4)设计实验检验单质气体A______ 。

已知:白色固体D是光导纤维的主要成分。请回答:
(1)组成X的三种元素的名称是
(2)由白色固体D制备的光导纤维作通讯材料时,遇强碱性溶液易造成断路,请用离子方程式解释其原因
(3)写出液体X与适量水在一定条件下反应的化学方程式
(4)设计实验检验单质气体A
您最近一年使用:0次
解题方法
8 . 氯元素能与许多元素形成种类繁多的化合物,这些含氯化合物在生活及工农业生产中发挥着重要的作用。
(1)从海水中获取粗盐的方法是_______ 。
(2)利用电解饱和食盐水可以制备氢气、氯气、氢氧化钠。电解时阳极产物为_______ ,该产物的检验方法为_______ 。
(3)工业上用氯气和消石灰反应制备漂白粉,其有效成分是_______ (填化学式);写出漂白粉露置在空气中失效过程中所涉及的化学方程式:_______ 、_______ 。
(4)H2与Cl2在点燃条件下可以制取HCl。某同学对HCl性质进行如下预测:
①从物质类别上看,HCl属于酸,其水溶液能与碳酸钙反应,相应的离子方程式为_______ 。
②从化合价角度看,HCl中的Cl元素显-1价,处于氯元素的最低价,因此-1价的Cl元素在反应中可以被_______ (选填“氧化”或“还原”),在一定条件下能与_______ 发生氧化还原反应(填编号)。
a.KI b.NaOH c.KMnO4
(5)已知HClO4是强酸,HClO4在水中的电离方程式为_______ 。
(1)从海水中获取粗盐的方法是
(2)利用电解饱和食盐水可以制备氢气、氯气、氢氧化钠。电解时阳极产物为
(3)工业上用氯气和消石灰反应制备漂白粉,其有效成分是
(4)H2与Cl2在点燃条件下可以制取HCl。某同学对HCl性质进行如下预测:
①从物质类别上看,HCl属于酸,其水溶液能与碳酸钙反应,相应的离子方程式为
②从化合价角度看,HCl中的Cl元素显-1价,处于氯元素的最低价,因此-1价的Cl元素在反应中可以被
a.KI b.NaOH c.KMnO4
(5)已知HClO4是强酸,HClO4在水中的电离方程式为
您最近一年使用:0次
解题方法
9 . 某同学欲在实验中利用一氧化碳还原氧化铁反应的实验,实验装置如图甲所示。
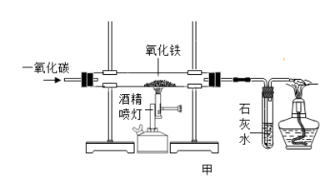
回答下列问题:
(1)硬质玻璃管中实验现象为___________ 发生反应的化学方程式___________
(2)下面是甲装置的基本操作步骤:①点燃酒精喷灯给氧化铁加热;②停止通入一氧化碳。;③熄灭酒精喷灯,继续通一氧化碳直至装置冷却(防止刚生成的铁在高温下又与氧气反应,使实验失败);④先通入一氧化碳一段时间(目的是排尽玻璃管内的空气,防止加热时玻璃管内的一氧化碳与空气的混合气体发生爆炸)正确的排序为:___________
(3)装置中链接澄清石灰水的作用是___________ ;请写出相关的的离子方程式:___________
(4)实验室加热氯化铵和氢氧化钙固体混合物制取氨气(已知:氨气密度比空气小,极易溶于水,与空气不反应),则实验室制取氨气选用的实验装置组合为___________ (填字母)
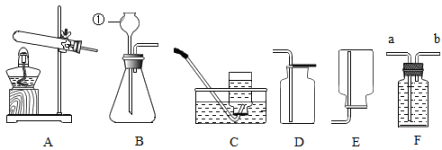
(5)仪器①的名称为___________ 。

回答下列问题:
(1)硬质玻璃管中实验现象为
(2)下面是甲装置的基本操作步骤:①点燃酒精喷灯给氧化铁加热;②停止通入一氧化碳。;③熄灭酒精喷灯,继续通一氧化碳直至装置冷却(防止刚生成的铁在高温下又与氧气反应,使实验失败);④先通入一氧化碳一段时间(目的是排尽玻璃管内的空气,防止加热时玻璃管内的一氧化碳与空气的混合气体发生爆炸)正确的排序为:
(3)装置中链接澄清石灰水的作用是
(4)实验室加热氯化铵和氢氧化钙固体混合物制取氨气(已知:氨气密度比空气小,极易溶于水,与空气不反应),则实验室制取氨气选用的实验装置组合为

(5)仪器①的名称为
您最近一年使用:0次
10 . 人体呼出气体中主要含有氮气、氧气、水蒸气、二氧化碳。为验证人体呼出气体的成分,某兴趣小组利用下面装置进行实验。请回答:
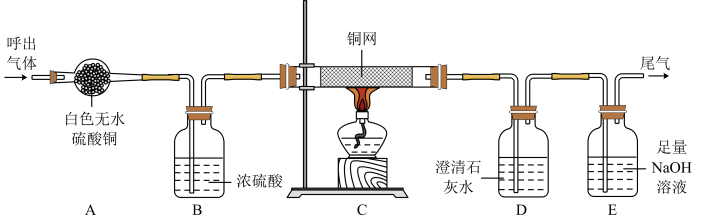
(1)呼出气体通过装置A可观察到_______ ,目的是_______ ;
(2)随反应进行,装置中铜网逐渐变为黑色,其反应的化学方程式为_______ 。
(3)装置D出现白色浑浊,证明呼出的气体中含有_______ 。
(4)E装置的作用是_______ 。

(1)呼出气体通过装置A可观察到
(2)随反应进行,装置中铜网逐渐变为黑色,其反应的化学方程式为
(3)装置D出现白色浑浊,证明呼出的气体中含有
(4)E装置的作用是
您最近一年使用:0次
2022-09-07更新
|
84次组卷
|
2卷引用:山东省临沂市重点中学2022-2023学年高一上学期9月入学考试化学试题



