名校
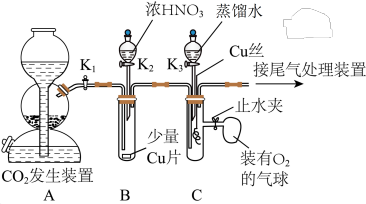
1 . 某兴趣小组设计实验验证铜与浓硝酸、稀硝酸的反应,装置如图所示(夹持装置未画出):
按图示连接好装置,_______后,装入药品,关闭 、
、 ,打开
,打开 ,一段时间后,再关闭
,一段时间后,再关闭 ,打开
,打开 ,加入足量的浓
,加入足量的浓 。
。
实验二:验证铜与稀硝酸的反应
待装置B中反应完全后……
回答下列有关问题:
(1)实验一中的横线上应填入的内容是_______ ;装置B中装浓硝酸的仪器名称是_______ 。
(2)实验一中“关闭 、
、 ,打开
,打开 ”的目的是
”的目的是_______
(3)装置B中发生反应的离子方程式为_______
(4)实验二的后续操作顺序为_______ (填标号),打开止水夹后装置C的具支试管中的现象为_______ 。
a.打开止水夹 b.打开 c.打开
c.打开 ,加入蒸馏水 d.关闭
,加入蒸馏水 d.关闭 e.插入铜丝。
e.插入铜丝。
(5)实验结束后,有同学观察到装置B中溶液呈绿色,装置C中溶液呈蓝色。小组同学认为颜色不同的原因可能如下:
猜想1:硝酸铜溶液的物质的量浓度不同,溶液颜色不同,浓度小时呈蓝色,浓度大时呈绿色。
猜想2: 溶解在硝酸铜溶液中,导致溶液颜色不同。
溶解在硝酸铜溶液中,导致溶液颜色不同。
继续实验,打开 ,一段时间后,装置B中溶液变为蓝色,说明
,一段时间后,装置B中溶液变为蓝色,说明_______ 可能成立,请设计实验验证另一猜想的可能性:_______ 。
按图示连接好装置,_______后,装入药品,关闭
 、
、 ,打开
,打开 ,一段时间后,再关闭
,一段时间后,再关闭 ,打开
,打开 ,加入足量的浓
,加入足量的浓 。
。实验二:验证铜与稀硝酸的反应
待装置B中反应完全后……
回答下列有关问题:
(1)实验一中的横线上应填入的内容是
(2)实验一中“关闭
 、
、 ,打开
,打开 ”的目的是
”的目的是(3)装置B中发生反应的离子方程式为
(4)实验二的后续操作顺序为
a.打开止水夹 b.打开
 c.打开
c.打开 ,加入蒸馏水 d.关闭
,加入蒸馏水 d.关闭 e.插入铜丝。
e.插入铜丝。(5)实验结束后,有同学观察到装置B中溶液呈绿色,装置C中溶液呈蓝色。小组同学认为颜色不同的原因可能如下:
猜想1:硝酸铜溶液的物质的量浓度不同,溶液颜色不同,浓度小时呈蓝色,浓度大时呈绿色。
猜想2:
 溶解在硝酸铜溶液中,导致溶液颜色不同。
溶解在硝酸铜溶液中,导致溶液颜色不同。继续实验,打开
 ,一段时间后,装置B中溶液变为蓝色,说明
,一段时间后,装置B中溶液变为蓝色,说明
您最近一年使用:0次
2024-06-01更新
|
384次组卷
|
4卷引用:2024届辽宁省沈阳市第二中学高三下学期三模化学试题
2 . 物质的性质除主要与物质的结构有关外还与外界条件有关。有人提出“ 与干燥的
与干燥的 不反应”和“
不反应”和“ 与潮湿的
与潮湿的 才能反应”,某小组设计如下实验路线。
才能反应”,某小组设计如下实验路线。___________ 。
(2)为了验证 与干燥的
与干燥的 是否反应,连接好装置,X是
是否反应,连接好装置,X是___________ 。打开___________ ,关闭___________ ,打开分液漏斗的活塞加入稀硫酸,产生气体一段时间,再在干燥管中装入干燥的 ,继续通入一段时间气体,点燃酒精灯加热铜丝,观察现象。则加入稀硫酸,产生一段时间气体后再点燃酒精灯的目的是
,继续通入一段时间气体,点燃酒精灯加热铜丝,观察现象。则加入稀硫酸,产生一段时间气体后再点燃酒精灯的目的是___________ 。
(3)若打开 ,关闭
,关闭 ,加入稀硫酸,点燃酒精灯,观察到
,加入稀硫酸,点燃酒精灯,观察到___________ 现象,___________ (选填“能”或“不能”)证明潮湿的 与
与 反应产生了
反应产生了 。请用化学方程式解释产生该现象的原因
。请用化学方程式解释产生该现象的原因___________ 。
(4)为验证第(3)实验产生的现象 是否与
是否与 反应,某小组取球形干燥管中反应后的固体溶于水中。然后向溶液中滴加
反应,某小组取球形干燥管中反应后的固体溶于水中。然后向溶液中滴加___________ ,产生___________ 现象说明 参与反应。
参与反应。
 与干燥的
与干燥的 不反应”和“
不反应”和“ 与潮湿的
与潮湿的 才能反应”,某小组设计如下实验路线。
才能反应”,某小组设计如下实验路线。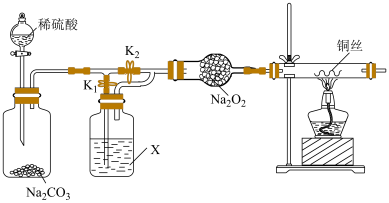
(2)为了验证
 与干燥的
与干燥的 是否反应,连接好装置,X是
是否反应,连接好装置,X是 ,继续通入一段时间气体,点燃酒精灯加热铜丝,观察现象。则加入稀硫酸,产生一段时间气体后再点燃酒精灯的目的是
,继续通入一段时间气体,点燃酒精灯加热铜丝,观察现象。则加入稀硫酸,产生一段时间气体后再点燃酒精灯的目的是(3)若打开
 ,关闭
,关闭 ,加入稀硫酸,点燃酒精灯,观察到
,加入稀硫酸,点燃酒精灯,观察到 与
与 反应产生了
反应产生了 。请用化学方程式解释产生该现象的原因
。请用化学方程式解释产生该现象的原因(4)为验证第(3)实验产生的现象
 是否与
是否与 反应,某小组取球形干燥管中反应后的固体溶于水中。然后向溶液中滴加
反应,某小组取球形干燥管中反应后的固体溶于水中。然后向溶液中滴加 参与反应。
参与反应。
您最近一年使用:0次
2024-05-30更新
|
267次组卷
|
2卷引用:2024届辽宁省部分学校高三下学期联考三模化学试题
名校
解题方法
3 . 某学生配制浓硫酸与浓硝酸的混合酸,当将浓硫酸较快地加入到浓硝酸中时,在容器口产生大量白雾,下列叙述跟解释这一现象无关的是
| A.浓硫酸具有强氧化性 |
| B.硝酸具有挥发性 |
| C.浓硫酸与水作用放出大量的热使浓硝酸挥发 |
| D.硝酸蒸气容易和空气中的水蒸气结合形成白雾 |
您最近一年使用:0次
名校
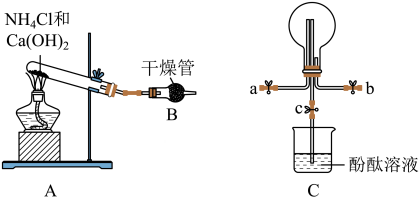
4 . 某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质。______ ;C中圆底烧瓶收集氨气时,请你选择氨气的进气口______ (填“a”或“b”)。
(2)若观察到装置C中的烧瓶内产生了红色喷泉,用化学方程式表示烧瓶内液体变红的原因______ 。
(3)干燥管B中装的试剂是______ (填物质名称)。
(4)以下装置(盛放的液体均为水)可用于吸收多余氨气的是______。(从A-D项中选择)
(2)若观察到装置C中的烧瓶内产生了红色喷泉,用化学方程式表示烧瓶内液体变红的原因
(3)干燥管B中装的试剂是
(4)以下装置(盛放的液体均为水)可用于吸收多余氨气的是______。(从A-D项中选择)
①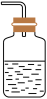 ②
②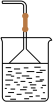 ③
③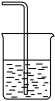 ④
④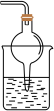
| A.①②③④ | B.①②④ | C.②④ | D.①② |
您最近一年使用:0次
5 . 某小组同学利用以下实验装置研究SO2的性质(经检验,装置的气密性良好)。实验过程中遇到以下问题:___________ 。
(2)ii中观察品红溶液现象___________ 。结论是:SO2有___________ 性。
(3)iii中石蕊溶液变___________ ,说明SO2与H2O反应生成了酸性物质。
(4)iv中观察到的现象是___________ ,离子方程式是:___________ ,结论是:SO2有___________ 性。
(5)v中产生现象___________ ,结论是:SO2有___________ 性。
(6)NaOH溶液的作用是___________ 。反应的离子方程式___________ 。
(7)若将铜丝换成足量铁丝与一定量浓H2SO4反应,随着硫酸溶液变稀得到的两种气体产物依次为___________ 、___________ 。

(2)ii中观察品红溶液现象
(3)iii中石蕊溶液变
(4)iv中观察到的现象是
(5)v中产生现象
(6)NaOH溶液的作用是
(7)若将铜丝换成足量铁丝与一定量浓H2SO4反应,随着硫酸溶液变稀得到的两种气体产物依次为
您最近一年使用:0次
名校
6 . 铜与浓硝酸反应,装置如图。
(1)铜与浓 反应的化学方程式为
反应的化学方程式为___________ 。
(2)分别取3mL浓 与不同质量的纯铜片(铜片均完成溶解)充分反应,反应剧烈,纯铜片逐渐溶解,试管内呈现
与不同质量的纯铜片(铜片均完成溶解)充分反应,反应剧烈,纯铜片逐渐溶解,试管内呈现___________ 色气体,溶液颜色发生变化如下:
取2份等体积①中溶液以相同流速分别通入 和空气,观察现象如下:
和空气,观察现象如下:
溶液呈绿色的可能原因为___________ (填标号),通入气体后,溶液由绿色变为蓝色的原因为___________ (填标号)。
A.硝酸铜溶液就是绿色
B.硝酸铜溶液浓度大
C. 溶解在硝酸铜溶液中
溶解在硝酸铜溶液中
D.溶液通入 时,
时, 被缓慢氧化为
被缓慢氧化为
E.溶液含有某种与绿色有关的还原性微粒,通入空气时较快被氧化
F.空气中的 溶于水显酸性,促进了溶液变蓝色
溶于水显酸性,促进了溶液变蓝色
(3)查阅文献知, 在溶液中存在如下反应:
在溶液中存在如下反应:
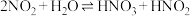 ,
,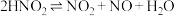
取3份等体积的①中绿色溶液,分别加入不同物质,现象如下:
加入 后溶液迅速变蓝,原因是
后溶液迅速变蓝,原因是 可能参与了下列反应(用化学方程式表示):
可能参与了下列反应(用化学方程式表示):
 ,
,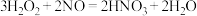 ,
,___________ 。
(4)综上分析,本实验中尾气处理反应的离子方程式为___________ ,硝酸铜溶液中存在___________ (填化学式)参与了形成绿色溶液的过程。

(1)铜与浓
 反应的化学方程式为
反应的化学方程式为(2)分别取3mL浓
 与不同质量的纯铜片(铜片均完成溶解)充分反应,反应剧烈,纯铜片逐渐溶解,试管内呈现
与不同质量的纯铜片(铜片均完成溶解)充分反应,反应剧烈,纯铜片逐渐溶解,试管内呈现| 编号 | ① | ② | ③ | ④ | ⑤ |
| 铜粉质量/g | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 |
| 溶液颜色 | 绿色 | 草绿色 | 蓝绿色偏绿 | 蓝绿色偏蓝 | 蓝色 |
 和空气,观察现象如下:
和空气,观察现象如下:| 通入气体 |  | 空气 |
| 现象 | 液面上方出现明显的红棕色气体,25min后溶液变为蓝色 | 液面上方出现明显的红棕色气体,5min后溶液变为蓝色 |
A.硝酸铜溶液就是绿色
B.硝酸铜溶液浓度大
C.
 溶解在硝酸铜溶液中
溶解在硝酸铜溶液中 D.溶液通入
 时,
时, 被缓慢氧化为
被缓慢氧化为
E.溶液含有某种与绿色有关的还原性微粒,通入空气时较快被氧化
F.空气中的
 溶于水显酸性,促进了溶液变蓝色
溶于水显酸性,促进了溶液变蓝色(3)查阅文献知,
 在溶液中存在如下反应:
在溶液中存在如下反应: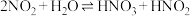 ,
,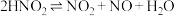
取3份等体积的①中绿色溶液,分别加入不同物质,现象如下:
| 加入物质 |  | 3滴30% 溶液 溶液 | 3滴水 |
| 现象 | 溶液绿色变深 | 溶液迅速变为蓝色 | 溶液颜色几乎不变 |
 后溶液迅速变蓝,原因是
后溶液迅速变蓝,原因是 可能参与了下列反应(用化学方程式表示):
可能参与了下列反应(用化学方程式表示): ,
,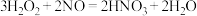 ,
,(4)综上分析,本实验中尾气处理反应的离子方程式为
您最近一年使用:0次
名校
解题方法
7 . 二氧化硫和亚硫酸在工农业生产中具有重要的用途。某化学兴趣小组对 和
和 的一些性质进行了探究。回答下列问题:
的一些性质进行了探究。回答下列问题:
Ⅰ.某同学设计了如图装置用于制取 和验证
和验证 的性质。
的性质。 具有一定氧化性。
具有一定氧化性。
(1)装置A中发生反应的化学方程式为___________ 。
(2)在框图内选择合适装置依次验证 的漂白性、酸性、还原性,上图各装置按气流从左到右方向连接顺序为A→
的漂白性、酸性、还原性,上图各装置按气流从左到右方向连接顺序为A→___________ (填装置字母,还原性设计两个装置)。
(3)实验前必须鼓入 ,目的是
,目的是___________ 。
(4)装置F中产生了白色沉淀,其成分是___________ (化学式)。
(5)实验中发现装置A中 可能部分被氧化,现需测定
可能部分被氧化,现需测定 的纯度:称取
的纯度:称取 样品,配成
样品,配成 溶液;取其中的
溶液;取其中的 溶液,与
溶液,与 酸性
酸性 溶液发生以下反应:
溶液发生以下反应: ,实验消耗
,实验消耗 溶液
溶液 ,以上样品中
,以上样品中 的质量分数为
的质量分数为___________ (保留三位有效数字)。
Ⅱ.探究 的酸性强于
的酸性强于 (可能所需要的装置和试剂如图所示)。
(可能所需要的装置和试剂如图所示)。___________ (填装置标号)。
(7)能证明 的酸性强于
的酸性强于 的现象
的现象___________ 。
 和
和 的一些性质进行了探究。回答下列问题:
的一些性质进行了探究。回答下列问题:Ⅰ.某同学设计了如图装置用于制取
 和验证
和验证 的性质。
的性质。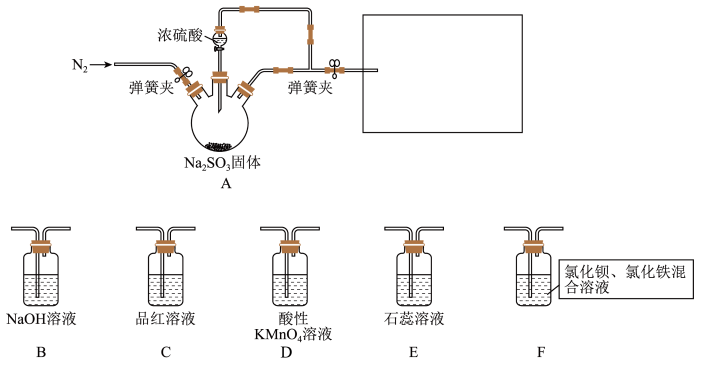
 具有一定氧化性。
具有一定氧化性。(1)装置A中发生反应的化学方程式为
(2)在框图内选择合适装置依次验证
 的漂白性、酸性、还原性,上图各装置按气流从左到右方向连接顺序为A→
的漂白性、酸性、还原性,上图各装置按气流从左到右方向连接顺序为A→(3)实验前必须鼓入
 ,目的是
,目的是(4)装置F中产生了白色沉淀,其成分是
(5)实验中发现装置A中
 可能部分被氧化,现需测定
可能部分被氧化,现需测定 的纯度:称取
的纯度:称取 样品,配成
样品,配成 溶液;取其中的
溶液;取其中的 溶液,与
溶液,与 酸性
酸性 溶液发生以下反应:
溶液发生以下反应: ,实验消耗
,实验消耗 溶液
溶液 ,以上样品中
,以上样品中 的质量分数为
的质量分数为Ⅱ.探究
 的酸性强于
的酸性强于 (可能所需要的装置和试剂如图所示)。
(可能所需要的装置和试剂如图所示)。
(7)能证明
 的酸性强于
的酸性强于 的现象
的现象
您最近一年使用:0次
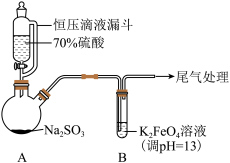
8 . 某实验小组探究SO2与K2FeO4的反应,实验如下。
资料:i.K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
ii.Fe3+可以与C2O 形成[Fe(C2O4)3]3-;
形成[Fe(C2O4)3]3-;
(1)A中产生SO2的化学方程式为___________ 。
(2)暗红褐色沉淀X可能含Fe3+、OH-、SO 、SO
、SO ,检验如下:
,检验如下:
实验二:向X中加入足量盐酸,沉淀溶解。取少量溶液,滴加KSCN溶液后变红。证明溶液中存在___________ 。另取少量溶液滴加BaCl2溶液,产生白色沉淀,但不能确认含有SO ,原因是
,原因是___________ 。
实验三:向X中加入H2C2O4溶液,沉淀溶解。继续滴加BaCl2溶液,产生白色沉淀,过滤后,向沉淀中加入盐酸,白色沉淀溶解。确认X中不含SO 。
。
实验三中用H2C2O4溶液溶解沉淀的目的是:___________ 。
实验四:向X中加入足量盐酸,沉淀溶解。加入几滴碘水(含淀粉),蓝色立即褪去。静置,一段时间后蓝色复现,振荡,不褪色。
结合离子方程式解释沉淀溶解后的现象:___________ 。
(3)查阅资料:a.Fe3+、SO 、H2O(或OH﹣)会形成配合物HOFeOSO2。
、H2O(或OH﹣)会形成配合物HOFeOSO2。 和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
①向溶液Y中滴加2滴KSCN溶液,未见红色;再加几滴6mol·L-1盐酸,溶液变红。溶液Y中存在Fe(Ⅲ),但直接滴加KSCN溶液未见红色的原因是___________ 。
②取出部分实验一中的橙色溶液,久置不褪色。结合资料a中过程ii分析实验一中溶液最终“几乎无色”的原因:___________ 。
总结:SO2与K2FeO4发生了氧化还原反应和复分解反应,并且遵循化学反应速率和限度规律。
资料:i.K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
ii.Fe3+可以与C2O
 形成[Fe(C2O4)3]3-;
形成[Fe(C2O4)3]3-;| 装置 | 操作及现象 |
| 实验一:向B中通入SO2,产生暗红褐色沉淀X和溶液Y(略显红色);继续通入SO2一段时间后,溶液呈红色,继而变为橙色,最终沉淀消失,溶液几乎无色。 |
(1)A中产生SO2的化学方程式为
(2)暗红褐色沉淀X可能含Fe3+、OH-、SO
 、SO
、SO ,检验如下:
,检验如下:实验二:向X中加入足量盐酸,沉淀溶解。取少量溶液,滴加KSCN溶液后变红。证明溶液中存在
 ,原因是
,原因是实验三:向X中加入H2C2O4溶液,沉淀溶解。继续滴加BaCl2溶液,产生白色沉淀,过滤后,向沉淀中加入盐酸,白色沉淀溶解。确认X中不含SO
 。
。实验三中用H2C2O4溶液溶解沉淀的目的是:
实验四:向X中加入足量盐酸,沉淀溶解。加入几滴碘水(含淀粉),蓝色立即褪去。静置,一段时间后蓝色复现,振荡,不褪色。
结合离子方程式解释沉淀溶解后的现象:
(3)查阅资料:a.Fe3+、SO
 、H2O(或OH﹣)会形成配合物HOFeOSO2。
、H2O(或OH﹣)会形成配合物HOFeOSO2。
 和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
①向溶液Y中滴加2滴KSCN溶液,未见红色;再加几滴6mol·L-1盐酸,溶液变红。溶液Y中存在Fe(Ⅲ),但直接滴加KSCN溶液未见红色的原因是
②取出部分实验一中的橙色溶液,久置不褪色。结合资料a中过程ii分析实验一中溶液最终“几乎无色”的原因:
总结:SO2与K2FeO4发生了氧化还原反应和复分解反应,并且遵循化学反应速率和限度规律。
您最近一年使用:0次
2024-04-15更新
|
617次组卷
|
3卷引用:辽宁省大连市大连第二十四中学2023-2024学年高一下学期期中考试化学试卷
辽宁省大连市大连第二十四中学2023-2024学年高一下学期期中考试化学试卷北京市朝阳区2023-2024学年高三下学期一模化学试题(已下线)压轴题12?化学实验综合题(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
9 . 某实验小组在探究 性质时,做了如下实验:
性质时,做了如下实验:
实验Ⅰ:向NaCl溶液中加入 溶液,溶液呈绿色。
溶液,溶液呈绿色。
实验Ⅱ:向 溶液中加入表面打磨掉氧化膜的金属Mg,产生大量气泡同时溶液中产生绿色沉淀。
溶液中加入表面打磨掉氧化膜的金属Mg,产生大量气泡同时溶液中产生绿色沉淀。
实验Ⅲ:向 溶液中加入适量氨水,溶液变为深蓝色。
溶液中加入适量氨水,溶液变为深蓝色。
实验Ⅳ:向实验Ⅲ的深蓝色溶液中加入 溶液,产生蓝色沉淀。
溶液,产生蓝色沉淀。
资料显示: 为黄色,
为黄色, 为绿色不溶物。
为绿色不溶物。
下列说法错误的是
 性质时,做了如下实验:
性质时,做了如下实验:实验Ⅰ:向NaCl溶液中加入
 溶液,溶液呈绿色。
溶液,溶液呈绿色。实验Ⅱ:向
 溶液中加入表面打磨掉氧化膜的金属Mg,产生大量气泡同时溶液中产生绿色沉淀。
溶液中加入表面打磨掉氧化膜的金属Mg,产生大量气泡同时溶液中产生绿色沉淀。实验Ⅲ:向
 溶液中加入适量氨水,溶液变为深蓝色。
溶液中加入适量氨水,溶液变为深蓝色。实验Ⅳ:向实验Ⅲ的深蓝色溶液中加入
 溶液,产生蓝色沉淀。
溶液,产生蓝色沉淀。资料显示:
 为黄色,
为黄色, 为绿色不溶物。
为绿色不溶物。下列说法错误的是
A.实验Ⅰ: 在NaCl溶液中部分转化为 在NaCl溶液中部分转化为 |
B.实验Ⅱ:Mg消耗了溶液中的 从而产生了 从而产生了 |
C.实验Ⅲ:有 生成 生成 |
D.实验Ⅳ:获得的蓝色沉淀为 |
您最近一年使用:0次
10 . 如图是实验室用二氧化锰和浓盐酸制备氯气并进行一系列相关实验的装置(夹持装置已略)。

(1)装置A中盛装浓盐酸的仪器名称为________ ,发生反应的离子方程式为________ 。
(2)装置B中盛装的试剂为________ ,在实验过程中可以起到安全瓶的作用,一旦后续装置堵塞,B中会出现________ 现象。
(3)装置C的作用是证明干燥的 无漂白性,但其水溶液具有漂白性,则Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是
无漂白性,但其水溶液具有漂白性,则Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是________ (填字母,试剂不重复使用)。
a.干燥的石蕊试纸 b.湿润的石蕊试纸
c.碱石灰 d.无水氯化钙
(4)装置E中溶液变蓝色,证明了氯气化学性质中的________ 性;装置F中的试剂为________ 溶液(填化学式)。
(5) 也可以与浓盐酸反应生成氯气,是实验室快速制氯气的方法之一,分别使用
也可以与浓盐酸反应生成氯气,是实验室快速制氯气的方法之一,分别使用 和
和 制备等量的氯气,转移电子数之比为
制备等量的氯气,转移电子数之比为________ 。

(1)装置A中盛装浓盐酸的仪器名称为
(2)装置B中盛装的试剂为
(3)装置C的作用是证明干燥的
 无漂白性,但其水溶液具有漂白性,则Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是
无漂白性,但其水溶液具有漂白性,则Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是a.干燥的石蕊试纸 b.湿润的石蕊试纸
c.碱石灰 d.无水氯化钙
(4)装置E中溶液变蓝色,证明了氯气化学性质中的
(5)
 也可以与浓盐酸反应生成氯气,是实验室快速制氯气的方法之一,分别使用
也可以与浓盐酸反应生成氯气,是实验室快速制氯气的方法之一,分别使用 和
和 制备等量的氯气,转移电子数之比为
制备等量的氯气,转移电子数之比为
您最近一年使用:0次