解题方法
1 . Na2O2具有强氧化性,H2具有还原性,某同学根据氧化还原反应的知识推测Na2O2与H2能发生反应。为了验证此推测结果,该同学设计并进行了如图所示实验。
I.实验探究
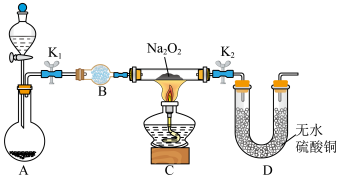
(1)装置A中用粗锌和稀盐酸制收氢气,B装置的作用是________ ,里面所盛放的试剂是_________ (填序号)。
①浓硫酸 ②碱石灰 ③无水硫酸铜
(2)下面是实验过程中的重要操作,正确的顺序是________ (填序号)。
A.加热至Na2O2逐渐熔化,反应一段时间
B.用小试管收集气体并检验其纯度
C.打开K1、K2,滴加稀盐酸
D.停止加热,充分冷却,关闭K1、K2
(3)实验过程中观察到淡黄色粉末慢慢变成白色固体,无水硫酸铜未变蓝色。由此可推测出Na2O2与H2反应生成的产物为________ (填化学式)。
II.数据处理
(4)实验结束后,该同学欲测定C装置内白色固体中未反应完的Na2O2含量,其操作流程如图:
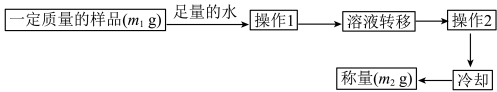
①测定过程中需要的仪器除固定)夹持仪器外,还有天平、烧杯、酒精灯、蒸发皿和_________ ,操作2的名称是_________ 。
②白色固体中Na2O2的质量分数为_______ (用含m1和m2的式子表示)。
③在转移溶液时,若溶液转移不完全,则测得的Na2O2质量分数__________ (填“偏大”“偏小”或“不变”)。
I.实验探究

(1)装置A中用粗锌和稀盐酸制收氢气,B装置的作用是
①浓硫酸 ②碱石灰 ③无水硫酸铜
(2)下面是实验过程中的重要操作,正确的顺序是
A.加热至Na2O2逐渐熔化,反应一段时间
B.用小试管收集气体并检验其纯度
C.打开K1、K2,滴加稀盐酸
D.停止加热,充分冷却,关闭K1、K2
(3)实验过程中观察到淡黄色粉末慢慢变成白色固体,无水硫酸铜未变蓝色。由此可推测出Na2O2与H2反应生成的产物为
II.数据处理
(4)实验结束后,该同学欲测定C装置内白色固体中未反应完的Na2O2含量,其操作流程如图:

①测定过程中需要的仪器除固定)夹持仪器外,还有天平、烧杯、酒精灯、蒸发皿和
②白色固体中Na2O2的质量分数为
③在转移溶液时,若溶液转移不完全,则测得的Na2O2质量分数
您最近一年使用:0次
名校
解题方法
2 . 某研究小组设计如下所示实验装置(夹持装置已略去)分别探究NO与铜粉、Na2O2的反应。
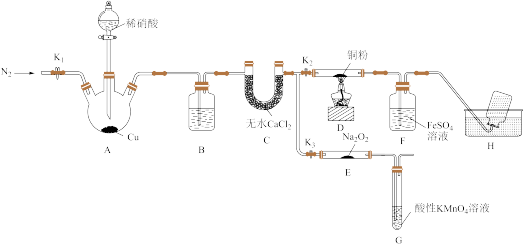
已知:①NO与Na2O2可发生反应2NO+Na2O2=2NaNO2。
②NO能被酸性高锰酸钾溶液氧化为
③在溶液中存在平衡FeSO4+NO⇌Fe(NO)SO4(棕色)
I.关闭K3,打开K2,探究NO与铜粉的反应并检验NO。
(1)反应开始前,打开K1,通入一段时间N2,其目的是_______ 。
(2)装置B中盛放的试剂为水,其作用是_______ 。
(3)装置F中的实验现象为_______ 。装置H中收集的气体为_______ (填化学式)。
(4)铜与稀硝酸反应的离子方程式为_______
II.关闭K2,打开K3,探究NO与Na2O2的反应并制备NaNO2。
(5)装置G的作用是_______ 。
(6)若省略装置C,则进入装置G中的气体除N2、NO外,可能还有_______ (填化学式)。
(7)测定反应后装置E中NaNO2的含量。已知;在酸性条件下, 可将
可将 还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。
还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。
①滴定过程中发生反应的离子方程式为_______ 。
②滴定过程中酸性KMnO4溶液的作用是_______ 。
③样品中NaNO2的质量分数为_______ 用含有a、b的代数式表示)。该实验要迅速操作,否则测定结果会偏小,原因是_______ 。

已知:①NO与Na2O2可发生反应2NO+Na2O2=2NaNO2。
②NO能被酸性高锰酸钾溶液氧化为

③在溶液中存在平衡FeSO4+NO⇌Fe(NO)SO4(棕色)
I.关闭K3,打开K2,探究NO与铜粉的反应并检验NO。
(1)反应开始前,打开K1,通入一段时间N2,其目的是
(2)装置B中盛放的试剂为水,其作用是
(3)装置F中的实验现象为
(4)铜与稀硝酸反应的离子方程式为
II.关闭K2,打开K3,探究NO与Na2O2的反应并制备NaNO2。
(5)装置G的作用是
(6)若省略装置C,则进入装置G中的气体除N2、NO外,可能还有
(7)测定反应后装置E中NaNO2的含量。已知;在酸性条件下,
 可将
可将 还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。
还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。①滴定过程中发生反应的离子方程式为
②滴定过程中酸性KMnO4溶液的作用是
③样品中NaNO2的质量分数为
您最近一年使用:0次
名校
解题方法
3 . 某学校化学兴趣小组设计如下实验探究铁的电化学腐蚀原理。
(1)实验一:甲小组同学设计如图所示装置证明铁发生了电化学腐蚀。
①用电极反应解释实验a的现象:________ 。
②写出实验b中生成蓝色沉淀的离子方程式:________ 。
③已知 具有氧化性。据此有同学认为仅通过实验b的现象不能证明铁发生了电化学腐蚀,理由是
具有氧化性。据此有同学认为仅通过实验b的现象不能证明铁发生了电化学腐蚀,理由是_________ 。
(2)实验二:乙小组同学向如图所示装置的容器a、b中分别加入 的
的 溶液,闭合K,电流计指针未发生偏转。加热容器a,电流计指针向右偏转。
溶液,闭合K,电流计指针未发生偏转。加热容器a,电流计指针向右偏转。
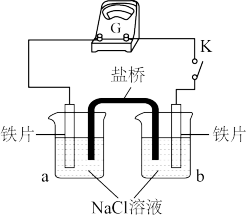
①分别取少量容器a、b中的溶液于试管中,滴加 溶液,容器a中的溶液所在的试管中出现蓝色沉淀,容器b中的溶液所在的试管中无变化,容器b中铁片做
溶液,容器a中的溶液所在的试管中出现蓝色沉淀,容器b中的溶液所在的试管中无变化,容器b中铁片做_______ 极。
②加热后,电流计指针发生偏转的原因可能是_______ 。
(3)实验三:丙小组同学向如图所示装置的容器a、b中各加入 不同质量分数的
不同质量分数的 溶液,实验数据如表所示:
溶液,实验数据如表所示:
则实验Ⅱ的容器b中发生的电极反应是______ 。
(1)实验一:甲小组同学设计如图所示装置证明铁发生了电化学腐蚀。
装置 | 分别进行的实验 | 现象 |
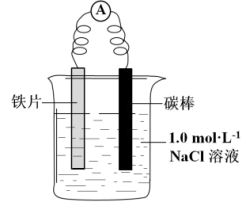 | a.连接好装置,一段时间后,向烧杯中滴加酚酞溶液 | 碳棒附近溶液变红 |
b连接好装置,一段时间后,向烧杯中滴加 溶液 溶液 | 铁片表面产生蓝色沉淀 |
①用电极反应解释实验a的现象:
②写出实验b中生成蓝色沉淀的离子方程式:
③已知
 具有氧化性。据此有同学认为仅通过实验b的现象不能证明铁发生了电化学腐蚀,理由是
具有氧化性。据此有同学认为仅通过实验b的现象不能证明铁发生了电化学腐蚀,理由是(2)实验二:乙小组同学向如图所示装置的容器a、b中分别加入
 的
的 溶液,闭合K,电流计指针未发生偏转。加热容器a,电流计指针向右偏转。
溶液,闭合K,电流计指针未发生偏转。加热容器a,电流计指针向右偏转。
①分别取少量容器a、b中的溶液于试管中,滴加
 溶液,容器a中的溶液所在的试管中出现蓝色沉淀,容器b中的溶液所在的试管中无变化,容器b中铁片做
溶液,容器a中的溶液所在的试管中出现蓝色沉淀,容器b中的溶液所在的试管中无变化,容器b中铁片做②加热后,电流计指针发生偏转的原因可能是
(3)实验三:丙小组同学向如图所示装置的容器a、b中各加入
 不同质量分数的
不同质量分数的 溶液,实验数据如表所示:
溶液,实验数据如表所示:实验标号 | 容器a | 容器b | 电流计指针偏转方向 |
Ⅰ | 0.1% | 0.01% | 向右 |
Ⅱ | 0.1% | 3.5% | 向左 |
Ⅲ | 3.5% | 饱和溶液 | 向右 |
则实验Ⅱ的容器b中发生的电极反应是
您最近一年使用:0次
2020-09-19更新
|
279次组卷
|
4卷引用:江西省景德镇一中2020-2021学年高一下学期期中考试化学(1班)试题



