名校
1 . 完成下列问题。
(1)氮的氧化物是主要的大气污染物,对大气的影响之一是导致酸雨。用化学方程式表示NO2形成酸雨的原因___________ ,该反应中氧化剂和还原剂的物质的量之比为___________ 。
(2)实验室常用的几种气体发生装置如图A、B、C所示:
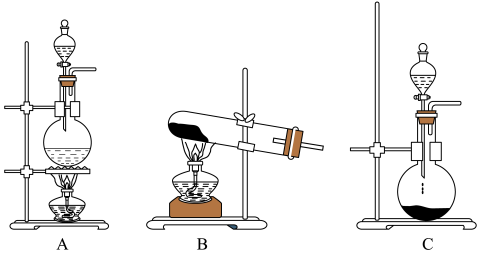
①实验室可以用B或C装置制取氨气,如果用B装置,通常使用的药品是___________ ;
②如图1是某学生设计收集氨气的几种装置,其中可行的是___________ 。

(3)某兴趣小组用如图2装置制备氨气,并探究氨气的还原性并检验产物。
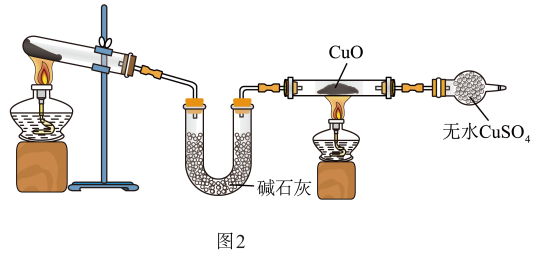
①实验现象为:黑色CuO变为红色;白色无水CuSO4粉末变为蓝色;同时生成一种无色气体,该气体无污染。请写出氨气与CuO反应的化学方程式___________ 。
②该装置中碱石灰的作用是干燥氨气,无水CuSO4检验反应有水的生成,该装置存在明显缺陷,请提出改进意见___________ 。
③有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。已知:在酸性溶液中Cu2O+2H+=Cu+Cu2++2H2O,请你设计一个简单的实验检验该红色物质中是否含有Cu2O_______ 。
(1)氮的氧化物是主要的大气污染物,对大气的影响之一是导致酸雨。用化学方程式表示NO2形成酸雨的原因
(2)实验室常用的几种气体发生装置如图A、B、C所示:

①实验室可以用B或C装置制取氨气,如果用B装置,通常使用的药品是
②如图1是某学生设计收集氨气的几种装置,其中可行的是

(3)某兴趣小组用如图2装置制备氨气,并探究氨气的还原性并检验产物。

①实验现象为:黑色CuO变为红色;白色无水CuSO4粉末变为蓝色;同时生成一种无色气体,该气体无污染。请写出氨气与CuO反应的化学方程式
②该装置中碱石灰的作用是干燥氨气,无水CuSO4检验反应有水的生成,该装置存在明显缺陷,请提出改进意见
③有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。已知:在酸性溶液中Cu2O+2H+=Cu+Cu2++2H2O,请你设计一个简单的实验检验该红色物质中是否含有Cu2O
您最近一年使用:0次
2023-07-13更新
|
76次组卷
|
2卷引用:江西省萍乡市安源中学2022-2023学年高一下学期期中考试化学试题
2 . 某化学兴趣小组对教材中乙醇性质及产物检验的实验进行了改进和创新,其改进后的实验装置如图所示,按图组装好仪器,装好试剂。
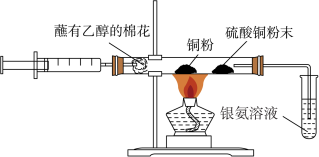
下列叙述正确的是

下列叙述正确的是
| A.因乙醇具有氧化性,所以医疗上常用75%(体积分数)的乙醇溶液作消毒液 |
| B.点燃酒精灯,轻轻推动注射器活塞即可实现乙醇的催化氧化及部分产物的检验 |
| C.可用酸性高锰酸钾溶液来鉴别乙烯、乙醇 |
| D.实验中铜粉和硫酸铜粉末颜色的变化,说明乙醇发生了还原反应 |
您最近一年使用:0次
2023-07-08更新
|
159次组卷
|
3卷引用:江西省萍乡市安源中学2022-2023学年高一下学期期末考试化学试题
3 . 某化学小组同学欲按如图装置进行实验,探究NH3催化氧化反应。

A、B装置可选药品:浓氨水、H2O2、蒸馏水、NaOH固体、MnO2
(1)装置A用于制取氧气,其发生反应的化学方程式是_______ 。
(2)装置D的名称是______ ,其所装试剂是_______ 。
(3)装置E中发生反应的化学方程式是______ 。
(4)实验一段时间后,观察到装置F中有红棕色气体,生成红棕色气体的化学方程式是_______ ,用离子方程式表示G中溶液变成蓝色的原因:_______ 。
(5)可用如图所示的装置替换上述装置中虚线框部分,化合物X为_______ 。NH4HCO3的作用是______ 。


A、B装置可选药品:浓氨水、H2O2、蒸馏水、NaOH固体、MnO2
(1)装置A用于制取氧气,其发生反应的化学方程式是
(2)装置D的名称是
(3)装置E中发生反应的化学方程式是
(4)实验一段时间后,观察到装置F中有红棕色气体,生成红棕色气体的化学方程式是
(5)可用如图所示的装置替换上述装置中虚线框部分,化合物X为

您最近一年使用:0次
名校
4 . 图(1)是实验室合成溴苯并检验其部分生成物的装置,下列说法错误的是( )
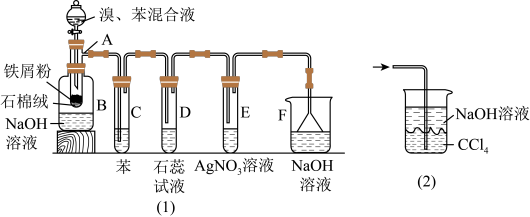
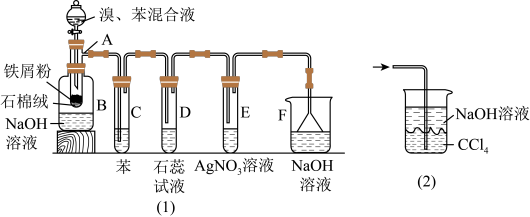
A.苯和液溴在A中发生反应的化学方程式为: +Br2 +Br2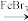 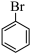 +HBr +HBr |
| B.实验中C中的液体逐渐变为浅红色,是因为溴具有挥发性 |
| C.D、E、F均具有防倒吸的作用,其中F不可以用图(2)所示装置代替 |
| D.D中石蕊试液慢慢变红,E中产生浅黄色沉淀 |
您最近一年使用:0次
2020-04-07更新
|
510次组卷
|
4卷引用:江西省萍乡市麻山中学2020届高三下学期5月第二次教学质量检测理科综合化学试题
5 . 新制氯水中含有多种粒子,某校化学研究性学习小组的同学为探究其性质,做了如下实验,请你帮助完成:

(1)氯碱工业生产中同时有副产品氯气生成,反应的化学方程式为____________ 。
(2)新制的饱和氯水与碳酸钙反应时制取较浓HClO溶液的方法之一。
实验一:定性研究
A 在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;
B 过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
C 为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生。经检测,上述实验中产生的无色气体均为CO2。
①已知:Ka1(H2CO3)=4.45×10-7,Ka2(HCO3-)=5.61×10-11,Ka(HClO)=2.95×10-8,写出将少量的氯气通入到过量的碳酸钠溶液中所发生反应的离子方程式:____________ 。
②试推测步骤B的滤液中的溶质除了CaCl2,HClO外,还有____________ 。
实验二:定量研究
在仪器A内放有用塑料网包住的块状碳酸钙(过量)和150mL新制饱和氯水,按如图所示的装置进行实验(实验前仪器B中充满了饱和NaHCO3溶液,部分夹持装置已省略),待不再产出气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热A中的液体,直到仪器B中的气体不再增加(不考虑HClO的分解)。
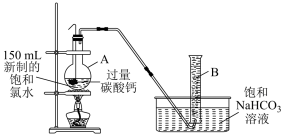
③仪器A的名称为__________ 。
④准确读出仪器B中气体体积的实验操作步骤依次是:
a.____________ ;
b.____________ ;
c.平视与刻度线相切的液面读数。
⑤实验结束后,测得仪器B中收集到的气体体积在标准状况下为168mL,则150mL新制的饱和氯水与过量碳酸钙完全反应后,所得溶液中HClO的物质的量浓度为__________ 。(反应前后,溶液体积变化忽略不计)。

(1)氯碱工业生产中同时有副产品氯气生成,反应的化学方程式为
(2)新制的饱和氯水与碳酸钙反应时制取较浓HClO溶液的方法之一。
实验一:定性研究
A 在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;
B 过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
C 为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生。经检测,上述实验中产生的无色气体均为CO2。
①已知:Ka1(H2CO3)=4.45×10-7,Ka2(HCO3-)=5.61×10-11,Ka(HClO)=2.95×10-8,写出将少量的氯气通入到过量的碳酸钠溶液中所发生反应的离子方程式:
②试推测步骤B的滤液中的溶质除了CaCl2,HClO外,还有
实验二:定量研究
在仪器A内放有用塑料网包住的块状碳酸钙(过量)和150mL新制饱和氯水,按如图所示的装置进行实验(实验前仪器B中充满了饱和NaHCO3溶液,部分夹持装置已省略),待不再产出气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热A中的液体,直到仪器B中的气体不再增加(不考虑HClO的分解)。

③仪器A的名称为
④准确读出仪器B中气体体积的实验操作步骤依次是:
a.
b.
c.平视与刻度线相切的液面读数。
⑤实验结束后,测得仪器B中收集到的气体体积在标准状况下为168mL,则150mL新制的饱和氯水与过量碳酸钙完全反应后,所得溶液中HClO的物质的量浓度为
您最近一年使用:0次



