1 . 为了探究 、
、 同时通入
同时通入 中发生的反应,某校化学兴趣小组同学设计了如图所示的实验装置。
中发生的反应,某校化学兴趣小组同学设计了如图所示的实验装置。 、
、 气体,现采用
气体,现采用 固体与
固体与 的硫酸为原料制取
的硫酸为原料制取 ,采用
,采用 和浓盐酸(
和浓盐酸( )为原料制取
)为原料制取 。在此实验中,F仪器的作用是
。在此实验中,F仪器的作用是___________ ;发生装置B应选择以下三种装置中的___________ (填①或②或③)。___________ ,写出气体发生装置B中主要反应的离子方程式___________ 。
(3)将适量的蔗糖放入烧杯中,加少量水拌匀,再加适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。上述现象体现了浓硫酸的___________ (填序号)①酸性②吸水性③脱水性④强氧化性,请写出“体积膨胀,并放出有刺激性气味的气体”对应的化学方程式:___________ 。
(4)为验证通入D装置中的气体是 过量还是
过量还是 过量,兴趣小组的同学准备了以下试剂:a.氯化铁溶液b.氯化亚铁溶液c.硫氰化钾溶液d.氯化钡溶液e.品红溶液f.酸性高锰酸钾溶液;
过量,兴趣小组的同学准备了以下试剂:a.氯化铁溶液b.氯化亚铁溶液c.硫氰化钾溶液d.氯化钡溶液e.品红溶液f.酸性高锰酸钾溶液;
若 过量,取适量D中溶液滴加至盛有
过量,取适量D中溶液滴加至盛有___________ (选填一个序号)试剂的试管内,再加入___________ (选填一个序号)试剂,发生的现象是___________ 。
 、
、 同时通入
同时通入 中发生的反应,某校化学兴趣小组同学设计了如图所示的实验装置。
中发生的反应,某校化学兴趣小组同学设计了如图所示的实验装置。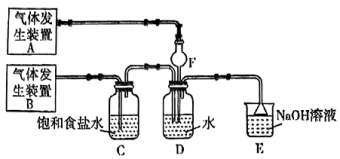
 、
、 气体,现采用
气体,现采用 固体与
固体与 的硫酸为原料制取
的硫酸为原料制取 ,采用
,采用 和浓盐酸(
和浓盐酸( )为原料制取
)为原料制取 。在此实验中,F仪器的作用是
。在此实验中,F仪器的作用是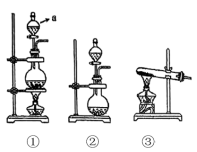
(3)将适量的蔗糖放入烧杯中,加少量水拌匀,再加适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。上述现象体现了浓硫酸的
(4)为验证通入D装置中的气体是
 过量还是
过量还是 过量,兴趣小组的同学准备了以下试剂:a.氯化铁溶液b.氯化亚铁溶液c.硫氰化钾溶液d.氯化钡溶液e.品红溶液f.酸性高锰酸钾溶液;
过量,兴趣小组的同学准备了以下试剂:a.氯化铁溶液b.氯化亚铁溶液c.硫氰化钾溶液d.氯化钡溶液e.品红溶液f.酸性高锰酸钾溶液;若
 过量,取适量D中溶液滴加至盛有
过量,取适量D中溶液滴加至盛有
您最近半年使用:0次
名校
解题方法
2 . 将 分别通入如图四种溶液中,现象及
分别通入如图四种溶液中,现象及 表现的性质均正确的是
表现的性质均正确的是
 分别通入如图四种溶液中,现象及
分别通入如图四种溶液中,现象及 表现的性质均正确的是
表现的性质均正确的是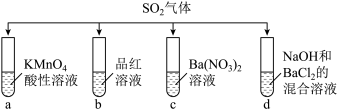
A.酸性 溶液褪色, 溶液褪色, 表现氧化性 表现氧化性 |
B.品红溶液先褪色,加热后又重新变红, 表现还原性 表现还原性 |
C.c溶液中出现白色沉淀, 表现还原性和酸性 表现还原性和酸性 |
D.d溶液中无明显现象, 表现酸性 表现酸性 |
您最近半年使用:0次
名校
解题方法
3 . 二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。
(1)工业上用黄铁矿(主要成分为 ,其中硫元素为
,其中硫元素为 价)在高温条件下和氧气反应制备
价)在高温条件下和氧气反应制备
 ,该反应中被氧化的元素是
,该反应中被氧化的元素是___________ (填元素符号)。当该反应转移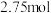 电子时,生成的二氧化硫在标准状况下的体积为
电子时,生成的二氧化硫在标准状况下的体积为___________ L。
(2)实验室中用下列装置测定 被催化氧化为
被催化氧化为 的转化率。(已知
的转化率。(已知 的熔点为
的熔点为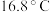 ,假设气体进入装置时均被完全吸收,且忽略空气中
,假设气体进入装置时均被完全吸收,且忽略空气中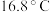 的影响)
的影响) 浓硫酸的仪器名称为
浓硫酸的仪器名称为___________ ,A装置内发生反应的化学方程式为___________ 。
②当停止通入 ,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是
,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是___________ 。
③实验结束后,若装置D增加的质量为 ,装置E中产生白色沉淀的质量为
,装置E中产生白色沉淀的质量为 ,则此条件下二氧化硫的转化率是
,则此条件下二氧化硫的转化率是___________ (用含字母的代数式表示,不用化简)(转化率=发生反应的某种反应物的物质的量/该反应物反应前的总物质的量 )。
)。
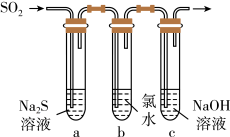
(3)某学习小组设计了如图所示装置来验证二氧化硫的化学性质。___________ 。
②为验证二氧化硫的还原性,反应一段时间后,取试管b中的溶液分成三份,分别进行如下实验。
方案I:向第一份溶液中加入 溶液,有白色沉淀生成
溶液,有白色沉淀生成
方案II:向第二份溶液中加入品红溶液,红色褪去
方案III:向第三份溶液中加入 溶液,产生白色沉淀
溶液,产生白色沉淀
上述方案合理的是___________ (填“I”“II”或“III”);试管b中发生反应的离子方程式为___________ 。
(1)工业上用黄铁矿(主要成分为
 ,其中硫元素为
,其中硫元素为 价)在高温条件下和氧气反应制备
价)在高温条件下和氧气反应制备
 ,该反应中被氧化的元素是
,该反应中被氧化的元素是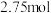 电子时,生成的二氧化硫在标准状况下的体积为
电子时,生成的二氧化硫在标准状况下的体积为(2)实验室中用下列装置测定
 被催化氧化为
被催化氧化为 的转化率。(已知
的转化率。(已知 的熔点为
的熔点为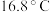 ,假设气体进入装置时均被完全吸收,且忽略空气中
,假设气体进入装置时均被完全吸收,且忽略空气中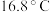 的影响)
的影响)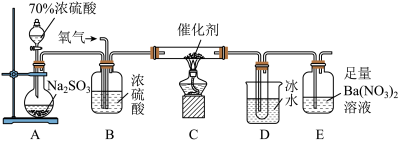
 浓硫酸的仪器名称为
浓硫酸的仪器名称为②当停止通入
 ,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是
,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是③实验结束后,若装置D增加的质量为
 ,装置E中产生白色沉淀的质量为
,装置E中产生白色沉淀的质量为 ,则此条件下二氧化硫的转化率是
,则此条件下二氧化硫的转化率是 )。
)。(3)某学习小组设计了如图所示装置来验证二氧化硫的化学性质。
②为验证二氧化硫的还原性,反应一段时间后,取试管b中的溶液分成三份,分别进行如下实验。
方案I:向第一份溶液中加入
 溶液,有白色沉淀生成
溶液,有白色沉淀生成方案II:向第二份溶液中加入品红溶液,红色褪去
方案III:向第三份溶液中加入
 溶液,产生白色沉淀
溶液,产生白色沉淀上述方案合理的是
您最近半年使用:0次
名校
解题方法
4 . 二氧化硫虽污染环境,但在生活、生产中又有着广泛应用,根据要求回答问题。
Ⅰ.某同学根据铜与浓硫酸反应能生成 ,预测锌与浓硫酸反应生成的产物可能为混合气体(水蒸气除外),设计如下装置进行验证(加热和部分夹持装置略):
,预测锌与浓硫酸反应生成的产物可能为混合气体(水蒸气除外),设计如下装置进行验证(加热和部分夹持装置略):
(1)A中盛放浓硫酸的仪器名称为___________ 。
(2)该同学预测的混合气体的成分可能为___________ 。
(3)C装置所盛试剂可以是___________ (填一种),实验过程中,理论上可观察到E、F装置的实验现象分别为___________ 、___________ 。
Ⅱ.为测定空气中 的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的
的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的
 的酸性高锰酸钾溶液。若管道中空气流量为
的酸性高锰酸钾溶液。若管道中空气流量为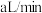 ,经过bmin溶液恰好褪色,假定样品中的
,经过bmin溶液恰好褪色,假定样品中的 可以被溶液充分吸收。
可以被溶液充分吸收。
(4)写出上述反应的离子方程式:___________ 。
(5)该样品中的 含量是
含量是___________ g/L。
Ⅰ.某同学根据铜与浓硫酸反应能生成
 ,预测锌与浓硫酸反应生成的产物可能为混合气体(水蒸气除外),设计如下装置进行验证(加热和部分夹持装置略):
,预测锌与浓硫酸反应生成的产物可能为混合气体(水蒸气除外),设计如下装置进行验证(加热和部分夹持装置略):
(1)A中盛放浓硫酸的仪器名称为
(2)该同学预测的混合气体的成分可能为
(3)C装置所盛试剂可以是
Ⅱ.为测定空气中
 的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的
的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的
 的酸性高锰酸钾溶液。若管道中空气流量为
的酸性高锰酸钾溶液。若管道中空气流量为 ,经过bmin溶液恰好褪色,假定样品中的
,经过bmin溶液恰好褪色,假定样品中的 可以被溶液充分吸收。
可以被溶液充分吸收。(4)写出上述反应的离子方程式:
(5)该样品中的
 含量是
含量是
您最近半年使用:0次
2024-04-23更新
|
130次组卷
|
2卷引用:四川省攀枝花市第三高级中学2023-2024学年高一下学期第一次月考化学试题
名校
解题方法
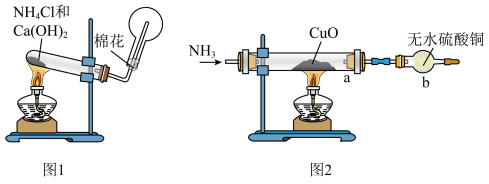
5 . 人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图1装置制备氨气,图2装置探究其相关性质。
(1)图1装置中生成 的化学方程式为
的化学方程式为_____ 。
(2)检验圆底烧瓶中已收集满氨气的方法是_____ 。
Ⅱ.探究氨气与氧化铜的反应(如图2)验证氨气的性质及部分反应产物:
(3)无水硫酸铜的作用是_____ ;有同学认为需要在无水硫酸铜的后面再接一个装有 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是_____ 。
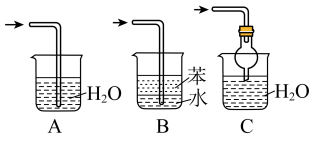
(4)该实验缺少尾气吸收装置。如图中能用来吸收尾气的装置是_____ (填字母)。 粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为_____ ,证明氨气具有_____ (填“氧化”或“还原”)性。
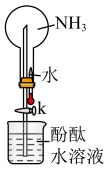
(6)①如图是进行氨气喷泉实验的装置,氨气使烧杯中溶液由无色变为红色,其原因是(用方程式表示)_____ 。
②在上图的烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是_____ 。 和
和 B.
B. 和氢氧化钠溶液 C.
和氢氧化钠溶液 C. 和饱和食盐水 D.
和饱和食盐水 D. 和烧碱溶液
和烧碱溶液
(1)图1装置中生成
 的化学方程式为
的化学方程式为(2)检验圆底烧瓶中已收集满氨气的方法是
Ⅱ.探究氨气与氧化铜的反应(如图2)验证氨气的性质及部分反应产物:
(3)无水硫酸铜的作用是
 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是(4)该实验缺少尾气吸收装置。如图中能用来吸收尾气的装置是
 粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为(6)①如图是进行氨气喷泉实验的装置,氨气使烧杯中溶液由无色变为红色,其原因是(用方程式表示)
②在上图的烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是
 和
和 B.
B. 和氢氧化钠溶液 C.
和氢氧化钠溶液 C. 和饱和食盐水 D.
和饱和食盐水 D. 和烧碱溶液
和烧碱溶液
您最近半年使用:0次
6 . 某研究性学习小组学生根据氧化还原反应规律,探究 、
、 与
与 反应的情况,提出假设并进行相关实验。
反应的情况,提出假设并进行相关实验。
Ⅰ.从理论上分析 和
和 都既有氧化性又有还原性,于是提出如下假设:
都既有氧化性又有还原性,于是提出如下假设:
假设1: 氧化
氧化 ;
;
假设2: 氧化
氧化 。
。
(1)甲同学设计如图装置进行实验:___________ 。
②待试管B中充满红棕色气体,关闭旋塞a和b;取下试管B,向其中加入适量 粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
结论:甲同学认为假设2正确。
(2)乙同学认为甲同学设计的实验存在缺陷,为达到实验目的,在A、B之间应增加一个装置,该装置的作用是___________ 。乙同学用改进后的装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;带火星的木条未复燃,得出结论:假设Ⅰ正确。则 和
和 反应的化学方程式是
反应的化学方程式是___________ 。
Ⅱ.该研究性学习小组同学还认为易与 发生反应,应该更易被氧化。查阅资料:
发生反应,应该更易被氧化。查阅资料: ;
;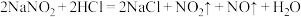 ;酸性条件下,能与
;酸性条件下,能与 反应生成
反应生成 和
和 。
。
(3)丙同学用下图所示装置(部分夹持装置略)探究 与
与 的反应。
的反应。 ,目的是
,目的是___________ 。
②B中观察到的主要现象的是___________ (填字母编号)。
a.铜片逐渐溶解,溶液变为蓝色
b.有红棕色气泡产生
c.有无色气泡产生
③C、E中所盛装的试剂不能是___________ (填字母编号)。
a.无水硫酸铜 b.无水氯化钙 c.碱石灰 d.生石灰
④充分反应后,检验D装置中产物的方法是:取D装置中产物少许,___________ ,则产物是 。
。
 、
、 与
与 反应的情况,提出假设并进行相关实验。
反应的情况,提出假设并进行相关实验。Ⅰ.从理论上分析
 和
和 都既有氧化性又有还原性,于是提出如下假设:
都既有氧化性又有还原性,于是提出如下假设:假设1:
 氧化
氧化 ;
;假设2:
 氧化
氧化 。
。(1)甲同学设计如图装置进行实验:

②待试管B中充满红棕色气体,关闭旋塞a和b;取下试管B,向其中加入适量
 粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。结论:甲同学认为假设2正确。
(2)乙同学认为甲同学设计的实验存在缺陷,为达到实验目的,在A、B之间应增加一个装置,该装置的作用是
 和
和 反应的化学方程式是
反应的化学方程式是Ⅱ.该研究性学习小组同学还认为易与
 发生反应,应该更易被氧化。查阅资料:
发生反应,应该更易被氧化。查阅资料: ;
;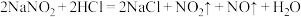 ;酸性条件下,能与
;酸性条件下,能与 反应生成
反应生成 和
和 。
。(3)丙同学用下图所示装置(部分夹持装置略)探究
 与
与 的反应。
的反应。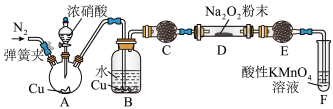
 ,目的是
,目的是②B中观察到的主要现象的是
a.铜片逐渐溶解,溶液变为蓝色
b.有红棕色气泡产生
c.有无色气泡产生
③C、E中所盛装的试剂不能是
a.无水硫酸铜 b.无水氯化钙 c.碱石灰 d.生石灰
④充分反应后,检验D装置中产物的方法是:取D装置中产物少许,
 。
。
您最近半年使用:0次
2024-04-08更新
|
553次组卷
|
5卷引用:四川省自贡市蜀光中学2023-2024学年高一下学期4月月考化学试题
7 . 已知反应: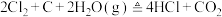 。某实验小组用高锰酸钾与浓盐酸反应制取氯气,并验证已知反应产物中的
。某实验小组用高锰酸钾与浓盐酸反应制取氯气,并验证已知反应产物中的 ,装置连接如下:
,装置连接如下:
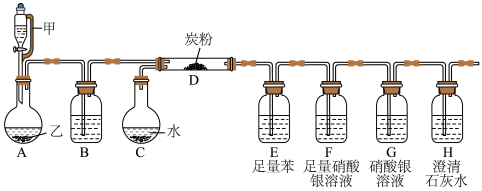
已知:氯气易溶于苯中。
回答下列问题:
(1)装置
 中仪器甲的名称是
中仪器甲的名称是(2)装置
 中的试剂是
中的试剂是(3)设计装置
 的目的是
的目的是 的作用是
的作用是(4)判断产物中含有
 的实验现象是
的实验现象是(5)用双线桥表示该反应电子转移的方向和数目:
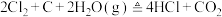
您最近半年使用:0次
8 . 利用图示装置进行实验,经过一段时间后,装置Ⅱ中实验现象正确的是
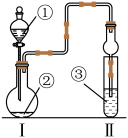
| 选项 | ① | ② | ③ | 装置Ⅱ中实验现象 |
| A | 浓盐酸 | MnO2 | 紫色石蕊溶液 | 石蕊溶液先变红,后褪色 |
| B | 稀硫酸 | 碳酸钠 | 饱和碳酸钠溶液 | 产生白色沉淀 |
| C | 浓氨水 | 生石灰 | 硫酸铝溶液 | 先产生白色沉淀,后沉淀溶解 |
| D | 70%硫酸 | Na2SO3 | Na2S溶液 | 无明显现象 |

| A.A | B.B | C.C | D.D |
您最近半年使用:0次
9 . 用如图所示实验装置(夹持仪器已省略)探究铜丝与过量浓硫酸的反应。下列实验不合理的是
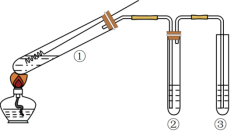
A.移动装置①中铜丝可控制 的量 的量 |
B.装置②中选用品红溶液验证 的生成 的生成 |
C.装置③中选用 溶液吸收多余的 溶液吸收多余的 |
D.向装置①反应后溶液中直接加水,确认有 生成 生成 |
您最近半年使用:0次
10 . 数字化实验将传感器、数据采集器和计算机相连,采集实验过程中各种物理量变化的数据并记录和呈现,如图采集的用强光照射盛有氯水的密闭广口瓶,并用传感器测定广口瓶中数据,得到如图曲线。下列说法错误的是
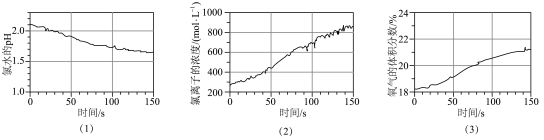

| A.图(1)说明强光照射下,氯水中H+浓度增大 |
| B.结合上图可知,氯水应保存在棕色试剂瓶中,并置于冷暗处 |
C.结合上图可知,若将氯水长时间强光照射,产物为盐酸和 |
| D.结合上图可知,经强光照射一段时间后,氯水的酸性和漂白性均增强 |
您最近半年使用:0次
2024-03-07更新
|
46次组卷
|
2卷引用:四川省成都市锦江区嘉祥外国语学校2023-2024学年高一上学期半期考试(期中)化学试题



