解题方法
1 . 某化学自主实验小组利用如图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)。(夹持、固定装置均略去)。
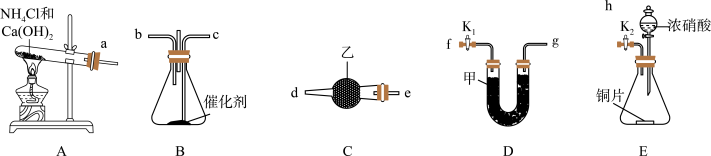
(1)A装置发生的化学反应方程式为______ 。
(2)如按装置由左向右,连接上述装置的正确顺序是_____ 。
a→f→g→_______→_______→_______→_______→h(填各接口字母)。
(3)装置B中NO2能够在催化剂作用下被NH3还原,生成氮气和水,写出发生反应的化学方程式:_____ 。
(4)甲是_____ (填药品名称),作用是______ 。
(5)此实验装置存在一个明显的缺陷是_____ 。
(6)若装置E反应过程中共产生标准状况下气体22.4L(不考虑NO2与N2O4的转化)则消耗的浓硝酸的物质的量为_____ 。

(1)A装置发生的化学反应方程式为
(2)如按装置由左向右,连接上述装置的正确顺序是
a→f→g→_______→_______→_______→_______→h(填各接口字母)。
(3)装置B中NO2能够在催化剂作用下被NH3还原,生成氮气和水,写出发生反应的化学方程式:
(4)甲是
(5)此实验装置存在一个明显的缺陷是
(6)若装置E反应过程中共产生标准状况下气体22.4L(不考虑NO2与N2O4的转化)则消耗的浓硝酸的物质的量为
您最近一年使用:0次
2 . 氯气、氯水、漂白粉都是常见的含氯消毒剂。回答下列有关问题。
Ⅰ.实验室中制备
方法一: 与浓盐酸反应
与浓盐酸反应
方法二:漂白粉与浓盐酸反应,原理为
(1)方法一的化学反应方程式为____________ ,发生装置为______ (填编号)。

(2)当制得相同质量 时,方法一与方法二转移的电子数之比为
时,方法一与方法二转移的电子数之比为______ 。
Ⅱ.某实验小组利用如图装置制备氯水,并探究其部分性质。
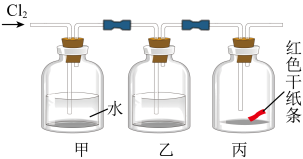
(3)若实验过程中观察到红色干纸条未褪色,则乙中的试剂可能是______ (填编号)。
A.浓 B.饱和NaCl溶液 C.NaOH溶液
B.饱和NaCl溶液 C.NaOH溶液
(4)将装置甲中所得氯水滴入含有酚酞的NaOH稀溶液中,观察到溶液红色褪去。有同学提出如下两种原因:
【原因1】氯水中含有的 中和掉NaOH而使溶液褪色
中和掉NaOH而使溶液褪色
【原因2】氯水中含有的______ 具有漂白性而使溶液褪色
请设计实验验证:褪色的原因确实存在“原因2”。向褪色后的溶液中滴加______ (填试剂与现象)。
Ⅰ.实验室中制备

方法一:
 与浓盐酸反应
与浓盐酸反应方法二:漂白粉与浓盐酸反应,原理为

(1)方法一的化学反应方程式为

(2)当制得相同质量
 时,方法一与方法二转移的电子数之比为
时,方法一与方法二转移的电子数之比为Ⅱ.某实验小组利用如图装置制备氯水,并探究其部分性质。

(3)若实验过程中观察到红色干纸条未褪色,则乙中的试剂可能是
A.浓
 B.饱和NaCl溶液 C.NaOH溶液
B.饱和NaCl溶液 C.NaOH溶液(4)将装置甲中所得氯水滴入含有酚酞的NaOH稀溶液中,观察到溶液红色褪去。有同学提出如下两种原因:
【原因1】氯水中含有的
 中和掉NaOH而使溶液褪色
中和掉NaOH而使溶液褪色【原因2】氯水中含有的
请设计实验验证:褪色的原因确实存在“原因2”。向褪色后的溶液中滴加
您最近一年使用:0次
名校
解题方法
3 . 用下列仪器或装置进行相应实验,部分现象描述和解释不正确的是
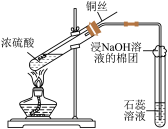 | 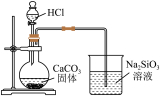 |  | 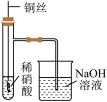 |
| ① | ② | ③ | ④ |
| A.①中石蕊溶液变为红色后不褪色 |
| B.②的烧杯中产生白色沉淀,说明非金属性Cl>C>Si |
| C.③中产生红棕色气体,不能说明木炭与浓硝酸发生了反应 |
| D.④的试管内先出现红棕色气体,后变无色 |
您最近一年使用:0次
2023-04-21更新
|
405次组卷
|
4卷引用:四川省宜宾市第四中学校2022-2023学年高一下学期5月期中考试化学试题
4 . 某化学兴趣小组利用如图装置制备氨气并探究相关性质。
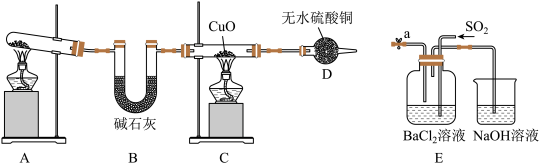
(1)A装置中生成 的化学方程式为
的化学方程式为_______ 。
(2)D装置后接尾气吸收装置,下列能用来吸收尾气的装置是_______ (填装置序号)。
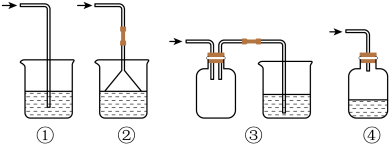
(3)若将D与a相连,在E中产生白色沉淀,其沉淀的化学式为_______ 。设计实验验证E装置中含有
_______ 。
(4)若向a处分别通入大量_______ (填下列气体编号),在E中不会产生白色沉淀。
A. B.
B.  C.
C.  D.
D. 
(5)实验发现C中粉末完全变红,D中无水硫酸铜变蓝,还产生一种单质气体。
①若红色固体为单质,实验后将C中固体与浓硫酸混合加热,其化学方程式为_______ ;若充分反应后红色固体有剩余,再加入下列的_______ 试剂,固体又可以继续溶解。
A.稀 B.
B. 溶液 C.
溶液 C. 溶液 D.
溶液 D. 溶液
溶液
②已知 也为红色固体,反应前C中CuO质量为8 g,反应后C中红色固体质量为6.8 g,则C中发生的总反应方程式为
也为红色固体,反应前C中CuO质量为8 g,反应后C中红色固体质量为6.8 g,则C中发生的总反应方程式为_______ 。

(1)A装置中生成
 的化学方程式为
的化学方程式为(2)D装置后接尾气吸收装置,下列能用来吸收尾气的装置是

(3)若将D与a相连,在E中产生白色沉淀,其沉淀的化学式为

(4)若向a处分别通入大量
A.
 B.
B.  C.
C.  D.
D. 
(5)实验发现C中粉末完全变红,D中无水硫酸铜变蓝,还产生一种单质气体。
①若红色固体为单质,实验后将C中固体与浓硫酸混合加热,其化学方程式为
A.稀
 B.
B. 溶液 C.
溶液 C. 溶液 D.
溶液 D. 溶液
溶液②已知
 也为红色固体,反应前C中CuO质量为8 g,反应后C中红色固体质量为6.8 g,则C中发生的总反应方程式为
也为红色固体,反应前C中CuO质量为8 g,反应后C中红色固体质量为6.8 g,则C中发生的总反应方程式为
您最近一年使用:0次
名校
解题方法
5 . 某同学按如图所示实验装置探究铜与浓硫酸的反应,记录实验现象如表。

下列说法不正确的是

| 试管 | 实验现象 |
| ① | 白雾、白色固体产生 |
| ② | 大量白色沉淀 |
| ③ | 少量白色沉淀 |
| ④ | 品红溶液褪色 |
| A.①中玻璃管有平衡气压的作用 |
| B.②③中的白色沉淀成分相同 |
| C.为了确定①中白色固体是否为硫酸铜,可将试管内的物质缓慢注入水中,振荡观察 |
D.实验时若先往装置内通入足量 ,再加热试管①,实验现象不变 ,再加热试管①,实验现象不变 |
您最近一年使用:0次
2023-04-21更新
|
422次组卷
|
2卷引用:四川省成都市第七中学2022-2023学年高一下学期期中考试化学试题
名校
解题方法
6 . 用如图所示装置制取 并验证
并验证 的某些性质。回答下列问题:
的某些性质。回答下列问题:
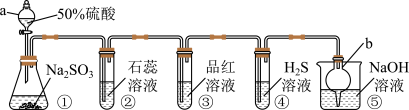
(1)仪器a的名称是___________ ,仪器b的作用是___________ ,装置⑤中NaOH溶液的作用是___________ 。
(2)装置②中的实验现象是___________ 。反应结束后,对装置③的试管加热,可观察到的现象是___________ 。
(3)装置④中发生反应的化学方程式为___________ ,在该反应中 作
作___________ 剂。
(4)将制得的 依次通入装置②、③、④,其中实验现象与通入
依次通入装置②、③、④,其中实验现象与通入 不同的是装置
不同的是装置___________ 。
 并验证
并验证 的某些性质。回答下列问题:
的某些性质。回答下列问题:
(1)仪器a的名称是
(2)装置②中的实验现象是
(3)装置④中发生反应的化学方程式为
 作
作(4)将制得的
 依次通入装置②、③、④,其中实验现象与通入
依次通入装置②、③、④,其中实验现象与通入 不同的是装置
不同的是装置
您最近一年使用:0次
名校
解题方法
7 . 阅读下面一段材料并回答问题。
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 。
(2)制备 需要在
需要在_______  填“酸性”、“碱性”或“中性”
填“酸性”、“碱性”或“中性” 环境中进行。
环境中进行。
(3)下列关于 的说法中,不正确的是
的说法中,不正确的是_______ 。
 是强氧化性的盐
是强氧化性的盐
 固体保存需要防潮
固体保存需要防潮
 其消毒和净化水的原理相同
其消毒和净化水的原理相同
 其净水优点有:作用快、安全性好、无异味
其净水优点有:作用快、安全性好、无异味
(4)将 与水反应的化学方程式补充完整:
与水反应的化学方程式补充完整:_______
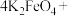 _______
_______ _______
_______ 胶体
胶体 _______
_______ _______
_______
该反应消耗1个 时,转移的电子数为
时,转移的电子数为_______ 个
(5)消毒净化 水,至少需要
水,至少需要 的质量为
的质量为_______  。
。
| 高铁酸钾使用说明书 【化学式】K2FeO4 【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气K2FeO4通过强烈 的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附 性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用 【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1L水投放5 mg K2FeO4即可达到卫生标准 ... ... |
 中铁元素的化合价为
中铁元素的化合价为(2)制备
 需要在
需要在 填“酸性”、“碱性”或“中性”
填“酸性”、“碱性”或“中性” 环境中进行。
环境中进行。(3)下列关于
 的说法中,不正确的是
的说法中,不正确的是 是强氧化性的盐
是强氧化性的盐 固体保存需要防潮
固体保存需要防潮 其消毒和净化水的原理相同
其消毒和净化水的原理相同 其净水优点有:作用快、安全性好、无异味
其净水优点有:作用快、安全性好、无异味(4)将
 与水反应的化学方程式补充完整:
与水反应的化学方程式补充完整: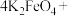 _______
_______ _______
_______ 胶体
胶体 _______
_______ _______
_______
该反应消耗1个
 时,转移的电子数为
时,转移的电子数为(5)消毒净化
 水,至少需要
水,至少需要 的质量为
的质量为 。
。
您最近一年使用:0次
解题方法
8 . 甲同学分别对铜与硝酸的反应进行探究,请你参与并完成有关问题的解答。
甲组同学采用如图所示装置验证铜与硝酸的反应。已知仪器A中盛有足量的一定浓度的硝酸溶液,试管B中盛有4.8g铜。
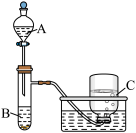
(1)请写出铜与稀硝酸反应的化学方程式:___________ 。
(2)在铜与硝酸的反应中,硝酸所表现出的化学性质除有氧化性还有___________ 。
(3)仪器C中收集的气体时的主要是___________ (填化学式)。待气体收集满后将其集气瓶正放在桌面上,拿下玻璃片,可以观察到的现象是___________ 反应方程为___________ 。
(4)待试管B中的铜反应完全后,如果向B中液体里加入足量氢氧化钠溶液,可生成沉淀的质量为___________ g。
甲组同学采用如图所示装置验证铜与硝酸的反应。已知仪器A中盛有足量的一定浓度的硝酸溶液,试管B中盛有4.8g铜。

(1)请写出铜与稀硝酸反应的化学方程式:
(2)在铜与硝酸的反应中,硝酸所表现出的化学性质除有氧化性还有
(3)仪器C中收集的气体时的主要是
(4)待试管B中的铜反应完全后,如果向B中液体里加入足量氢氧化钠溶液,可生成沉淀的质量为
您最近一年使用:0次
名校
解题方法
9 . 某研究小组探究电解FeCl2溶液的电极反应产物
(1)配制1 mol⋅L FeCl2溶液,测得
FeCl2溶液,测得 ,从化合价角度分析,
,从化合价角度分析, 具有的性质
具有的性质_______ 。
(2)该小组同学预测电解FeCl2溶液两极的现象:阳极有黄绿色气体产生,阴极有无色气体产生。该小组同学用如图装置电解1 mol⋅L FeCl2溶液:
FeCl2溶液:
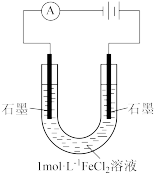
①取少量银灰色固体洗涤后,加稀H2SO4有气泡产生,再向溶液中加入_______ (试剂和现象),证明该固体为Fe。
②该小组同学分析红褐色固体产生的原因,甲同学认为2Cl--2e-=Cl2↑,Cl2可氧化Fe2+最终生成Fe(OH)3,乙同学认为_______ 。
(3)该小组同学进一步探究电解1 mol⋅L
 溶液电极产物的影响因素。
溶液电极产物的影响因素。
①写出实验III中电解FeCl2溶液的离子反应方程式_______ 。
②对比实验I、II、III可以得出结论:阳极:Fe2+放电时,酸性较强主要生成Fe3+;酸性较弱主要生成Fe(OH)3;阴极:_______ 。
③对比实验I、IV、V可以得出结论:增大电压,不仅可以改变离子的放电能力,也可以_______ 。
(4)综合分析上述实验,电解过程中电极反应的产物与_______ 有关。
(1)配制1 mol⋅L
 FeCl2溶液,测得
FeCl2溶液,测得 ,从化合价角度分析,
,从化合价角度分析, 具有的性质
具有的性质(2)该小组同学预测电解FeCl2溶液两极的现象:阳极有黄绿色气体产生,阴极有无色气体产生。该小组同学用如图装置电解1 mol⋅L
 FeCl2溶液:
FeCl2溶液:
| 实验 | 条件 | 操作及现象 | ||
| 电压 | pH | 阳极 | 阴极 | |
| I | 1.5v | 4.91 | 无气泡产生,溶液逐渐变浑浊,5分钟后电极表面析出红褐色固体 | 无气泡产生,4分钟后电极表面有银灰色金属状固体附着 |
②该小组同学分析红褐色固体产生的原因,甲同学认为2Cl--2e-=Cl2↑,Cl2可氧化Fe2+最终生成Fe(OH)3,乙同学认为
(3)该小组同学进一步探究电解1 mol⋅L

 溶液电极产物的影响因素。
溶液电极产物的影响因素。| 实验 | 条件 | 操作及现象 | ||
| 电压 | pH | 阳极 | 阴极 | |
| II | 1.5v | 2.38 | 无气泡产生,溶液出现少量浑浊,滴加KSCN溶液变红色 | 无气泡产生,电极表面有银灰色金属状固体附着 |
| III | 1.5v | 1.00 | 无气泡产生,溶液无浑浊现象,滴加KSCN溶液变红色 | 有气泡产生,无固体附着 |
| IV | 3.0v | 4.91 | 无气泡产生,溶液逐渐变浑浊,3分钟后电极表面有红褐色固体产生 | 极少量气泡产生,1分钟出现镀层金属 |
| V | 6.0v | 4.91 | 有气泡产生,遇湿润的淀粉碘化钾试纸变蓝。溶液逐渐变浑浊 | 大量气泡产生,迅速出现镀层金属 |
②对比实验I、II、III可以得出结论:阳极:Fe2+放电时,酸性较强主要生成Fe3+;酸性较弱主要生成Fe(OH)3;阴极:
③对比实验I、IV、V可以得出结论:增大电压,不仅可以改变离子的放电能力,也可以
(4)综合分析上述实验,电解过程中电极反应的产物与
您最近一年使用:0次
10 . 进行下列封管实验都产生明显现象,其中不涉及化学反应的是
A. | B. | C. | D.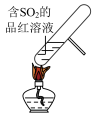 |
您最近一年使用:0次
2023-04-05更新
|
401次组卷
|
3卷引用:四川省成都市石室中学2023届高三下学期高考适应性考试(二)理科综合化学试题



