名校
1 . 某化学兴趣小组在实验室用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取SO2并完成相关性质探究(不考虑水蒸气)。(已知:C+2H2SO4(浓) CO2+2SO2↑+2H2O)
CO2+2SO2↑+2H2O)
(1)有同学认为制得的SO2中可能混有杂质,其化学式为_________ 。
为验证气体成分,兴趣小组同学设计了如图所示装置进行了实验探究。_________ ;装置C中品红溶液的作用是_________ 。
(3)装置H的作用为_________ 。
兴趣小组设计如图装置验证二氧化硫的化学性质。___________ ;
为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成。
(5)上述方案中合理的是___________ (填Ⅰ、Ⅱ或Ⅲ);试管b中发生反应的离子方程式为___________ 。
(6)如果用硫酸溶液和 固体反应制取
固体反应制取 装置如图所示。其中
装置如图所示。其中 导管的作用是
导管的作用是________ 。 含量(假设空气中无其他还原性气体)。
含量(假设空气中无其他还原性气体)。 (标准状况下),最终所得固体质量为
(标准状况下),最终所得固体质量为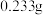 ,通过计算确定该空气中二氧化硫的含量是
,通过计算确定该空气中二氧化硫的含量是________ 。(结果精确到 )
)
 CO2+2SO2↑+2H2O)
CO2+2SO2↑+2H2O)(1)有同学认为制得的SO2中可能混有杂质,其化学式为
为验证气体成分,兴趣小组同学设计了如图所示装置进行了实验探究。
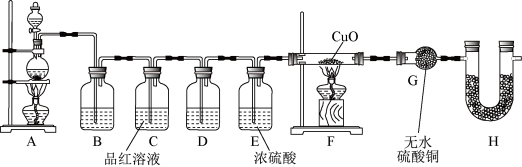
(3)装置H的作用为
兴趣小组设计如图装置验证二氧化硫的化学性质。

为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成。
(5)上述方案中合理的是
(6)如果用硫酸溶液和
 固体反应制取
固体反应制取 装置如图所示。其中
装置如图所示。其中 导管的作用是
导管的作用是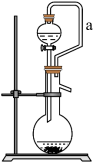
 含量(假设空气中无其他还原性气体)。
含量(假设空气中无其他还原性气体)。
 (标准状况下),最终所得固体质量为
(标准状况下),最终所得固体质量为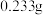 ,通过计算确定该空气中二氧化硫的含量是
,通过计算确定该空气中二氧化硫的含量是 )
)
您最近半年使用:0次
7日内更新
|
147次组卷
|
2卷引用:宁夏石嘴山市平罗中学2023-2024学年高一下学期4月月考化学试题
名校
解题方法
2 . 某小组同学用如图所示装置制取氨气并验证氨气的性质。请回答:
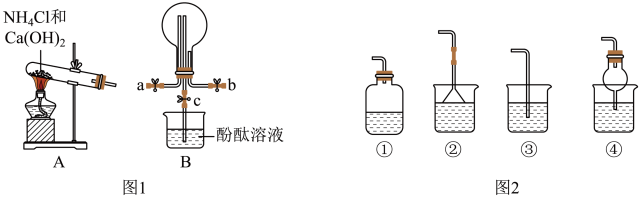
(1)实验室制取氨气的化学方程式是_______ 。
(2)用图1装置B收集氨气时,应选择氨气的进气口是_______ (选填“a”或“b”)。
(3)打开图1装置B中的止水夹c,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是_______ 。
(4)为防止环境污染,图2装置(盛放的液体均为水)可用于吸收多余氨气的是_______ (填序号、下同)。
(5)生石灰与水反应生成 并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用如图的气体发生装置是
并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用如图的气体发生装置是_______ 。
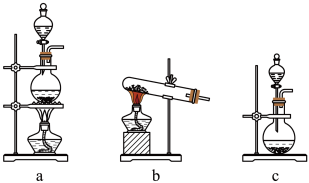

(1)实验室制取氨气的化学方程式是
(2)用图1装置B收集氨气时,应选择氨气的进气口是
(3)打开图1装置B中的止水夹c,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是
(4)为防止环境污染,图2装置(盛放的液体均为水)可用于吸收多余氨气的是
(5)生石灰与水反应生成
 并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用如图的气体发生装置是
并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用如图的气体发生装置是
您最近半年使用:0次
名校
解题方法
3 . 为了探究元素周期律,设计实验验证卤素单质氧化性的相对强弱,实验如下:
资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
(1)a中反应的离子方程式是___________ 。
(2)实验I中b可以得出的氧化性强弱是___________ 。
(3)①甲同学认为:实验Ⅱ观察到___________ 现象,得出氧化性Br2>I2。
②乙同学对上述实验进行反思,认为实验II不能充分证明氧化性Br2>I2,他补做了实验Ⅲ.
补做实验Ⅲ的目的是___________ 。
综合实验I和Ⅲ,得出氧化性Cl2>Br2>I2.由此实验得出的结论:同主族元素从上到下,原子的得电子能力逐渐减弱
资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
| 实验I | 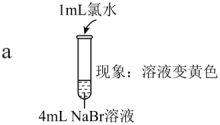 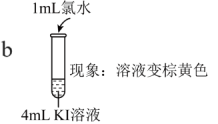 |
| 实验II | 取a中的黄色溶液少许,加入KI溶液,再加入淀粉溶液。 |
(1)a中反应的离子方程式是
(2)实验I中b可以得出的氧化性强弱是
(3)①甲同学认为:实验Ⅱ观察到
②乙同学对上述实验进行反思,认为实验II不能充分证明氧化性Br2>I2,他补做了实验Ⅲ.
| 实验III | 另取a中黄色溶液少许,加入足量NaBr固体,振荡,然后加入KI溶液和淀粉溶液。 |
综合实验I和Ⅲ,得出氧化性Cl2>Br2>I2.由此实验得出的结论:同主族元素从上到下,原子的得电子能力逐渐减弱
您最近半年使用:0次
2024-02-13更新
|
55次组卷
|
2卷引用:宁夏回族自治区石嘴山市第三中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
4 . 下列是某兴趣小组根据课本实验设计的一个能说明Na2CO3与NaHCO3热稳定性的套管实验。请观察如图实验装置并分析实验原理,判断下列说法错误的是
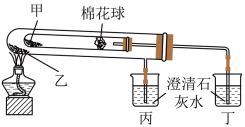
| A.Na2CO3热稳定性大于NaHCO3 |
| B.甲为Na2CO3,乙为NaHCO3 |
| C.要证明物质受热能产生水,可在两支试管内塞上沾有无水硫酸铜粉末的棉花球 |
| D.整个实验过程中可以看到丙烧杯的澄清石灰水不变浑浊 |
您最近半年使用:0次
2024-01-16更新
|
93次组卷
|
4卷引用:宁夏银川市永宁县永宁中学2023-2024学年高一上学期第一次月考化学试卷
名校
解题方法
5 . 钠、碳及它们的化合物在生产、生活中有着重要的用途。
Ⅰ.某课外实验小组从煤油中取出一块钠,用滤纸吸干其表面的煤油,用刀切下数块,分别进行实验研究。
(1)钠块切面处迅速变暗,反应的化学方程式为_______ 。
(2)将一小块钠放入坩埚中加热,反应的化学方程式为_______ 。
(3)将加热过的一小块钠放入盛有氯气的集气瓶中,反应的化学方程式为_______ 。
(4)将一小块Na投入到盛有适量水的烧杯中,反应的化学方程式为_______ 。反应放出大量热,依据的现象是_______ 。
(5)将一小块Na投入到盛有适量硫酸铜溶液的烧杯中,观察到溶液中出现蓝色沉淀,写出产生蓝色沉淀的化学方程式为_______ 。
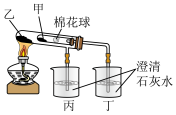
Ⅱ.利用图示装置比较碳酸钠和碳酸氢钠的热稳定性
(6)则物质甲的化学式为_______ ,若要除去碳酸钠固体中的碳酸氢钠,发生反应的化学方程式为_______ 。
Ⅲ.在呼吸面具和潜水艇中,可用过氧化钠作供氧剂。采用下图所示实验装置进行实验,证明过氧化钠可用做供氧剂。
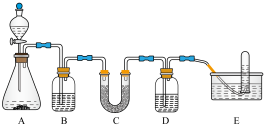
已知:A中加入碳酸钙和稀盐酸,B中加入饱和NaHCO3溶液;C中加入Na2O2,D中加入NaOH溶液,E中加入水。回答下列问题:
(7)B的作用是除去CO2中混有的HCl。请写出NaHCO3溶液与HCl反应的化学方程式:_______ 。
(8)C中Na2O2与CO2反应的化学方程式为_______ 。
(9)D的作用为_______ ,E中收集到的气体成分为_______ 。
Ⅰ.某课外实验小组从煤油中取出一块钠,用滤纸吸干其表面的煤油,用刀切下数块,分别进行实验研究。
(1)钠块切面处迅速变暗,反应的化学方程式为
(2)将一小块钠放入坩埚中加热,反应的化学方程式为
(3)将加热过的一小块钠放入盛有氯气的集气瓶中,反应的化学方程式为
(4)将一小块Na投入到盛有适量水的烧杯中,反应的化学方程式为
(5)将一小块Na投入到盛有适量硫酸铜溶液的烧杯中,观察到溶液中出现蓝色沉淀,写出产生蓝色沉淀的化学方程式为
Ⅱ.利用图示装置比较碳酸钠和碳酸氢钠的热稳定性
(6)则物质甲的化学式为

Ⅲ.在呼吸面具和潜水艇中,可用过氧化钠作供氧剂。采用下图所示实验装置进行实验,证明过氧化钠可用做供氧剂。

已知:A中加入碳酸钙和稀盐酸,B中加入饱和NaHCO3溶液;C中加入Na2O2,D中加入NaOH溶液,E中加入水。回答下列问题:
(7)B的作用是除去CO2中混有的HCl。请写出NaHCO3溶液与HCl反应的化学方程式:
(8)C中Na2O2与CO2反应的化学方程式为
(9)D的作用为
您最近半年使用:0次
6 . 为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验。
(1)高温下,让铁粉与水蒸气反应,见题图。试管中发生的化学方程式是________________ ,该反应中氧化剂是________________ 。

(2)如图:

①往A溶液中滴入几滴KSCN溶液,溶液的颜色________________ 。
②写出上述过程中A→B的离子方程式________________ 。
③描述C暴露在空气中的颜色变化________________ 。写出相关的化学方程式________________ 。
④写出B加入氯水的离子方程式________________ 。
(1)高温下,让铁粉与水蒸气反应,见题图。试管中发生的化学方程式是

(2)如图:

①往A溶液中滴入几滴KSCN溶液,溶液的颜色
②写出上述过程中A→B的离子方程式
③描述C暴露在空气中的颜色变化
④写出B加入氯水的离子方程式
您最近半年使用:0次
2024-01-09更新
|
193次组卷
|
2卷引用:宁夏吴忠市青铜峡市2023-2024学年高一上学期12月月考化学试题
名校
解题方法
7 . Ⅰ.实验室用如图装置制备并收集干燥、纯净的Cl2.已知碳酸的酸性比次氯酸的强,回答下列问题:
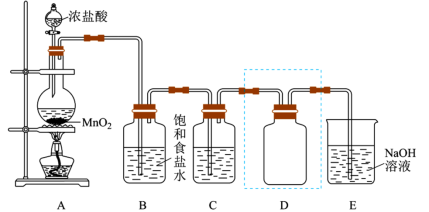
(1)装置A中,装二氧化锰的玻璃仪器的名称是_______ ,发生反应的化学方程式是_______
(2)装置B的作用是_______ 。
(3)装置C中盛放的物质是_______ 。
(4)装置D用于收集Cl2,装置D中进气方向为_______ (填“甲”或“乙”),若在D中放入干燥的布条,布条_______ (填“褪色”或“不褪色”)。
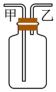
(5)装置E用于吸收尾气,E中发生反应的离子方程式是_______ 。
(6)可用Cl2和冷的石灰乳反应制备漂白粉,写出化学方程式_______ 。
Ⅱ.游泳池中的水需要经常杀菌、消毒。某化学兴趣小组对游泳池中使用的消毒剂进行了研究性学习。
(7)氯气是游泳池中水体消毒杀菌的常用消毒剂之一,请用化学方程式表示它能消毒杀菌的原因_______ 。
(8)游泳池也可使用漂白液(主要成分是次氯酸钠)来进行消毒杀菌。与氯气相比较,请写出使用漂白液的一个优点:_______ 。
(9)用于游泳池消毒杀菌的消毒剂还有很多。下列物质中,可以用于游泳池杀菌消毒的是_______ (填字母)。
A.二氧化硫 B.臭氧 C.高锰酸钾

(1)装置A中,装二氧化锰的玻璃仪器的名称是
(2)装置B的作用是
(3)装置C中盛放的物质是
(4)装置D用于收集Cl2,装置D中进气方向为

(5)装置E用于吸收尾气,E中发生反应的离子方程式是
(6)可用Cl2和冷的石灰乳反应制备漂白粉,写出化学方程式
Ⅱ.游泳池中的水需要经常杀菌、消毒。某化学兴趣小组对游泳池中使用的消毒剂进行了研究性学习。
(7)氯气是游泳池中水体消毒杀菌的常用消毒剂之一,请用化学方程式表示它能消毒杀菌的原因
(8)游泳池也可使用漂白液(主要成分是次氯酸钠)来进行消毒杀菌。与氯气相比较,请写出使用漂白液的一个优点:
(9)用于游泳池消毒杀菌的消毒剂还有很多。下列物质中,可以用于游泳池杀菌消毒的是
A.二氧化硫 B.臭氧 C.高锰酸钾
您最近半年使用:0次
名校
8 . 二氧化氯(ClO2)具有强氧化性,是优良的饮用水消毒剂。ClO2常温下为黄绿色气体,熔点-59℃,沸点11℃,极易溶于水且不与水反应,浓的ClO2受热时易爆炸。我国广泛使用的方法是用干燥的Cl2与NaClO2固体反应制取ClO2,实验室模拟制备ClO2装置如图所示:
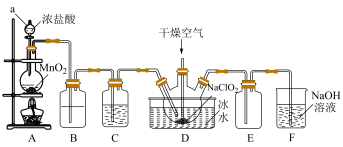
(1)仪器a的名称是:___________ ,装置A中反应的离子方程式为:___________ 。
(2)装置B中盛装的试剂是___________ ,装置C中试剂的作用是:___________ 。
(3)为防止ClO2制备装置发生爆炸,实验中采取的措施:①将装置置于冰水浴中降温,②___________ 。
(4)装置E为ClO2的收集装置,应将其置于___________ 水浴中(填“热”或“冰”)。
(5)装置F为氯气的尾气吸收装置,小组同学用胶头滴管将新制的饱和氯水慢慢滴入含有酚酞的NaOH溶液中,当滴到一定量时,红色突然褪去,小组同学对褪色原因提出假设:
假设1:___________ 。
假设2:可能是氯水中存在HClO具有强氧化性,漂白褪色。
该小组同学设计实验证明假设1是否成立。实验方案为:取少许褪色后的溶液于试管中,滴加足量的NaOH溶液,若___________ (填“实验现象”),则假设1成立。

(1)仪器a的名称是:
(2)装置B中盛装的试剂是
(3)为防止ClO2制备装置发生爆炸,实验中采取的措施:①将装置置于冰水浴中降温,②
(4)装置E为ClO2的收集装置,应将其置于
(5)装置F为氯气的尾气吸收装置,小组同学用胶头滴管将新制的饱和氯水慢慢滴入含有酚酞的NaOH溶液中,当滴到一定量时,红色突然褪去,小组同学对褪色原因提出假设:
假设1:
假设2:可能是氯水中存在HClO具有强氧化性,漂白褪色。
该小组同学设计实验证明假设1是否成立。实验方案为:取少许褪色后的溶液于试管中,滴加足量的NaOH溶液,若
您最近半年使用:0次
2023-11-06更新
|
622次组卷
|
2卷引用:宁夏银川市第二中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
9 . 学习小组在实验室中利用下图所示装置制备SO2并进行相关性质的探究。回答下列问题:
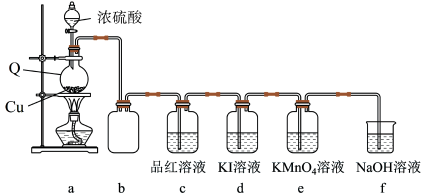
(1)仪器Q的名称为___________ ;装置 中品红溶液褪色,可证明SO2具有
中品红溶液褪色,可证明SO2具有___________ 性,装置b的作用是___________ 。
(2)向分液漏斗中滴加浓硫酸之前,需先通入一段时间N2,此操作的目的是___________ 。
(3)装置a中反应的化学方程式为___________ 。
(4)探究:探究SO2在KI溶液体系中的反应产物
实验开始后,发现装置d中的溶液迅速变黄,继续通入SO2,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在反应:SO2+4I-+4H+=S↓+2I2+2H2O。但有同学提出上述反应生成的I2可与SO2发生反应:SO2+I2+2H2O=SO +2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
+2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
Ⅰ.取适量装置d中浊液,向其中滴加几滴___________ ,振荡,无明显变化,浊液中无I2。
a.高锰酸钾溶液 b.淀粉溶液 c.氢氧化钠溶液
Ⅱ.将装置d中浊液进行分离,得淡黄色固体和澄清溶液;取适量分离后的澄清溶液于试管中,___________ ,出现白色沉淀,产物溶液中存在SO 。
。
综上可知,SO2在KI溶液中发生了歧化反应,其反应的离子方程式为___________ 。

(1)仪器Q的名称为
 中品红溶液褪色,可证明SO2具有
中品红溶液褪色,可证明SO2具有(2)向分液漏斗中滴加浓硫酸之前,需先通入一段时间N2,此操作的目的是
(3)装置a中反应的化学方程式为
(4)探究:探究SO2在KI溶液体系中的反应产物
实验开始后,发现装置d中的溶液迅速变黄,继续通入SO2,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在反应:SO2+4I-+4H+=S↓+2I2+2H2O。但有同学提出上述反应生成的I2可与SO2发生反应:SO2+I2+2H2O=SO
 +2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
+2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。Ⅰ.取适量装置d中浊液,向其中滴加几滴
a.高锰酸钾溶液 b.淀粉溶液 c.氢氧化钠溶液
Ⅱ.将装置d中浊液进行分离,得淡黄色固体和澄清溶液;取适量分离后的澄清溶液于试管中,
 。
。综上可知,SO2在KI溶液中发生了歧化反应,其反应的离子方程式为
您最近半年使用:0次
名校
解题方法
10 . 下图是实验室制备氯气并进行一系列相关实验的部分装置(夹持设备已略)。
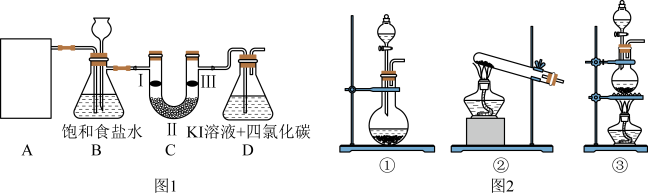
(1)实验室可以用 与浓盐酸反应制备氯气,发生反应的化学方程式为
与浓盐酸反应制备氯气,发生反应的化学方程式为_______ 。该实验中,A部分的发生装置可选图2中的_______ (填序号)。
(2)装置B中饱和食盐水的作用是_______ ;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,写出发生堵塞时B中的现象_______ 。
(3)装置C的实验目的是验证氯气是否具有漂白性,则C中I、Ⅱ、Ⅲ应依次放入_______ (填字母)。
(4)设计装置D的目的是比较氯、碘单质的氧化性。当向D中缓缓通入一定量氯气时,观察到D中_______ ,即可证明 氧化性大于
氧化性大于 。
。
(5)该实验装置存在明显的缺陷,应进行的改进措施是_______ (用离子方程式表示)。

(1)实验室可以用
 与浓盐酸反应制备氯气,发生反应的化学方程式为
与浓盐酸反应制备氯气,发生反应的化学方程式为(2)装置B中饱和食盐水的作用是
(3)装置C的实验目的是验证氯气是否具有漂白性,则C中I、Ⅱ、Ⅲ应依次放入
| 选项 | a | b | c | d |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 浓硫酸 | 碱石灰 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
 氧化性大于
氧化性大于 。
。(5)该实验装置存在明显的缺陷,应进行的改进措施是
您最近半年使用:0次
2023-07-31更新
|
296次组卷
|
3卷引用:宁夏回族自治区银川市宁夏育才中学2023-2024学年高一上学期1月期末考试化学试题
宁夏回族自治区银川市宁夏育才中学2023-2024学年高一上学期1月期末考试化学试题陕西省汉中市2020-2021学年高一上学期期末考试化学试题(已下线)期末测试卷02-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)



