1 . 焦亚硫酸钠(Na2S2O5)是一种常用的食品抗氧化剂(易被氧化)。实验室利用如图所示装置制取少量焦亚硫酸钠,并探究SO2的性质(夹持装置已略去)。
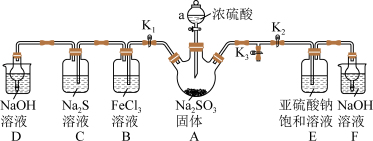
请回答下列问题:(实验前已除去装置中的空气)
(1)关闭K2、K3,打开K1,装置B中发生反应的离子方程式为___________ ;
(2)观察到装置C中产生的现象是___________ ;
(3)实验前,配制亚硫酸钠饱和溶液所用的蒸馏水需经煮沸后迅速冷却,目的___________ ,关闭K1、K3,打开K2,一段时间后装置E中有Na2S2O5晶体析出,装置E中发生反应的化学方程式为___________ ;
(4)设计实验验证Na2S2O5晶体在空气中已被氧化,所需试剂为___________ ;
(5)在测定某葡萄酒中Na2S2O5的残留量时,取40.00mL葡萄酒样品,加入指示剂,用0.01000mol·L-1的碘标准液滴定,当溶液___________ ,即为终点。测定实验中,消耗碘标准液10.00mL,该样品中Na2S2O5的残留量为___________ g·L-1(以SO2计算)。

请回答下列问题:(实验前已除去装置中的空气)
(1)关闭K2、K3,打开K1,装置B中发生反应的离子方程式为
(2)观察到装置C中产生的现象是
(3)实验前,配制亚硫酸钠饱和溶液所用的蒸馏水需经煮沸后迅速冷却,目的
(4)设计实验验证Na2S2O5晶体在空气中已被氧化,所需试剂为
(5)在测定某葡萄酒中Na2S2O5的残留量时,取40.00mL葡萄酒样品,加入指示剂,用0.01000mol·L-1的碘标准液滴定,当溶液
您最近一年使用:0次
名校
解题方法
2 . 碳、硫的含量影响钢铁性能。碳、硫含量的一种测定方法是将钢样中的碳、硫转化为气体,再用测碳、测硫装置进行测定。如图将转化的气体CO2和SO2通入测碳装置中,采用重量法测定碳的含量。下列说法不正确的是
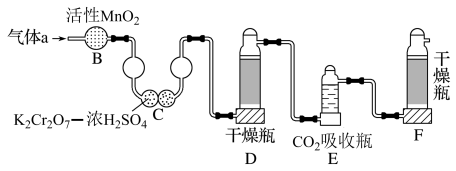

| A.B装置中MnO2作氧化剂 |
| B.C装置用于检验SO2是否除尽 |
| C.D和F装置瓶底均装有碱性干燥剂 |
| D.E装置用NaOH做吸收剂 |
您最近一年使用:0次
名校
解题方法
3 . 某小组同学想利用所学的知识去探究SO2的性质,设计了如下研究程序,合理的是
| A.分类(预测SO2的化学性质)→观察(得出SO2的物理性质)→实验→比较并得出结论 |
| B.观察(得出SO2的物理性质)→分类(预测SO2的化学性质)→实验(观察实验现象、验证预测)→比较得出结论,对于异常现象再预测,再实验,再验证 |
| C.观察(得出SO2的物理性质)→实验→分类(预测SO2的化学性质)→比较并得出结论 |
| D.实验→分类(预测SO2的化学性质)→观察(得出SO2的物理性质)→比较并得出结论 |
您最近一年使用:0次
2021-12-04更新
|
49次组卷
|
6卷引用:宁夏石嘴山市平罗中学2021-2022学年高一上学期期中考试化学试题
解题方法
4 . 由一种短周期金属元素和一种非金属元素组成的化合物X可与水发生复分解反应。某校兴趣小组用如图所示装置(夹持装置略去)对其进行探究实验。
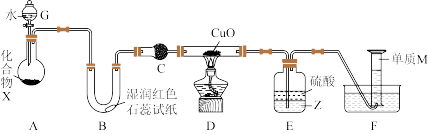
(1) 中红色石蕊试纸变蓝,则单质
中红色石蕊试纸变蓝,则单质 的电子式为
的电子式为___________ 。
(2)化合物 中含组成单质
中含组成单质 的元素的质量分数为16.9%,写出
的元素的质量分数为16.9%,写出 与水反应的化学方程式:
与水反应的化学方程式:___________ 。
(3) 中的试剂名称为
中的试剂名称为___________ 。
(4)实验时,装置 中硬质玻璃管内的现象为
中硬质玻璃管内的现象为___________ 。
(5)装置 中试剂
中试剂 为
为___________ (填化学式),装置 的作用是
的作用是___________ 。
(6)若不通过 、
、 两装置,请设计实验方案证明
两装置,请设计实验方案证明 中发生了反应(不通过观察
中发生了反应(不通过观察 中固体颜色变化:
中固体颜色变化:___________ 。
(7)若装置 中固体样品含有杂质(杂质不参与反应),某同学通过测定
中固体样品含有杂质(杂质不参与反应),某同学通过测定 中单质
中单质 在标准状况下的体积和固体样品的质量,以确定固体样品中
在标准状况下的体积和固体样品的质量,以确定固体样品中 的质量分数,判断该方案是否可行,并说明原因:
的质量分数,判断该方案是否可行,并说明原因:___________ 。


(1)
 中红色石蕊试纸变蓝,则单质
中红色石蕊试纸变蓝,则单质 的电子式为
的电子式为(2)化合物
 中含组成单质
中含组成单质 的元素的质量分数为16.9%,写出
的元素的质量分数为16.9%,写出 与水反应的化学方程式:
与水反应的化学方程式:(3)
 中的试剂名称为
中的试剂名称为(4)实验时,装置
 中硬质玻璃管内的现象为
中硬质玻璃管内的现象为(5)装置
 中试剂
中试剂 为
为 的作用是
的作用是(6)若不通过
 、
、 两装置,请设计实验方案证明
两装置,请设计实验方案证明 中发生了反应(不通过观察
中发生了反应(不通过观察 中固体颜色变化:
中固体颜色变化:(7)若装置
 中固体样品含有杂质(杂质不参与反应),某同学通过测定
中固体样品含有杂质(杂质不参与反应),某同学通过测定 中单质
中单质 在标准状况下的体积和固体样品的质量,以确定固体样品中
在标准状况下的体积和固体样品的质量,以确定固体样品中 的质量分数,判断该方案是否可行,并说明原因:
的质量分数,判断该方案是否可行,并说明原因:
您最近一年使用:0次
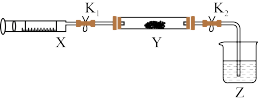
5 . ClO2作为一种广谱型的消毒剂,将逐渐用来取代Cl2,成为自来水的消毒剂。已知ClO2是一种易溶于水而难溶于有机溶剂的气体,实验室制备ClO2的原理是用亚氯酸钠固体与氯气反应: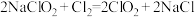 。下图是某兴趣小组在实验室制备和收集一定量纯净的
。下图是某兴趣小组在实验室制备和收集一定量纯净的 的装置(某些夹持装置和垫持用品省略)。其中
的装置(某些夹持装置和垫持用品省略)。其中 中盛有
中盛有 液体(用于除去
液体(用于除去 中的未反应的
中的未反应的 )。
)。
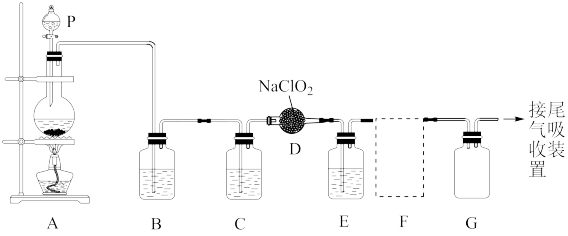
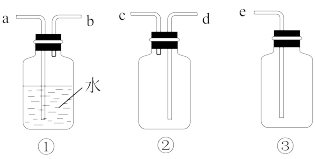
(1)仪器 的名称是
的名称是___________ 。
(2)写出装置 中烧瓶内发生反应的离子方程式:
中烧瓶内发生反应的离子方程式:___________ 。
(3) 装置中所盛试剂是
装置中所盛试剂是___________ 。
(4) 为
为 收集装置,应选用的装置是
收集装置,应选用的装置是___________ (填序号),其中与 装置导管相连的导管口是
装置导管相连的导管口是___________ (填接口字母)。
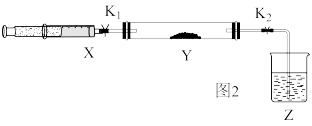
(5)该小组进一步研究 的性质,探究
的性质,探究 能否与
能否与 发生氧化还原反应。实验室用铜丝和浓硫酸反应生成
发生氧化还原反应。实验室用铜丝和浓硫酸反应生成 的化学方程式为
的化学方程式为___________ 。利用下列装置,在 中盛放少量
中盛放少量 。打开
。打开 、
、 ,将注射器
,将注射器 中
中 缓慢推入
缓慢推入 中,
中, 装置中淡黄色粉末颜色变成白色。设计方案检验生成的白色物质中含有
装置中淡黄色粉末颜色变成白色。设计方案检验生成的白色物质中含有 ;其方案为
;其方案为___________ 。
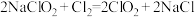 。下图是某兴趣小组在实验室制备和收集一定量纯净的
。下图是某兴趣小组在实验室制备和收集一定量纯净的 的装置(某些夹持装置和垫持用品省略)。其中
的装置(某些夹持装置和垫持用品省略)。其中 中盛有
中盛有 液体(用于除去
液体(用于除去 中的未反应的
中的未反应的 )。
)。

(1)仪器
 的名称是
的名称是(2)写出装置
 中烧瓶内发生反应的离子方程式:
中烧瓶内发生反应的离子方程式:(3)
 装置中所盛试剂是
装置中所盛试剂是(4)
 为
为 收集装置,应选用的装置是
收集装置,应选用的装置是 装置导管相连的导管口是
装置导管相连的导管口是(5)该小组进一步研究
 的性质,探究
的性质,探究 能否与
能否与 发生氧化还原反应。实验室用铜丝和浓硫酸反应生成
发生氧化还原反应。实验室用铜丝和浓硫酸反应生成 的化学方程式为
的化学方程式为 中盛放少量
中盛放少量 。打开
。打开 、
、 ,将注射器
,将注射器 中
中 缓慢推入
缓慢推入 中,
中, 装置中淡黄色粉末颜色变成白色。设计方案检验生成的白色物质中含有
装置中淡黄色粉末颜色变成白色。设计方案检验生成的白色物质中含有 ;其方案为
;其方案为
您最近一年使用:0次
名校
6 . 某小组探究三草酸合铁酸钾(K3[Fe(C2O4)3]·3H2O)的热分解产物,按图所示装置进行实验。
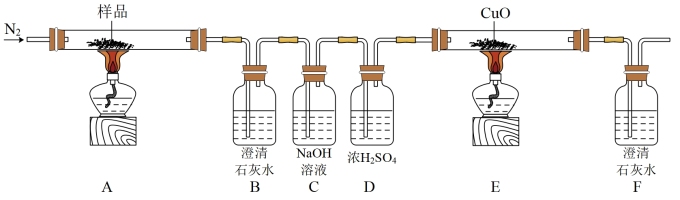
(1)通入N2的目的是___________ 。
(2)实验中观察到装置B变浑浊、E中固体变为红色、F变浑浊,由此可判断分解产物一定有___________ ,___________ 。
(3)样品完全分解后,装置A中的残留固体有FeO,Fe2O3和K2O,且FeO与Fe2O3的物质的量之比为2:1.再结合以上信息,写出三草酸合铁酸钾完全分解的化学方程式___________ 。
(4)为测定Fe2+和Fe3+溶液中铁元素的总含量,实验操作如下:准确量取20.00mL溶液于带塞锥形瓶中,加入足量H2O2,调节pH<2,加热除去过量H2O2;加入过量KI充分反应,再用0.1000mol∙L-1硫代硫酸钠标准液滴定至终点,消耗标准液20.00mL(已知I2+2 =2I-+
=2I-+ )。
)。
①加热除去过量H2O2的目的是___________ 。
②加入KI溶液发生的离子方程式___________ 。
③溶液中铁元素的总含量为___________ g·L-1

(1)通入N2的目的是
(2)实验中观察到装置B变浑浊、E中固体变为红色、F变浑浊,由此可判断分解产物一定有
(3)样品完全分解后,装置A中的残留固体有FeO,Fe2O3和K2O,且FeO与Fe2O3的物质的量之比为2:1.再结合以上信息,写出三草酸合铁酸钾完全分解的化学方程式
(4)为测定Fe2+和Fe3+溶液中铁元素的总含量,实验操作如下:准确量取20.00mL溶液于带塞锥形瓶中,加入足量H2O2,调节pH<2,加热除去过量H2O2;加入过量KI充分反应,再用0.1000mol∙L-1硫代硫酸钠标准液滴定至终点,消耗标准液20.00mL(已知I2+2
 =2I-+
=2I-+ )。
)。①加热除去过量H2O2的目的是
②加入KI溶液发生的离子方程式
③溶液中铁元素的总含量为
您最近一年使用:0次
2021-10-01更新
|
361次组卷
|
3卷引用:宁夏银川一中2022届高三第二次月考理科综合化学试题
宁夏银川一中2022届高三第二次月考理科综合化学试题甘肃省会宁县第三中学2021-2022学年高三上学期第三次月考化学试题(已下线)专题10 性质探究类综合实验-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
7 . 某研究性学习小组利用以下装置制取并探究氨气的性质。A中发生反应的化学方程式:2NH4Cl+Ca(OH)2 2NH3↑+2H2O+CaCl2。
2NH3↑+2H2O+CaCl2。

(1)仪器a的名称是__________________ 。
(2)A中的反应______ (填“是”或“不是”)氧化还原反应。
(3)A装置还可用于实验室制取______ 气体(填字母)。
a.CO2 b.H2 c.O2 d.Cl2
(4)为防止氨气逸出,造成空气污染,尾气处理的合适装置是____ (填“F”或“G”)。
(5)实验室收集氨气的方法是________ 。
(6)C、D装置中试纸颜色有变化的是_____ (填“C”或“D”)。
(7)实验进行一段时间后挤压装置E中的胶头滴管,滴入1~2滴浓盐酸,观察到的现象是__________ 。
(8)生石灰与水反应生成Ca(OH)2并放出热量[化学方程式为CaO+H2O=Ca(OH)2]。实验室利用此原理,往生石灰中滴加浓氨水,可以快速制取氨气。你认为生石灰可用下列_______ (填字母)物质代替。
a.碱石灰(NaOH与CaO的固体混合物)
b.NaOH固体
c.浓硫酸
d.石灰石(含CaCO3)
 2NH3↑+2H2O+CaCl2。
2NH3↑+2H2O+CaCl2。
(1)仪器a的名称是
(2)A中的反应
(3)A装置还可用于实验室制取
a.CO2 b.H2 c.O2 d.Cl2
(4)为防止氨气逸出,造成空气污染,尾气处理的合适装置是
(5)实验室收集氨气的方法是
(6)C、D装置中试纸颜色有变化的是
(7)实验进行一段时间后挤压装置E中的胶头滴管,滴入1~2滴浓盐酸,观察到的现象是
(8)生石灰与水反应生成Ca(OH)2并放出热量[化学方程式为CaO+H2O=Ca(OH)2]。实验室利用此原理,往生石灰中滴加浓氨水,可以快速制取氨气。你认为生石灰可用下列
a.碱石灰(NaOH与CaO的固体混合物)
b.NaOH固体
c.浓硫酸
d.石灰石(含CaCO3)
您最近一年使用:0次
解题方法
8 . 如下图所示的装置中,A是氯气发生仪器,C、D为气体净化装置(C中装有饱和食盐水,D中装有浓硫酸),E是硬质玻璃管装有细铁丝网,F为干燥的空广口瓶,烧杯G中装有氢氧化钠溶液。
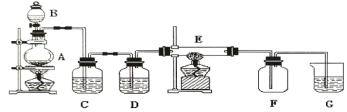
请回答下列问题:
(1)仪器A的名称是___________ ;B中盛装的药品是___________ ;
(2)请写出实验室制氯气的化学方程式并用单线桥法标出电子转移的方向和数目___________ ;
(3)C装置的作用是___________ ; D装置的作用是___________ ;
(4)E中发生化学反应的方程式为___________ ;
(5)烧杯G中氢氧化钠溶液的作用是___________ ;其发生反应的化学方程式为:___________ 。

请回答下列问题:
(1)仪器A的名称是
(2)请写出实验室制氯气的化学方程式并用单线桥法标出电子转移的方向和数目
(3)C装置的作用是
(4)E中发生化学反应的方程式为
(5)烧杯G中氢氧化钠溶液的作用是
您最近一年使用:0次
名校
解题方法
9 . 铁与水蒸气反应的实验装置如图,下列说法正确的是
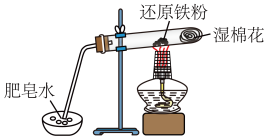

| A.实验时,试管口应高于试管底 |
| B.加热时试管内生成黑色物质,点燃肥皂泡可听到爆鸣声 |
| C.产生的气体在点燃前不需要检验纯度 |
| D.试管中发生化合反应 |
您最近一年使用:0次
2021-01-24更新
|
156次组卷
|
3卷引用:宁夏银川一中2020-2021学年高一上学期期末考试(GAC)化学试题
名校
解题方法
10 . 某同学为了检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物的性质,其中反应原理为C+2H2SO4 CO2↑+2SO2↑+2H2O↑。装置已经连接好,请回答下列问题。
CO2↑+2SO2↑+2H2O↑。装置已经连接好,请回答下列问题。
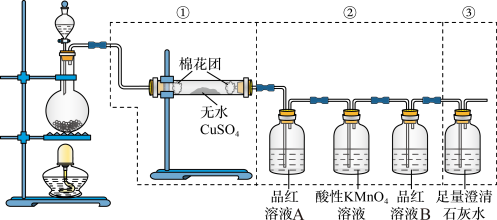
(1)①中无水硫酸铜的作用是_______ 。
(2)②中酸性KMnO4溶液的作用是_______ 。
(3)②中两次用到品红溶液,它们的作用分别是A_______ B_______ 。
(4)澄清石灰水的作用_______ ,出现的现象是_______ 。
 CO2↑+2SO2↑+2H2O↑。装置已经连接好,请回答下列问题。
CO2↑+2SO2↑+2H2O↑。装置已经连接好,请回答下列问题。
(1)①中无水硫酸铜的作用是
(2)②中酸性KMnO4溶液的作用是
(3)②中两次用到品红溶液,它们的作用分别是A
(4)澄清石灰水的作用
您最近一年使用:0次



