1 . 铜和浓硫酸共热能发生反应:Cu + 2H2SO4  CuSO4 + SO2↑+ 2H2O 。某化学兴趣小组的同学利用下图所示的装置,探究铜与浓硫酸的反应情况以及二氧化硫的化学性质。
CuSO4 + SO2↑+ 2H2O 。某化学兴趣小组的同学利用下图所示的装置,探究铜与浓硫酸的反应情况以及二氧化硫的化学性质。
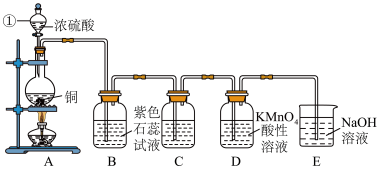
(1)上述装置中,仪器①的名称为_______ 。
(2)B中的现象是:_______ 。
(3)C中溶液的作用是检验SO2具有漂白性,则C中应装入的是_______ 溶液。
(4)D中溶液由紫色褪为无色,证明二氧化硫具有_______ 性(填“氧化”或“还原”)。
(5)若E中NaOH溶液足量,则其中发生反应的离子方程式为:_______ 。
(6)将烧瓶中反应后的溶液用水稀释,得到的溶液呈_______ 色。
(7)反应完毕,烧瓶中有铜剩余,请根据你所学知识判断,硫酸_______ (填“有”或“没有“)剩余。
 CuSO4 + SO2↑+ 2H2O 。某化学兴趣小组的同学利用下图所示的装置,探究铜与浓硫酸的反应情况以及二氧化硫的化学性质。
CuSO4 + SO2↑+ 2H2O 。某化学兴趣小组的同学利用下图所示的装置,探究铜与浓硫酸的反应情况以及二氧化硫的化学性质。
(1)上述装置中,仪器①的名称为
(2)B中的现象是:
(3)C中溶液的作用是检验SO2具有漂白性,则C中应装入的是
(4)D中溶液由紫色褪为无色,证明二氧化硫具有
(5)若E中NaOH溶液足量,则其中发生反应的离子方程式为:
(6)将烧瓶中反应后的溶液用水稀释,得到的溶液呈
(7)反应完毕,烧瓶中有铜剩余,请根据你所学知识判断,硫酸
您最近一年使用:0次
解题方法
2 . 将一块金属钠投入滴有紫色石蕊溶液的冷水中,可观察到的现象有
①钠投入水中,先沉入水底,后浮出水面②钠熔成闪亮的小球③反应后溶液变红④钠立即与水反应,并有气体产生⑤小球在水面上四处游动⑥有“嘶嘶”的响声发出
①钠投入水中,先沉入水底,后浮出水面②钠熔成闪亮的小球③反应后溶液变红④钠立即与水反应,并有气体产生⑤小球在水面上四处游动⑥有“嘶嘶”的响声发出
| A.①②③④ | B.②③④⑤ | C.②④⑤⑥ | D.③④⑥ |
您最近一年使用:0次
3 . 如图是实验室研究潜水艇中供氧体系反应机理的装置图(夹持仪器略)。
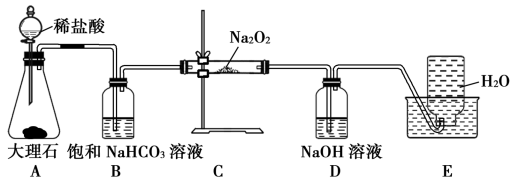
(1)A装置为CO2的发生装置,反应的离子方程式为_______ 。
(2)B装置可除去A装置中可能挥发出的HCl,反应的离子方程式为_______ 。
(3)C装置为O2的发生装置,同时该反应生成一种正盐,则反应的化学方程式为_______ 。
(4)D装置的作用_______ ,反应的化学方程式为_______ 。
(5)E装置为排水法收集O2的装置,检验所收集的气体为O2的方法为:_______ 。

(1)A装置为CO2的发生装置,反应的离子方程式为
(2)B装置可除去A装置中可能挥发出的HCl,反应的离子方程式为
(3)C装置为O2的发生装置,同时该反应生成一种正盐,则反应的化学方程式为
(4)D装置的作用
(5)E装置为排水法收集O2的装置,检验所收集的气体为O2的方法为:
您最近一年使用:0次
名校
4 . Fe是应用最广泛的金属,被誉为“金属之王”。某兴趣小组对Fe、Fe2+及Fe3+的某些性质进行实验探究。
(一)A小组按如图所示操作进行实验,探究氧化剂的氧化性强弱。
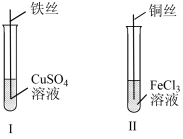
(1)Ⅰ中发生反应的离子方程式为___ 。
(2)Ⅱ中发生反应的化学方程式为___ 。
(3)结合实验Ⅰ、Ⅱ可知Fe2+,Cu2+,Fe3+的氧化性由强到弱的顺序为___ 。
(二)B小组研究Fe与水蒸气的反应,分别进行了如图实验。
请回答:
(4)实验Ⅰ中湿棉花的作用是____ 。
(5)实验Ⅰ中反应的化学方程式是___ 。
(6)若观察到实验Ⅰ中肥皂液持续产生肥皂泡,实验Ⅱ中溶液B呈现红色。说明溶液A中含有___ 。
(7)若观察到实验Ⅰ中肥皂液持续产生肥皂泡,但实验Ⅱ中溶液B未呈现红色。溶液B未呈现红色的原因是___ 。
(一)A小组按如图所示操作进行实验,探究氧化剂的氧化性强弱。

(1)Ⅰ中发生反应的离子方程式为
(2)Ⅱ中发生反应的化学方程式为
(3)结合实验Ⅰ、Ⅱ可知Fe2+,Cu2+,Fe3+的氧化性由强到弱的顺序为
(二)B小组研究Fe与水蒸气的反应,分别进行了如图实验。
| 实验Ⅰ | 实验Ⅱ |
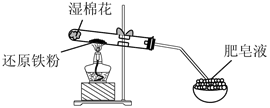 | 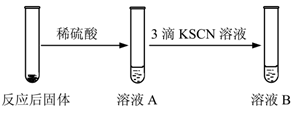 |
(4)实验Ⅰ中湿棉花的作用是
(5)实验Ⅰ中反应的化学方程式是
(6)若观察到实验Ⅰ中肥皂液持续产生肥皂泡,实验Ⅱ中溶液B呈现红色。说明溶液A中含有
(7)若观察到实验Ⅰ中肥皂液持续产生肥皂泡,但实验Ⅱ中溶液B未呈现红色。溶液B未呈现红色的原因是
您最近一年使用:0次
5 .  和
和 是两种重要的钠盐。
是两种重要的钠盐。
(1)探究 、
、 的稳定性
的稳定性

如图所示,在加热过程中能观察到产生白色沉淀的烧杯是___________ (填“Ⅰ”或“Ⅱ”),该烧杯中发生反应的离子方程式是___________ ,通过该实验可比较出___________ (填“ ”或“
”或“ ”)更稳定。
”)更稳定。
(2)探究 、
、 溶液分别与盐酸反应过程的热量变化
溶液分别与盐酸反应过程的热量变化
步骤1:分别取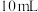 等浓度的
等浓度的 、
、 溶液,测量温度为
溶液,测量温度为 ;
;
步骤2:分别加入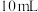 密度约为
密度约为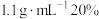 的盐酸(20℃),搅拌,测量温度为
的盐酸(20℃),搅拌,测量温度为 ;
;
步骤3:数据记录:
步骤4:实验分析。甲同学分析上述数据认为两个反应都放出热量,乙同学认为甲同学的分析不严谨,应该补做如下实验:向盛有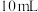 水(20℃)的烧杯中加入
水(20℃)的烧杯中加入___________ ,搅拌,测量温度为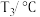 ,再比较
,再比较 和
和 的大小。若
的大小。若___________ ,说明 溶液与盐酸的反应吸收热量,而
溶液与盐酸的反应吸收热量,而 与盐酸的反应放出热量。
与盐酸的反应放出热量。
(3)除去 粉末中混有的少量
粉末中混有的少量 的方法是
的方法是___________ ,所涉及反应的化学方程式为___________ 。
 和
和 是两种重要的钠盐。
是两种重要的钠盐。(1)探究
 、
、 的稳定性
的稳定性
如图所示,在加热过程中能观察到产生白色沉淀的烧杯是
 ”或“
”或“ ”)更稳定。
”)更稳定。(2)探究
 、
、 溶液分别与盐酸反应过程的热量变化
溶液分别与盐酸反应过程的热量变化步骤1:分别取
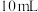 等浓度的
等浓度的 、
、 溶液,测量温度为
溶液,测量温度为 ;
;步骤2:分别加入
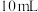 密度约为
密度约为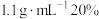 的盐酸(20℃),搅拌,测量温度为
的盐酸(20℃),搅拌,测量温度为 ;
;步骤3:数据记录:
| 温度 试剂 | 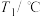 | 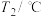 |
 | 20.0 | 23.7 |
 | 20.0 | 20.8 |
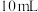 水(20℃)的烧杯中加入
水(20℃)的烧杯中加入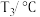 ,再比较
,再比较 和
和 的大小。若
的大小。若 溶液与盐酸的反应吸收热量,而
溶液与盐酸的反应吸收热量,而 与盐酸的反应放出热量。
与盐酸的反应放出热量。(3)除去
 粉末中混有的少量
粉末中混有的少量 的方法是
的方法是
您最近一年使用:0次
2021-12-03更新
|
112次组卷
|
3卷引用:广西南宁市宾阳县宾阳中学2021-2022学年高一上学期期中考试化学试题
解题方法
6 . 在实验室里,某同学取一小块金属钠做钠与水反应的实验,试回答下列问题:
(1)切开的金属钠暴露在空气中,观察到的现象是___________ ,所发生反应的化学方程式是___________ 。
(2)将钠投入水中后,钠熔化成一个小球,根据这一现象你能得出的结论是:①_____ ,②_____ 。将一小块钠投入盛有石灰水的烧杯中,不可能观察到的现象是③ _____ (填序号)。
A.有气体生成
B.钠熔化成小球并在液面上游动
C.烧杯底部有银白色的金属钙生成
D.溶液变浑浊
(3)钠与水反应的化学方程式为_____ 。
(4)根据上述实验过程中钠所发生的有关变化,试说明金属钠着火应用什么扑灭___________ 。
(1)切开的金属钠暴露在空气中,观察到的现象是
(2)将钠投入水中后,钠熔化成一个小球,根据这一现象你能得出的结论是:①
A.有气体生成
B.钠熔化成小球并在液面上游动
C.烧杯底部有银白色的金属钙生成
D.溶液变浑浊
(3)钠与水反应的化学方程式为
(4)根据上述实验过程中钠所发生的有关变化,试说明金属钠着火应用什么扑灭
您最近一年使用:0次
解题方法
7 . 绿矾(FeSO4·xH2O)是自然界存在的一种矿石,翠绿如宝石,很早就引起人们的重视;绿矾焙烧是一种生产硫酸的古老方法。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,若产生___________ 现象,说明该样品已变质。
(2)为测定绿矾中结晶水含量,将石英玻璃管A(带两端开关K1和K2)称重,质量为150.0g,将样品装入石英玻璃管中,再次将装置A称重,质量为177.7g。按如图所示连接好装置进行实验,A中发生的反应为:FeSO4·xH2O FeSO4+xH2O↑。
FeSO4+xH2O↑。
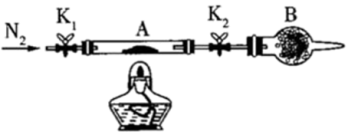
①仪器B的名称是___________ 。
②下列实验操作步骤,正确的顺序为da___________ e;重复上述操作步骤,直至装置A恒重,质量为165.2g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2 d.打开K1和K2,缓缓通入N2 e.称量装置A f.冷却到室温
③根据实验记录,计算绿矾化学式中结晶水数目x=___________ (结果保留到小数点后一位)。
(3)为探究硫酸亚铁高温分解的产物,将(2)中已恒重的装置A接入如图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。
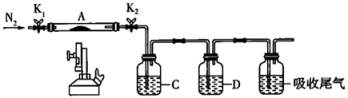
①加热前通入N2的作用是___________ 。
②C中盛有BaCl2溶液,观察到C中有白色沉淀生成,则该沉淀是___________ (填化学式)。
③D中所盛的试剂为品红溶液,观察到溶液褪色。根据上述实验现象,写出硫酸亚铁高温分解的化学反应方程式:___________ 。
(4)绿矾的纯度可通过KMnO4滴定法测定。现称取2.780g绿矾样品,配制成250mL溶液,用硫酸酸化的0.0100mol·L-1的KMnO4溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
①此滴定实验达到终点的现象是___________ 。
②上表中第一次实验记录数据明显大于后两次,其原因可能是___________ (填字母)。
A.第一次滴定前酸式滴定管尖嘴有气泡,滴定结束无气泡
B.第一次滴定用的锥形瓶用待测液润洗过
C.第一次滴定结束时,俯视读取酸性高锰酸钾溶液的体积
D.后两次滴定所用酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,若产生
(2)为测定绿矾中结晶水含量,将石英玻璃管A(带两端开关K1和K2)称重,质量为150.0g,将样品装入石英玻璃管中,再次将装置A称重,质量为177.7g。按如图所示连接好装置进行实验,A中发生的反应为:FeSO4·xH2O
 FeSO4+xH2O↑。
FeSO4+xH2O↑。
①仪器B的名称是
②下列实验操作步骤,正确的顺序为da
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2 d.打开K1和K2,缓缓通入N2 e.称量装置A f.冷却到室温
③根据实验记录,计算绿矾化学式中结晶水数目x=
(3)为探究硫酸亚铁高温分解的产物,将(2)中已恒重的装置A接入如图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。

①加热前通入N2的作用是
②C中盛有BaCl2溶液,观察到C中有白色沉淀生成,则该沉淀是
③D中所盛的试剂为品红溶液,观察到溶液褪色。根据上述实验现象,写出硫酸亚铁高温分解的化学反应方程式:
(4)绿矾的纯度可通过KMnO4滴定法测定。现称取2.780g绿矾样品,配制成250mL溶液,用硫酸酸化的0.0100mol·L-1的KMnO4溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 24.52 | 24.02 | 23.98 |
②上表中第一次实验记录数据明显大于后两次,其原因可能是
A.第一次滴定前酸式滴定管尖嘴有气泡,滴定结束无气泡
B.第一次滴定用的锥形瓶用待测液润洗过
C.第一次滴定结束时,俯视读取酸性高锰酸钾溶液的体积
D.后两次滴定所用酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低
您最近一年使用:0次
名校
8 . “绿色化学”走进课堂,某学习小组在老师的指导下,设计了“氯气与金属钠反应”的实验。实验操作:钠与氯气反应的装置可作如图改进,将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆粒大小的金属钠(已吸净煤油),玻璃管尾部塞一团浸有 溶液的棉花球。先给钠预热,到钠熔化成小球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是
溶液的棉花球。先给钠预热,到钠熔化成小球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是
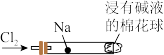
 溶液的棉花球。先给钠预热,到钠熔化成小球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是
溶液的棉花球。先给钠预热,到钠熔化成小球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是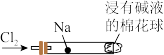
A.浸有 溶液的棉球主要用于防止空气中二氧化碳进来与钠反应 溶液的棉球主要用于防止空气中二氧化碳进来与钠反应 |
| B.反应生成的大量白烟是氯化钠晶体 |
| C.从实验现象上判断钠的熔点较低 |
| D.钠有很强的还原性,本质原因是钠原子的最外层只有1个电子,该电子很容易失去 |
您最近一年使用:0次
2021-09-16更新
|
1442次组卷
|
11卷引用:广西河池市高级中学2021-2022学年高三上学期第二次月考化学试题
广西河池市高级中学2021-2022学年高三上学期第二次月考化学试题浙江省宁波市镇海中学2020-2021学年高一上学期期末考试化学试卷山东省滨州邹平市黄山中学2021-2022学年高一上学期第一次月考化学试题重庆市育才中学校2021-2022学年高一上学期期中考试化学试题 广东省汕头市澄海中学2021-2022学年高一上学期期中考试化学试题湖南省衡阳市2021-2022学年高一上学期期末质量检测化学试题(已下线)2.2.2 氯气与金属、非金属及还原性化合物的反应-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)广东省广州市第二中学教育集团2022-2023学年高一上学期期中考试化学试题湖北省荆州中学2022-2023学年高一上学期期末考试化学试题(已下线)【知识图鉴】单元讲练测必修第一册第二单元03巩固练江西省赣州市信丰中学2023-2024学年高一上学期第四次月考化学试题
20-21高一下·广西南宁·阶段练习
解题方法
9 . 某化学小组欲进行如下的实验探究金属与浓硫酸反应。试回答下列问题:

(1)利用上图装置研究铜与浓硫酸反应,反应的化学方程式为___________ 。C装置中的试剂应为___________ 溶液。
(2)将上述实验中的铜改为铁,在常温下进行,无明显现象,其原因是___________ 。在加热条件下,实验的后阶段可观察到倒立的漏斗边沿有气体冒出,该气体可能为___________ 。验证该气体的实验方案如下:

①装置连接顺序:X→___________→___________→___________→___________→a→b→___________;___________
②能证明上述假设成立的实验现象是___________ 。
③某学习小组经过讨论发现该实验方案还不够严谨,请你指出不严谨之处___________ 。

(1)利用上图装置研究铜与浓硫酸反应,反应的化学方程式为
(2)将上述实验中的铜改为铁,在常温下进行,无明显现象,其原因是

①装置连接顺序:X→___________→___________→___________→___________→a→b→___________;
②能证明上述假设成立的实验现象是
③某学习小组经过讨论发现该实验方案还不够严谨,请你指出不严谨之处
您最近一年使用:0次
解题方法
10 . 实验室里研究不同价态硫元素之间的转化。
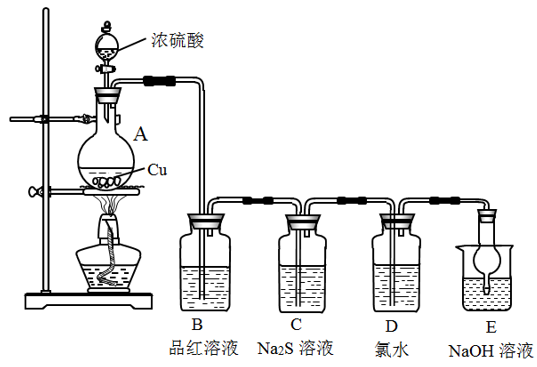
(1)盛装浓硫酸仪器的名称是___________ 。
(2)A装置中发生反应的化学方程式为___________ 。
(3)写出D装置中发生反应的离子方程式___________ 。
(4)C装置中观察到的现象是___________ ;上述实验体现SO2的性质有漂白性、氧化性和___________ 。
(5)下列有关硫及其化合物的叙述正确的是___________ 。
A.食品中添加适量二氧化硫可以起到防腐和抗氧化等作用
B.硫在足量空气中燃烧生成SO3
C.向SO2水溶液中滴加BaCl2溶液,会生成BaSO3白色沉淀
D.浓硫酸与蔗糖反应的实验体现了浓硫酸的脱水性和强氧化性
E.除去SO2中含有的少量HCl气体,可以使气体通过饱和Na2SO3溶液

(1)盛装浓硫酸仪器的名称是
(2)A装置中发生反应的化学方程式为
(3)写出D装置中发生反应的离子方程式
(4)C装置中观察到的现象是
(5)下列有关硫及其化合物的叙述正确的是
A.食品中添加适量二氧化硫可以起到防腐和抗氧化等作用
B.硫在足量空气中燃烧生成SO3
C.向SO2水溶液中滴加BaCl2溶液,会生成BaSO3白色沉淀
D.浓硫酸与蔗糖反应的实验体现了浓硫酸的脱水性和强氧化性
E.除去SO2中含有的少量HCl气体,可以使气体通过饱和Na2SO3溶液
您最近一年使用:0次



