1 . 镁能在二氧化碳中燃烧: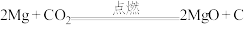 ,钠比镁更活泼,那么钠能在二氧化碳中燃烧吗?某研究性学习小组设计了如图装置进行探究。
,钠比镁更活泼,那么钠能在二氧化碳中燃烧吗?某研究性学习小组设计了如图装置进行探究。
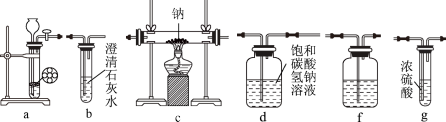
请回答下列问题:
(1)写出装置a中发生反应的离子方程式___________ 。
(2)按照气流的方向从左至右连接装置:a接___________ 、___________ 、___________ 、___________ 、___________ 。
(3)装置f中应盛放的试剂是___________ ,装置b的作用是___________ 。
(4)实验过程中,在点燃装置c中的酒精灯前,必须经过必要的操作,方可进行后续的实验,该必要操作的目的是___________ 。
(5)实验发现钠在充满二氧化碳气体的玻璃管里剧烈地燃烧,产生大量的白烟并伴有黑色物质生成。取一部分生成物于试管中,往试管中加水,白色物质溶解,黑色物质不溶。过滤,得到澄清的滤液。将滤纸上的黑色物质移人小试管中,加少量浓硫酸,加热,有刺激性气味的气体生成。则该黑色物质与浓硫酸共热的化学反应方程式为___________ 。
(6)往(5)所得滤液中加澄清石灰水,溶液变浑浊。再滴入稀盐酸,溶液中有气泡出现。试写出钠与二氧化碳反应的化学方程式:___________ 。
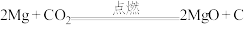 ,钠比镁更活泼,那么钠能在二氧化碳中燃烧吗?某研究性学习小组设计了如图装置进行探究。
,钠比镁更活泼,那么钠能在二氧化碳中燃烧吗?某研究性学习小组设计了如图装置进行探究。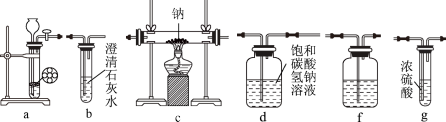
请回答下列问题:
(1)写出装置a中发生反应的离子方程式
(2)按照气流的方向从左至右连接装置:a接
(3)装置f中应盛放的试剂是
(4)实验过程中,在点燃装置c中的酒精灯前,必须经过必要的操作,方可进行后续的实验,该必要操作的目的是
(5)实验发现钠在充满二氧化碳气体的玻璃管里剧烈地燃烧,产生大量的白烟并伴有黑色物质生成。取一部分生成物于试管中,往试管中加水,白色物质溶解,黑色物质不溶。过滤,得到澄清的滤液。将滤纸上的黑色物质移人小试管中,加少量浓硫酸,加热,有刺激性气味的气体生成。则该黑色物质与浓硫酸共热的化学反应方程式为
(6)往(5)所得滤液中加澄清石灰水,溶液变浑浊。再滴入稀盐酸,溶液中有气泡出现。试写出钠与二氧化碳反应的化学方程式:
您最近一年使用:0次
2 . 某化学兴趣小组利用如图所示装置进行“铁与水反应”的实验,并检验产物的性质,且要对反应后硬质试管中固体物质的组成进行探究。请回答下列问题:
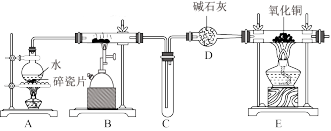
(1)A的作用是___________ ,B中反应的化学方程式为___________ 。
(2)D的作用是___________ 。
(3)E中的现象是______ 。
(4)A、B两个装置中应先点燃______ 处的酒精(喷)灯(填“A”或“E”),点燃E处酒精灯之前应进行的操作是______ 。
(5)该小组对反应后硬质试管中固体物质的组成提出了如下假设。
假设1:只有Fe;
假设2:只有____ (填化学式);
假设3:既有Fe也有Fe3O4。
(6)为了验证反应后硬质试管中固体物质的组成,该同学进行了定量研究:反应前固体物质的质量为5.6g,反应后固体物质的质量为6.6g.从数据分析,反应后硬质试管中固体物质的组成为_____ 。

(1)A的作用是
(2)D的作用是
(3)E中的现象是
(4)A、B两个装置中应先点燃
(5)该小组对反应后硬质试管中固体物质的组成提出了如下假设。
假设1:只有Fe;
假设2:只有
假设3:既有Fe也有Fe3O4。
(6)为了验证反应后硬质试管中固体物质的组成,该同学进行了定量研究:反应前固体物质的质量为5.6g,反应后固体物质的质量为6.6g.从数据分析,反应后硬质试管中固体物质的组成为
您最近一年使用:0次
名校
解题方法
3 . 某实验小组欲在实验室探究氯气的性质和模拟工业上制取漂白粉,设计了如下装置进行实验。

回答下列问题:
(1)装置A中发生反应的化学方程式为___________ ,装置B的作用是___________ 。
(2)实验时,观察到装置C中出现的现象是___________ ,出现该现象的原因是___________ 。
(3)若装置E中布条不褪色,装置F中布条褪色,则装置D中盛放的试剂甲是___________ (填名称)。
(4)装置G中生成漂白粉,漂白粉的有效成分是___________ ,漂白粉应密闭保存,请说明原因:___________ 。

回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)实验时,观察到装置C中出现的现象是
(3)若装置E中布条不褪色,装置F中布条褪色,则装置D中盛放的试剂甲是
(4)装置G中生成漂白粉,漂白粉的有效成分是
您最近一年使用:0次
2021-12-18更新
|
211次组卷
|
2卷引用:山西省临汾新华中学2021-2022学年高一上学期第四次月考化学试题
名校
解题方法
4 . 某实验小组用漂白粉[主要成分为CaCl2、Ca(ClO)2]和浓盐酸制备氯气,进行相关性质实验,并模拟制备“84”消毒液,实验装置如下图所示(夹持仪器已略):

已知:
回答下列问题:
(1)A中盛浓盐酸的仪器名称是___________ 。
(2)探究新制氯水的组成
①关闭k1、k4,打开k2、k3,至C中的水变为浅黄绿色时关闭k2。
②取C中溶液,滴加少量紫色石蕊溶液,观察到的现象是___________ ,证明新制氯水中含有的微粒是___________ (填化学符号)。
③甲同学打开k4,将C中溶液放入B中,观察到的现象是___________ ,据此甲同学认为Cl2溶于水生成Cl-。乙同学认为甲的结论不正确,乙同学的理由是___________ ,改进措施是___________ 。
(3)模拟制备“84”消毒液。操作为关闭k3,打开k1、k2,至E中充满大量黄绿色气体时关闭k2.取E中溶液VmL,先加入足量双氧水,发生反应 ,再加入足量硝酸酸化的硝酸银溶液,充分反应,过滤、洗涤、干燥、称量,得固体mg,试计算所制“84”消毒液中有效成分的物质的量浓度为
,再加入足量硝酸酸化的硝酸银溶液,充分反应,过滤、洗涤、干燥、称量,得固体mg,试计算所制“84”消毒液中有效成分的物质的量浓度为___________ mol·L-1(用含“V”和“m”的式子表示)。

已知:

回答下列问题:
(1)A中盛浓盐酸的仪器名称是
(2)探究新制氯水的组成
①关闭k1、k4,打开k2、k3,至C中的水变为浅黄绿色时关闭k2。
②取C中溶液,滴加少量紫色石蕊溶液,观察到的现象是
③甲同学打开k4,将C中溶液放入B中,观察到的现象是
(3)模拟制备“84”消毒液。操作为关闭k3,打开k1、k2,至E中充满大量黄绿色气体时关闭k2.取E中溶液VmL,先加入足量双氧水,发生反应
 ,再加入足量硝酸酸化的硝酸银溶液,充分反应,过滤、洗涤、干燥、称量,得固体mg,试计算所制“84”消毒液中有效成分的物质的量浓度为
,再加入足量硝酸酸化的硝酸银溶液,充分反应,过滤、洗涤、干燥、称量,得固体mg,试计算所制“84”消毒液中有效成分的物质的量浓度为
您最近一年使用:0次
2021-12-10更新
|
167次组卷
|
3卷引用:山西省太原市第五中学2021-2022学年高一上学期12月月考化学试题
5 . 已知氯气和氢氧化钠的反应条件不同,产物也不同。在实验室里可用如图所示装置制取氯酸钠、次氯酸钠和探究氯水的性质。
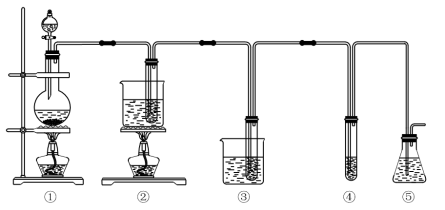
图中:①为氯气发生装置;②试管里盛有15mL30%NaOH溶液,并置于热水浴中;③试管里盛有15mL8%NaOH溶液,并置于冰水浴中;④试管里盛有紫色石蕊试液;⑤为尾气吸收装置。请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的MnO2,通过___ (填写仪器名称)向烧瓶中加入适量的___ (填写试剂名称)。
(2)写出制取氯气的离子反应方程式__ 。
(3)实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有___ (填写下列编号字母)的净化装置。
(4)比较制取氯酸钠和次氯酸钠的条件,指出二者的差异:___ 。
(5)反应完毕经冷却后,②的试管中有大量晶体析出,图中符合该晶体溶解度随温度变化规律的曲线是___ (选填字母);从②的试管中分离该晶体的操作是___ 。(填写实验操作名称)

(6)实验中可观察到④的试管中溶液颜色会发生变化:___ ,原因是___ (填写离子方程式)。
(7)本实验中制取氯酸钠的化学方程式是__ 。

图中:①为氯气发生装置;②试管里盛有15mL30%NaOH溶液,并置于热水浴中;③试管里盛有15mL8%NaOH溶液,并置于冰水浴中;④试管里盛有紫色石蕊试液;⑤为尾气吸收装置。请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的MnO2,通过
(2)写出制取氯气的离子反应方程式
(3)实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有
| A.碱石灰 | B.饱和食盐水 | C.浓硫酸 | D.饱和碳酸氢钠溶液 |
(5)反应完毕经冷却后,②的试管中有大量晶体析出,图中符合该晶体溶解度随温度变化规律的曲线是

(6)实验中可观察到④的试管中溶液颜色会发生变化:
(7)本实验中制取氯酸钠的化学方程式是
您最近一年使用:0次
名校
解题方法
6 . 下列关于化学学习和研究的说法错误的是
| A.化学模型有助于解释一些化学现象 |
| B.化学家提出的假设都能被实验证实 |
| C.运用分类的方法,可根据物质所属的类别预测物质的性质 |
| D.化学基本原理的应用是有一定条件的 |
您最近一年使用:0次
2021-11-16更新
|
143次组卷
|
2卷引用:山西省怀仁市2021-2022学年高三上学期期中化学试题
名校
解题方法
7 . 学校化学兴趣小组对过氧化钠的化学性质进行了初步探究。
(I)该小组设计如图实验装置,验证“二氧化碳与水接触时才能和过氧化钠反应”。
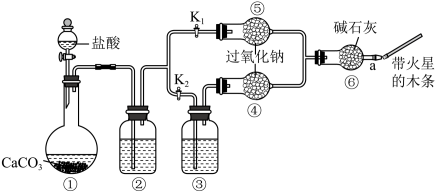
步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤2:打开弹簧夹K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(1)装置①中反应的离子方程式是___________ ;
(2)装置②的作用是___________ ;装置③中的试剂是___________ 。
(3)本实验预期现象是___________ 。
(4)过氧化钠跟二氧化碳反应的化学方程式是___________ 。
(5)有同学提出质疑:“上述实验不足以证明有水存在时,过氧化钠跟二氧化碳发生了化学反应”,所以需要补充的实验操作是:取⑤中反应后的少量固体,___________ 。
(II)Na2O2具有强氧化性,H2具有还原性,该小组成员根据氧化还原反应的知识推测Na2O2与H2可能发生反应。为了验证此推测结果,该小组设计并进行如图实验。
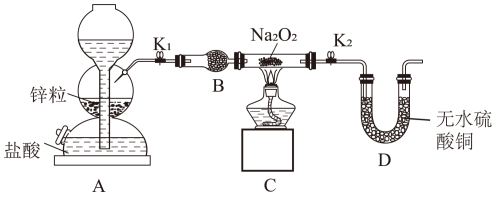
步骤1:按如图所示的装置组装仪器(图中夹持仪器已省略)并检查装置的气密性,然后装入药品。
步骤2:打开K1、K2,在产生的氢气流经装有Na2O2的硬质玻璃管的过程中,未观察到明显现象。
步骤3:进行必要的实验操作,淡黄色的粉末慢慢变成白色固体,无水硫酸铜未变蓝。
(6)B装置中所盛放的试剂是___________ ,其作用是___________ 。
(7)步骤3中的“必要操作”为打开K1、K2,______ (请按正确的顺序填入下列步骤的字母)。
A.加热至Na2O2逐渐熔化,反应一段时间
B.用小试管收集气体并检验其纯度
C.关闭K1
D.停止加热,充分冷却
(8)由上述实验可推出Na2O2与H2反应的化学方程式为___________ 。
(I)该小组设计如图实验装置,验证“二氧化碳与水接触时才能和过氧化钠反应”。

步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤2:打开弹簧夹K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(1)装置①中反应的离子方程式是
(2)装置②的作用是
(3)本实验预期现象是
(4)过氧化钠跟二氧化碳反应的化学方程式是
(5)有同学提出质疑:“上述实验不足以证明有水存在时,过氧化钠跟二氧化碳发生了化学反应”,所以需要补充的实验操作是:取⑤中反应后的少量固体,
(II)Na2O2具有强氧化性,H2具有还原性,该小组成员根据氧化还原反应的知识推测Na2O2与H2可能发生反应。为了验证此推测结果,该小组设计并进行如图实验。

步骤1:按如图所示的装置组装仪器(图中夹持仪器已省略)并检查装置的气密性,然后装入药品。
步骤2:打开K1、K2,在产生的氢气流经装有Na2O2的硬质玻璃管的过程中,未观察到明显现象。
步骤3:进行必要的实验操作,淡黄色的粉末慢慢变成白色固体,无水硫酸铜未变蓝。
(6)B装置中所盛放的试剂是
(7)步骤3中的“必要操作”为打开K1、K2,
A.加热至Na2O2逐渐熔化,反应一段时间
B.用小试管收集气体并检验其纯度
C.关闭K1
D.停止加热,充分冷却
(8)由上述实验可推出Na2O2与H2反应的化学方程式为
您最近一年使用:0次
名校
解题方法
8 . 某实验小组通过下图所示实验探究Na2O2与水的反应,下列说法不正确的是
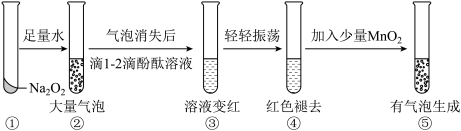

| A.②中的大量气泡主要成分是氧气 |
| B.③中溶液变红,说明有碱性物质生成 |
| C.④中现象可能是由于溶液中含有强漂白性物质造成的 |
| D.⑤中MnO2的主要作用是降低了水中氧气的溶解度 |
您最近一年使用:0次
2021-10-09更新
|
266次组卷
|
2卷引用:山西省长治市第二中学校2021-2022学年高一上学期期中考试化学试题
解题方法
9 . 同学们正在进行氢氧化钙与各种盐反应的探究实验。用A、B、C、D四支试管各取室温下等体积的氢氧化钙饱和溶液,再向A试管中滴加碳酸钠溶液、B试管中滴加氯化铜溶液、C试管中滴加氯化铵溶液、D试管中滴加氯化钠溶液,振荡。
(1)表达与交流:阳阳同学根据D试管中有没有看到现象,判断D试管无化学反应。你认为此判断的依据是否合理___________ (填”合理”或”不合理”),并解释其原因是___________ ;
(2)同学们对B试管中反应后得到的无色溶液,继续进行探究,他们选用两种不同类别的物质进行以下两个实验,请填写下列实验报告。
(1)表达与交流:阳阳同学根据D试管中有没有看到现象,判断D试管无化学反应。你认为此判断的依据是否合理
(2)同学们对B试管中反应后得到的无色溶液,继续进行探究,他们选用两种不同类别的物质进行以下两个实验,请填写下列实验报告。
| 实验内容 | 实验现象 | 实验结论 |
| 方案一:取少量滤液加入试管,向其中通入二氧化碳气体。 | ||
| 方案二:取少量滤液加入试管中,向其中 | 滤液中含有的两种溶质,分别是 |
您最近一年使用:0次
10 . 实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题:
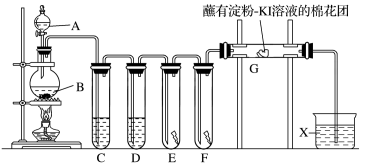
(1)A中盛有浓盐酸,B中盛有MnO2,写出反应的离子方程式:_______ 。
(2)E中为红色干布条,F中为红色湿布条,可观察到的现象是_______ 。对比E和F中现象的差异可得出的结论及解释是_______ 。
(3)试管C和D中试剂各为_______ 。
(4)装置G处发生反应的离子方程式为_______ 。
(5)用离子方程式表示试剂X的作用:_______ 。
(6)家庭中常用消毒液(主要成分为NaClO)与洁厕灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式:_______ 。

(1)A中盛有浓盐酸,B中盛有MnO2,写出反应的离子方程式:
(2)E中为红色干布条,F中为红色湿布条,可观察到的现象是
(3)试管C和D中试剂各为
(4)装置G处发生反应的离子方程式为
(5)用离子方程式表示试剂X的作用:
(6)家庭中常用消毒液(主要成分为NaClO)与洁厕灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
| 注意事项: 1.本品对棉织品有漂白脱色作用,对金属制品有腐蚀作用。 2.密封保存,请勿与洁厕灵同时使用。 3.保质期为一年 |
您最近一年使用:0次
2021-09-12更新
|
635次组卷
|
8卷引用:山西省稷山中学2021-2022学年高一上学期第二次月考化学试题
山西省稷山中学2021-2022学年高一上学期第二次月考化学试题河北省石家庄市第四中学2020-2021学年高一上学期期中考试化学试题广东省八校2021-2022学年高一上学期期中调研考试 化学试题 (已下线)期中测试卷03-【对点变式题】2021-2022学年高一化学上学期期中期末必考题精准练(人教版2019)广东省深圳市观澜中学2021-2022学年高一上学期期中考试化学试题甘肃省玉门市2021-2022学年高一 上学期“研课标读教材”期中学业质量监测试化学试题吉林省长春北师大附属学校2021-2022学年高一上学期期中考试化学试题(已下线)衔接点16 氯气的性质-2022年初升高化学无忧衔接?



