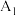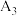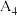1 . 研究硫及其化合物的应用价值对于社会发展意义重大。请回答以下问题。
(1)用下图装置制备纯净的SO2(同时生成一种正盐),请写出装置A中反应的离子方程式为___________ ,装置的连接顺序为: a → ___________ → e ( 按气流方向,用小写字母表示 ),C装置的仪器名称是___________ ,碱石灰的主要作用为___________ 。___________ ;
② 为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成。
上述方案中合理的是___________ (填Ⅰ、Ⅱ或Ⅲ);试管b中发生反应的离子方程式为___________ 。
(1)用下图装置制备纯净的SO2(同时生成一种正盐),请写出装置A中反应的离子方程式为
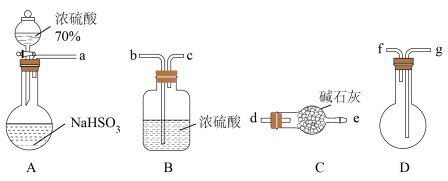
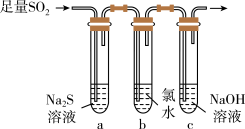
② 为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成。
上述方案中合理的是
您最近半年使用:0次
名校
解题方法
2 . 草酸是一种用途广泛的二元有机中强酸,某同学通过查阅资料设计了如图所示的装置(夹持仪器省略)制备一定量的草酸晶体( ),并验证其具有的某些性质。回答下列问题:
),并验证其具有的某些性质。回答下列问题:
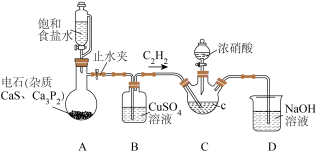
(1)装置B的作用是
 溶液检验有乙炔生成,则气体通过B后应先通入到盛有
溶液检验有乙炔生成,则气体通过B后应先通入到盛有 溶液中。
溶液中。(2)草酸在装置C中生成,反应的化学方程式为
(3)待反应结束后,从C中分离出草酸晶体,然后用0.1000 mol/L的酸性
 溶液进行滴定以测定其纯度。
溶液进行滴定以测定其纯度。①称量3.500 g草酸晶体配制100 mL溶液,下列配制操作中错误的是

②三次平行滴定实验中消耗 溶液的体积如表所示,其中第一次实验滴定后的液面位置如图所示:
溶液的体积如表所示,其中第一次实验滴定后的液面位置如图所示:
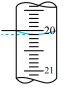
滴定次数 | 待测溶液体积/mL | 标准溶液的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液的体积/mL | ||
第一次 | 20.00 | 0.20 |
| |
第二次 | 20.00 | 2.56 | 28.40 | |
第三次 | 20.00 | 0.22 | 20.32 | |
则
您最近半年使用:0次
3 . 某小组设计如下实验装置制备漂白粉和氯酸钙并探究 的性质。
的性质。
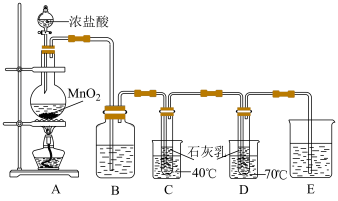
查阅资料:① 。
。
② 。
。
回答下列问题:
(1)B中试剂是______ 。
(2)写出A中反应的离子方程式:_______________________ 。
(3)C、D中常采用的加热方式为__________________ 。
(4)探究影响 漂白性的因素。
漂白性的因素。
①设计实验Ⅰ、Ⅱ的目的是_______________ 。
②实验测得: 。由此得出的结论是
。由此得出的结论是___________________ 。
③某同学根据相关原理预测: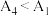 ,实验结果:
,实验结果: 。原理预测与实验结果相反的主要原因可能是
。原理预测与实验结果相反的主要原因可能是____________________________ 。
 的性质。
的性质。
查阅资料:①
 。
。②
 。
。回答下列问题:
(1)B中试剂是
(2)写出A中反应的离子方程式:
(3)C、D中常采用的加热方式为
(4)探究影响
 漂白性的因素。
漂白性的因素。实验 |
| 添加试剂 | 1%品红溶液 | 水浴温度 | 定溶液褪色时间/s |
I | 10mL | 2mL蒸馏水 | 2滴 | 25℃ |
|
Ⅱ | 10mL | 2mL | 2滴 | 25℃ |
|
Ⅲ | 10mL | 2mL | 2滴 | 25℃ |
|
Ⅳ | 10mL | 2mL蒸馏水 | 2滴 | 50℃ |
|
②实验测得:
 。由此得出的结论是
。由此得出的结论是③某同学根据相关原理预测:
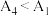 ,实验结果:
,实验结果: 。原理预测与实验结果相反的主要原因可能是
。原理预测与实验结果相反的主要原因可能是
您最近半年使用:0次
4 .  (四氢铝钠)是一种重要的还原剂和供氢剂,在有机合成中广泛应用。实验室制备原理为
(四氢铝钠)是一种重要的还原剂和供氢剂,在有机合成中广泛应用。实验室制备原理为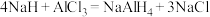 (在乙醚中进行,乙醚沸点:34.5℃)。某实验小组选择下列装置制备
(在乙醚中进行,乙醚沸点:34.5℃)。某实验小组选择下列装置制备 (装置可以重复使用,
(装置可以重复使用, 遇水蒸气剧烈反应)。下列叙述错误的是
遇水蒸气剧烈反应)。下列叙述错误的是
 (四氢铝钠)是一种重要的还原剂和供氢剂,在有机合成中广泛应用。实验室制备原理为
(四氢铝钠)是一种重要的还原剂和供氢剂,在有机合成中广泛应用。实验室制备原理为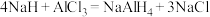 (在乙醚中进行,乙醚沸点:34.5℃)。某实验小组选择下列装置制备
(在乙醚中进行,乙醚沸点:34.5℃)。某实验小组选择下列装置制备 (装置可以重复使用,
(装置可以重复使用, 遇水蒸气剧烈反应)。下列叙述错误的是
遇水蒸气剧烈反应)。下列叙述错误的是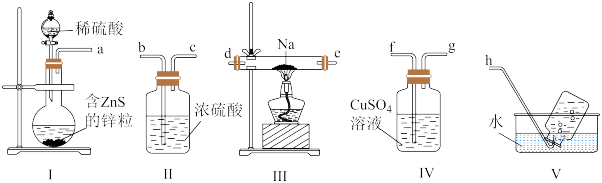
A.装置连接顺序为 |
| B.不能用浓硫酸、硝酸替代装置Ⅰ中的稀硫酸 |
| C.实验中观察到装置Ⅳ中产生黑色沉淀 |
D.实验室制备 的装置要保持干燥 的装置要保持干燥 |
您最近半年使用:0次
名校
解题方法
5 . 下图所示是某化学兴趣小组探究溶液中离子浓度与溶液导电的关系的装置图。
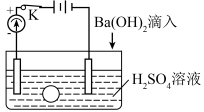
首先在水槽中加入200 mL 2 mol·L-1的H2SO4溶液,同时将一个表面光滑的小球放入溶液中,小球悬浮在溶液中央,闭合开关K,电流计发生偏转,然后再进行以下操作。请回答问题。
(1)向溶液中逐滴加入与H2SO4溶液密度相同的Ba(OH)2溶液至反应完全,观察到的现象是___________ ,反应的化学方程式是___________ ;
(2)将Ba(OH)2溶液换成浓度相同(假设密度也相同)的以下三种溶液(设反应后的体积为两溶液的体积和):
A.Ba(NO3)2 B.Na2SO4 C.Na2CO3
①滴加A的过程中,观察到的现象是___________ ,反应的化学方程式是___________ ;
②滴加B的过程中,小球的位置___________ ,电流计的偏转程度___________ ;
③滴加C的过程中,观察到的现象是___________ ,反应的化学方程式是___________ ,生成的Na2SO4的物质的量浓度为___________ 。

首先在水槽中加入200 mL 2 mol·L-1的H2SO4溶液,同时将一个表面光滑的小球放入溶液中,小球悬浮在溶液中央,闭合开关K,电流计发生偏转,然后再进行以下操作。请回答问题。
(1)向溶液中逐滴加入与H2SO4溶液密度相同的Ba(OH)2溶液至反应完全,观察到的现象是
(2)将Ba(OH)2溶液换成浓度相同(假设密度也相同)的以下三种溶液(设反应后的体积为两溶液的体积和):
A.Ba(NO3)2 B.Na2SO4 C.Na2CO3
①滴加A的过程中,观察到的现象是
②滴加B的过程中,小球的位置
③滴加C的过程中,观察到的现象是
您最近半年使用:0次
名校
解题方法
6 . 某同学做同周期元素性质递变实验时,自己设计了一套实验方案,并记录了有关实验现象如下表。
(1)请从表中实验现象(Ⅱ)中分别选出(I)对应的现象,将其序号(A、B、C……)填入(Ⅲ)中,并写出相应的化学方程式:
(2)通过以上实验分析同周期元素的符号是___________ ;
(3)从实验结果可以得出的结论是___________ ;
(4)从结构理论上简单说明具有上述结论的原因___________ 。
(1)请从表中实验现象(Ⅱ)中分别选出(I)对应的现象,将其序号(A、B、C……)填入(Ⅲ)中,并写出相应的化学方程式:
| 实验方案(I) | 实验现象(Ⅱ) | 答案(Ⅲ) | ||
| I | Ⅱ | 化学方程式 | ||
| 1.用砂纸擦过的镁带与沸水反应,再向反应液中滴加酚酞试液 | A.浮于水面,熔成小球,在水面上不定向移动,随之消失,溶液变成红色 | 1 | ||
| 2.钠与滴有酚酞试液的冷水反应 | B.产生大量可在空气中燃烧的气体,溶液变成浅红色 | 2 | ||
3.镁带与2 的盐酸反应 的盐酸反应 | C.反应不十分剧烈,产生的气体可在空气中燃烧 | 3 | ||
4.铝与2 的盐酸反应 的盐酸反应 | D.剧烈反应,产生的气体可在空气中燃烧 | 4 | ||
(3)从实验结果可以得出的结论是
(4)从结构理论上简单说明具有上述结论的原因
您最近半年使用:0次
名校
解题方法
7 . 某研究小组为了探究NaClO溶液的性质,设计了下列实验,并记录实验现象。
则以下判断错误的是
| 实验装置 | 实验序号 | 滴管试剂 | 试管试剂 | 实验现象 |
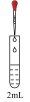 | ① |  NaClO溶液 NaClO溶液 | 饱和 溶液 溶液 | 产生白色沉淀,继而转化为棕黑色沉淀 |
| ② |  溶液 溶液 | 光照管壁有无色气泡产生 | ||
| ③ |   酸性溶液和KSCN溶液 酸性溶液和KSCN溶液 | 溶液变红 | ||
| ④ |   溶液 溶液 | 产生白色沉淀 |
A.实验①:发生的反应为 |
B.实验②:无色气体为 |
C.实验③:还原性强弱顺序: |
D.实验④: 与 与 的水解相互促进 的水解相互促进 |
您最近半年使用:0次
名校
解题方法
8 . 学习小组在实验室中利用下图所示装置制备 ,并进行相关性质的探究。回答下列问题:
,并进行相关性质的探究。回答下列问题:

(1)仪器Q的名称为______ ;装置b的作用是______ 。
(2)实验方案中出现的图标 和
和 ,前者要求实验者
,前者要求实验者______ (填防护措施),后者提示本实验应在实验室的______ 中进行(填设施名称),
(3)装置e中发生反应的离子方程式为______ 。
(4)实验开始后,发现装置d中的溶液迅速变黄,继续通入 ,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应:
,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应: 。
。
实验探究: 在
在 溶液体系中的反应产物。
溶液体系中的反应产物。
有同学提出上述可逆反应生成的 可与
可与 发生反应:
发生反应: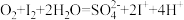 ,为进一步探究体系中的产物,完成下列实验方案:
,为进一步探究体系中的产物,完成下列实验方案:
综上可知, 在
在 溶液中发生了歧化反应(
溶液中发生了歧化反应( 是催化剂,只有硫元素变价),其反应的离子方程式为
是催化剂,只有硫元素变价),其反应的离子方程式为______ 。
 ,并进行相关性质的探究。回答下列问题:
,并进行相关性质的探究。回答下列问题:
(1)仪器Q的名称为
(2)实验方案中出现的图标
 和
和 ,前者要求实验者
,前者要求实验者(3)装置e中发生反应的离子方程式为
(4)实验开始后,发现装置d中的溶液迅速变黄,继续通入
 ,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应:
,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应: 。
。实验探究:
 在
在 溶液体系中的反应产物。
溶液体系中的反应产物。有同学提出上述可逆反应生成的
 可与
可与 发生反应:
发生反应: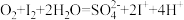 ,为进一步探究体系中的产物,完成下列实验方案:
,为进一步探究体系中的产物,完成下列实验方案:| 方案 | 操作 | 预期现象 | 结论 |
| i | 取适量装置中浊液,向其中滴加几滴 | 无明显变化 | 浊液中无 |
| ii | 将装置d中浊液进行分离 | 得淡黄色固体和澄清溶液 | |
| 取适量分离后的澄清溶液于试管中, | 产生白色沉淀 | 产物有 |
 在
在 溶液中发生了歧化反应(
溶液中发生了歧化反应( 是催化剂,只有硫元素变价),其反应的离子方程式为
是催化剂,只有硫元素变价),其反应的离子方程式为
您最近半年使用:0次
9 . 实验室中利用如图所示装置(夹持装置略)制备 并进行实验探究。
并进行实验探究。
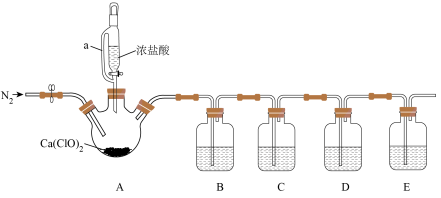
已知:C中试剂为滴有KSCN溶液的 溶液;D中试剂为
溶液;D中试剂为 的饱和溶液。
的饱和溶液。
回答下列问题:
(1)仪器a的名称为___________ 。
(2)写出装置A中生成 的化学方程式:
的化学方程式:___________ 。
(3)实验中观察到C中溶液先变红后褪色。
①溶液变红的原因为___________ 。
②溶液褪色的原因可能是___________ ,设计实验验证该猜想:___________ 。
(4)反应一段时间后,取D中适量溶液,加入 溶液,有白色沉淀生成。该实验能否证明氯气具有氧化性
溶液,有白色沉淀生成。该实验能否证明氯气具有氧化性___________ (填“能”或“不能”),若能,说明理由;若不能,请设计实验证明:___________ 。
 并进行实验探究。
并进行实验探究。
已知:C中试剂为滴有KSCN溶液的
 溶液;D中试剂为
溶液;D中试剂为 的饱和溶液。
的饱和溶液。回答下列问题:
(1)仪器a的名称为
(2)写出装置A中生成
 的化学方程式:
的化学方程式:(3)实验中观察到C中溶液先变红后褪色。
①溶液变红的原因为
②溶液褪色的原因可能是
(4)反应一段时间后,取D中适量溶液,加入
 溶液,有白色沉淀生成。该实验能否证明氯气具有氧化性
溶液,有白色沉淀生成。该实验能否证明氯气具有氧化性
您最近半年使用:0次
10 . 实验室用如下装置制取干燥纯净的氯气,并用氯气进行实验。回答下列问题:
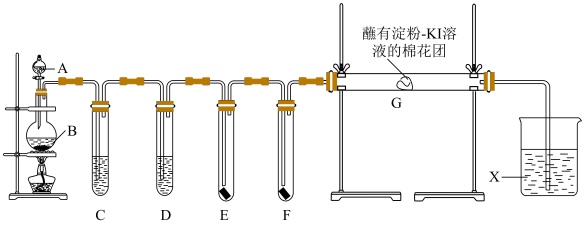
(1)装置连接完成后必须进行的操作是________ 。
(2)实验室制氯气的反应方程式为 ,其中参加反应的还原剂与氧化剂的数目之比为
,其中参加反应的还原剂与氧化剂的数目之比为_____ 。
(3)试管D中试剂为_______ 。
(4)E中为红色干布条,F中为红色湿布条,可观察到的现象是_______ 。对比E和F中现象的差异可得出的结论_______ 。
(5)装置G处棉花团变蓝,写出发生反应的化学方程式_______ (提示:淀粉遇I2变蓝)。

(1)装置连接完成后必须进行的操作是
(2)实验室制氯气的反应方程式为
 ,其中参加反应的还原剂与氧化剂的数目之比为
,其中参加反应的还原剂与氧化剂的数目之比为(3)试管D中试剂为
(4)E中为红色干布条,F中为红色湿布条,可观察到的现象是
(5)装置G处棉花团变蓝,写出发生反应的化学方程式
您最近半年使用:0次