1 . 某兴趣小组利用如下图装置探究Cl2的性质。
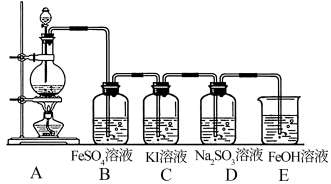
回答下列问题:
(1)A装置制取氯气时,在烧瓶里加入一定量的漂白粉,通过___________ (填写仪器名称)向烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在A与B之间安装盛有___________ (填写下列编号字母)的净化装置。
A、碱石灰 B、饱和食盐水 C、浓硫酸 D、饱和碳酸氢钠溶液
(2)B溶液发生反应的离子方程式_____
(3)D中SO 被Cl2氧化生成的微粒是
被Cl2氧化生成的微粒是_____
A、SO B、S C、SO2 D、H2SO4
B、S C、SO2 D、H2SO4
(4)C中现象是无色溶液变成棕黄色后又褪色。这是因为发生如下2个反应:
①___________ ;
②I2+Cl2+H2O=HIO3+___________ (不必配平)。
(5)E中NaOH的作用是___________ 。为证明E溶液中存在ClO-,取少量E中溶液放入试管中,滴加稀H2SO4至溶液呈酸性,再加入淀粉KI溶液,预期现象是______ ,该反应的氧化产物是___________ (写化学式)

回答下列问题:
(1)A装置制取氯气时,在烧瓶里加入一定量的漂白粉,通过
A、碱石灰 B、饱和食盐水 C、浓硫酸 D、饱和碳酸氢钠溶液
(2)B溶液发生反应的离子方程式
(3)D中SO
 被Cl2氧化生成的微粒是
被Cl2氧化生成的微粒是A、SO
 B、S C、SO2 D、H2SO4
B、S C、SO2 D、H2SO4
(4)C中现象是无色溶液变成棕黄色后又褪色。这是因为发生如下2个反应:
①
②I2+Cl2+H2O=HIO3+
(5)E中NaOH的作用是
您最近一年使用:0次
名校
解题方法
2 . 化学实验是科学探究过程中的一种重要方法,掌握化学实验的基本操作和物质的制备、转化及性质的探究尤为重要,请结合所学化学实验知识回答以下问题。某化学课外活动小组为了验证元素化学性质递变规律,进行如下实验探究。
探究:验证氯元素的非金属性比硫元素的非金属性强,设计如下实验:
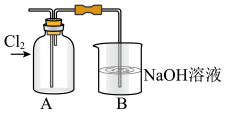
(1)装置A中盛放的试剂是____ (填选项),化学反应方程式是___ 。
A.Na2SO3溶液 B.Na2S溶液 C.Na2SO4溶液
(2)下列不能用于验证氯元素比硫元素非金属性强的依据为______ (填选项)。
①HCl的溶解度比H2S大 ②HCl的酸性比H2S强 ③HCl的稳定性比H2S大④HCl的还原性比H2S弱⑤HClO4的酸性比H2SO4强 ⑥还原性:Cl-<S2- ⑦Cl2能与H2S反应生成S ⑧在周期表中Cl处于S同周期的右侧
(3)若要验证非金属性:Cl>I,装置A中加入淀粉碘化钾混合溶液,观察到装置A中溶液_______ 的现象,即可证明。用元素周期律理论解释非金属性Cl>I的原因:_________ 。
探究:验证氯元素的非金属性比硫元素的非金属性强,设计如下实验:

(1)装置A中盛放的试剂是
A.Na2SO3溶液 B.Na2S溶液 C.Na2SO4溶液
(2)下列不能用于验证氯元素比硫元素非金属性强的依据为
①HCl的溶解度比H2S大 ②HCl的酸性比H2S强 ③HCl的稳定性比H2S大④HCl的还原性比H2S弱⑤HClO4的酸性比H2SO4强 ⑥还原性:Cl-<S2- ⑦Cl2能与H2S反应生成S ⑧在周期表中Cl处于S同周期的右侧
(3)若要验证非金属性:Cl>I,装置A中加入淀粉碘化钾混合溶液,观察到装置A中溶液
您最近一年使用:0次
2020-01-11更新
|
318次组卷
|
4卷引用:河南省新乡市原阳县第三高级中学2020-2021学年高一下学期第一次月考化学试题
解题方法
3 . 实验室用无水乙酸钠和碱石灰混合制甲烷:CH3COONa+NaOH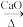 CH4↑+Na2CO3,为了探究甲烷的化学性质,进行了以下实验,B装置中的试剂为溴水或酸性KMnO4溶液,一段时间后,无水硫酸铜变蓝,澄清石灰水变浑浊。所需装置如图(部分夹持仪器已略去):
CH4↑+Na2CO3,为了探究甲烷的化学性质,进行了以下实验,B装置中的试剂为溴水或酸性KMnO4溶液,一段时间后,无水硫酸铜变蓝,澄清石灰水变浑浊。所需装置如图(部分夹持仪器已略去):
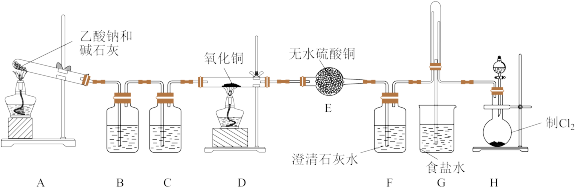
(1)写出H装置中反应的离子方程式:______________________ 。
(2)C装置中的试剂为___________ 。
(3)实验测得消耗的CH4和CuO的质量比为1∶20,则D中硬质玻璃管内发生反应的化学方程式为______
(4)实验开始前,先在G装置的大试管上套上黑色纸套,反应结束后,取下黑色纸套,使收集满气体的试管置于光亮处缓慢反应一段时间,观察到的现象有:
①试管中有少量白雾;
②导管内液面上升
③_______
④_______
(5)有关该实验的说法,正确的是______ (填字母)。
A.若B装置中的试剂是溴水,溴水无明显变化,说明CH4不能与卤素单质反应
B.若B中是酸性高锰酸钾溶液,溶液无明显变化,说明通常情况下甲烷难以被强氧化剂氧化
C.硬质玻璃管中的黑色固体粉末变红,说明甲烷具有氧化性
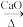 CH4↑+Na2CO3,为了探究甲烷的化学性质,进行了以下实验,B装置中的试剂为溴水或酸性KMnO4溶液,一段时间后,无水硫酸铜变蓝,澄清石灰水变浑浊。所需装置如图(部分夹持仪器已略去):
CH4↑+Na2CO3,为了探究甲烷的化学性质,进行了以下实验,B装置中的试剂为溴水或酸性KMnO4溶液,一段时间后,无水硫酸铜变蓝,澄清石灰水变浑浊。所需装置如图(部分夹持仪器已略去):
(1)写出H装置中反应的离子方程式:
(2)C装置中的试剂为
(3)实验测得消耗的CH4和CuO的质量比为1∶20,则D中硬质玻璃管内发生反应的化学方程式为
(4)实验开始前,先在G装置的大试管上套上黑色纸套,反应结束后,取下黑色纸套,使收集满气体的试管置于光亮处缓慢反应一段时间,观察到的现象有:
①试管中有少量白雾;
②导管内液面上升
③
④
(5)有关该实验的说法,正确的是
A.若B装置中的试剂是溴水,溴水无明显变化,说明CH4不能与卤素单质反应
B.若B中是酸性高锰酸钾溶液,溶液无明显变化,说明通常情况下甲烷难以被强氧化剂氧化
C.硬质玻璃管中的黑色固体粉末变红,说明甲烷具有氧化性
您最近一年使用:0次



