14-15高一上·安徽淮北·期末
名校
解题方法
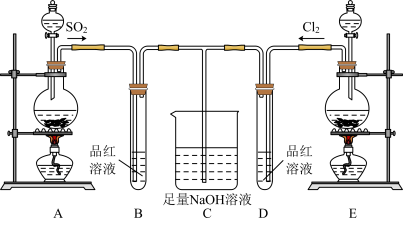
1 . 某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下实验装置:__ 。
(2)实验室可用装置E通过MnO2和浓盐酸反应制备Cl2,若有6molHCl参加反应,则转移电子的总数为___ 。
(3)反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象分别是:B__ ,D___ 。停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别是:B__ ,D__ 。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后漂白性肯定会更强。他们将制得的SO2和Cl2按物质的量之比为1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析产生该现象的原因:__ (用化学方程式表示)。
(2)实验室可用装置E通过MnO2和浓盐酸反应制备Cl2,若有6molHCl参加反应,则转移电子的总数为
(3)反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象分别是:B
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后漂白性肯定会更强。他们将制得的SO2和Cl2按物质的量之比为1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析产生该现象的原因:
您最近一年使用:0次
2020-09-16更新
|
154次组卷
|
8卷引用:2014-2015甘肃省白银市会宁县五中高一上学期期末化学试卷
2014-2015甘肃省白银市会宁县五中高一上学期期末化学试卷(已下线)2013-2014学年安徽省濉溪县高一上学期期末考试化学试卷(已下线)2013-2014学年河南省平顶山市高一第一学期期末调研考试化学试卷【全国百强校】西藏自治区拉萨中学2017-2018学年高一下学期期中考试化学试题吉林省公主岭市范家屯镇第一中学2019-2020学年高一上学期期末考试化学试题鲁科版(2019)高一必修第一册第三章易错疑难集训(二)高一必修第一册(苏教2019版)专题4 第一单元 含硫化合物的性质 易错疑难集训陕西省西安市选课分科摸底考2023-2024学年高一下学期4月月考化学试题
2 . 某研究小组制备氯气并对产生氯气的条件进行探究。
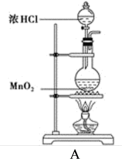
(1)装置A中用MnO2与浓盐酸反应制取Cl2,利用了浓HCl的_______ (填“氧化性”或“还原性”)。
(2)A中产生的气体不纯,含有的杂质可能是_______ 。(填写化学式)
(3)装置B用于吸收多余的Cl2,B中发生反应的离子方程式是_______ 。
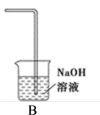
(4)该小组欲研究盐酸的浓度对制Cl2的影响,设计实验进行探究:
①已知MnO2呈弱碱性。Ⅰ中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,化学方程式是_______ 。
②Ⅱ中发生了分解反应,反应的化学方程式是_______ 。
③Ⅲ中无明显现象的原因,可能是c(H+)或c(Cl-)较低,设计实验Ⅳ进行探究:
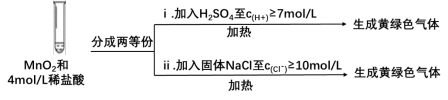
将实验Ⅲ、Ⅳ作对比,得出的结论是_______ ;
将ⅰ、ⅱ作对比,得出的结论是_______ 。

(1)装置A中用MnO2与浓盐酸反应制取Cl2,利用了浓HCl的
(2)A中产生的气体不纯,含有的杂质可能是
(3)装置B用于吸收多余的Cl2,B中发生反应的离子方程式是

(4)该小组欲研究盐酸的浓度对制Cl2的影响,设计实验进行探究:
| 实验 | 操作 | 现象 |
| Ⅰ | 常温下将MnO2和12mol/L浓盐酸混合 | 溶液呈浅棕色,略有刺激性气味 |
| Ⅱ | 将Ⅰ中混合物过滤,加热滤液 | 生成大量黄绿色气体 |
| Ⅲ | 加热MnO2和4mol/L稀盐酸混合物 | 无明显现象 |
②Ⅱ中发生了分解反应,反应的化学方程式是
③Ⅲ中无明显现象的原因,可能是c(H+)或c(Cl-)较低,设计实验Ⅳ进行探究:

将实验Ⅲ、Ⅳ作对比,得出的结论是
将ⅰ、ⅱ作对比,得出的结论是
您最近一年使用:0次
3 . 利用下列有关实验装置进行相关实验,不能达到实验目的的是


| A.用图甲所示装置检验金属钠与水反应的热效应 |
B.用图乙所示装置制取并收集干燥纯净的 |
C.用图丙所示装置可以比较 、 、 、S的氧化性 、S的氧化性 |
| D.用图丁所示装置检验氨气的水溶性 |
您最近一年使用:0次
2022-06-03更新
|
364次组卷
|
5卷引用:甘肃省庆阳市2021-2022学年高一下学期期末考试化学试题
4 . 某化学学习小组为了探究铁质材料碳素钢(仅含有C和Fe)和浓硫酸反应的气体产物,利用下列装置(部分夹持仪器已省略)进行了如下实验探究活动:
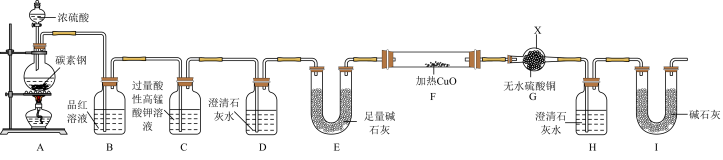
回答下列问题:
(1)仪器X的名称为___________ 。
(2)能证明实验生成 的实验现象为
的实验现象为___________ ;装置C的作用为___________ 。
(3)实验过程中观察到G中无水硫酸铜由白色变成蓝色,说明(填化学式)与 反应生成了
反应生成了 ,F中发生反应的化学方程式为
,F中发生反应的化学方程式为___________ ;产生该气体(F中的反应物)的原因为___________ 。
(4)若装置D中澄清石灰水变浑浊,装置H中澄清石灰水未变浑浊,说明生成了___________ (填“ ”或“CO”);若铁质材料中碳与浓硫酸反应生成的气体的物质的量之比为1:2,则该反应的化学方程式为
”或“CO”);若铁质材料中碳与浓硫酸反应生成的气体的物质的量之比为1:2,则该反应的化学方程式为___________ 。装置H后增加装置I的目的是___________ 。

回答下列问题:
(1)仪器X的名称为
(2)能证明实验生成
 的实验现象为
的实验现象为(3)实验过程中观察到G中无水硫酸铜由白色变成蓝色,说明(填化学式)与
 反应生成了
反应生成了 ,F中发生反应的化学方程式为
,F中发生反应的化学方程式为(4)若装置D中澄清石灰水变浑浊,装置H中澄清石灰水未变浑浊,说明生成了
 ”或“CO”);若铁质材料中碳与浓硫酸反应生成的气体的物质的量之比为1:2,则该反应的化学方程式为
”或“CO”);若铁质材料中碳与浓硫酸反应生成的气体的物质的量之比为1:2,则该反应的化学方程式为
您最近一年使用:0次
5 . 化学小组同学设计如下实验验证氯气的部分性质,并探究氯水的成分和性质。

回答下列问题:
(1)装置A中发生反应的化学方程式为_______ 。
(2)验证干燥的氯气没有漂白性的现象为_______ 。
(3)装置F的作用是_______ 。
(4)研究新制氯水的成分和性质。
以装置E的溶液进行下列实验:
资料:淀粉的特征反应——遇 变蓝色;
变蓝色; 。
。
①根据实验1可知,氧化性:
_______ (填“>”或“<”) 。
。
②实验2中证明溶液中含有_______ (填含氯微粒的分子式)。
③若用实验3证明氯水中含有氯离子,则实验操作为_______ 。
(5)同学们发现久置的氯水会失去漂白性。为探究氯水失效的原因进行实验:用强光照射盛有氯水的密闭细口瓶,并用传感器测定数据,得到如图曲线。两图中曲线变化的原因是_______ (用化学方程式表示);保存氯水的方法为_______ 。


回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)验证干燥的氯气没有漂白性的现象为
(3)装置F的作用是
(4)研究新制氯水的成分和性质。
以装置E的溶液进行下列实验:
| 实验序号 | 实验1 | 实验2 | 实验3 |
| 实验操作 |  | 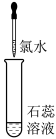 | |
| 实验现象 | 溶液变蓝 | 石蕊溶液先变红,后褪色 | 有白色沉淀生成 |
 变蓝色;
变蓝色; 。
。①根据实验1可知,氧化性:

 。
。②实验2中证明溶液中含有
③若用实验3证明氯水中含有氯离子,则实验操作为
(5)同学们发现久置的氯水会失去漂白性。为探究氯水失效的原因进行实验:用强光照射盛有氯水的密闭细口瓶,并用传感器测定数据,得到如图曲线。两图中曲线变化的原因是

您最近一年使用:0次
2022-11-15更新
|
99次组卷
|
2卷引用:甘肃省武威市民勤县第一中学2022-2023学年高一上学期期中考试化学试卷
名校
6 . 某实验小组对Cu与 的反应进行研究,实验如下。
的反应进行研究,实验如下。

(1)试管①中反应的化学方程式是_______ 。
(2)已知绿色是棕色和蓝色的混合色,绿色溶液变蓝是因为 与水生成了
与水生成了 和
和_______ 。
(3)对比③和⑤中现象,为探究③中立即产生气泡的原因,实验小组提出如下假设,并设计实验验证。
假设1: 对该反应有催化作用。
对该反应有催化作用。
假设2: 对该反应有催化作用。
对该反应有催化作用。
假设3: 对该反应有催化作用。
对该反应有催化作用。
(4)得出实验结论后,有同学认为还应补充对比实验:向④溶液加入几滴较浓的硝酸后加入铜片。补充该实验的目的是_______ 。
(5)某工厂用硝酸溶解废铜屑制备 ,为避免
,为避免 的生成,实验小组提出还应加入
的生成,实验小组提出还应加入 溶液,反应的离子方程式为
溶液,反应的离子方程式为_______ ;消耗含铜元素80%的废铜屑240 kg固体时,得到653.4 kg产品,产率为_______ 。
 的反应进行研究,实验如下。
的反应进行研究,实验如下。
(1)试管①中反应的化学方程式是
(2)已知绿色是棕色和蓝色的混合色,绿色溶液变蓝是因为
 与水生成了
与水生成了 和
和(3)对比③和⑤中现象,为探究③中立即产生气泡的原因,实验小组提出如下假设,并设计实验验证。
假设1:
 对该反应有催化作用。
对该反应有催化作用。假设2:
 对该反应有催化作用。
对该反应有催化作用。假设3:
 对该反应有催化作用。
对该反应有催化作用。| 序号 | 实验操作 | 实验现象 | 结论 |
| 3 | 向④中溶液加入少量 | 溶液蓝色加深,无其他明显现象 | 假设1不成立 |
| 4 | 铜片表面立即产生气泡 | 假设2成立 | |
| 5 | 向②中溶液通入少量 | 无明显变化 | |
| 6 | 向④中溶液加入少量 | 铜片表面立即产生气泡 | 假设3成立 |
(5)某工厂用硝酸溶解废铜屑制备
 ,为避免
,为避免 的生成,实验小组提出还应加入
的生成,实验小组提出还应加入 溶液,反应的离子方程式为
溶液,反应的离子方程式为
您最近一年使用:0次
2023-05-04更新
|
601次组卷
|
10卷引用:甘肃省平凉市静宁县文萃中学2023-2024学年高三上学期第三次模拟考试化学试题
甘肃省平凉市静宁县文萃中学2023-2024学年高三上学期第三次模拟考试化学试题福建省龙岩市一级校2022-2023学年高三上学期期末联考化学试题(已下线)考点11 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)物质含量的测定辽宁省部分县级重点中学2023-2024学年高三上学期11月期中考试化学试题广东省佛山市2023-2024学年高三上学期12月月考化学试题广东省深圳外国语学校(集团)高中部 2023-2024学年高三上学期第四次月考化学试题河北省部分学校2023-2024学年上学期高三七调考试化学试题广东省深圳市福田区福田中学2023-2024学年高三上学期12月月考化学考试(已下线)T12-实验综合题
解题方法
7 . 已知生石灰与水反应生成 并放出热量,实验室利用此原理向生石灰中滴加浓氨水制取氨气并探究其性质(部分夹持装置已略去)。
并放出热量,实验室利用此原理向生石灰中滴加浓氨水制取氨气并探究其性质(部分夹持装置已略去)。
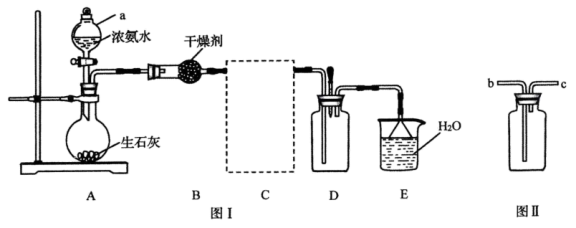
回答下列问题:
(1)仪器 的名称为
的名称为____________ ;装置 中的干燥剂为
中的干燥剂为___________ 。
(2)装置 如图Ⅱ所示,用于收集氨气,装置
如图Ⅱ所示,用于收集氨气,装置 应连接
应连接__________ (填“ ”或“
”或“ ”)。
”)。
(3)装置 中倒置漏斗的作用为
中倒置漏斗的作用为___________ 。
(4)实验进行一段时间后,挤压装置 中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象为
中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象为___________ ;向装置 中滴入1~2滴酚酞溶液,装置
中滴入1~2滴酚酞溶液,装置 中溶液颜色为
中溶液颜色为____________ 。
 并放出热量,实验室利用此原理向生石灰中滴加浓氨水制取氨气并探究其性质(部分夹持装置已略去)。
并放出热量,实验室利用此原理向生石灰中滴加浓氨水制取氨气并探究其性质(部分夹持装置已略去)。
回答下列问题:
(1)仪器
 的名称为
的名称为 中的干燥剂为
中的干燥剂为(2)装置
 如图Ⅱ所示,用于收集氨气,装置
如图Ⅱ所示,用于收集氨气,装置 应连接
应连接 ”或“
”或“ ”)。
”)。(3)装置
 中倒置漏斗的作用为
中倒置漏斗的作用为(4)实验进行一段时间后,挤压装置
 中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象为
中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象为 中滴入1~2滴酚酞溶液,装置
中滴入1~2滴酚酞溶液,装置 中溶液颜色为
中溶液颜色为
您最近一年使用:0次
2021-10-09更新
|
570次组卷
|
3卷引用:甘肃省白银市白银区大成学校2021-2022学年高一下学期6月月考化学试题
解题方法
8 . 按如图所示装置进行实验验证有关钠化合物的性质,填写有关现象及化学方程式。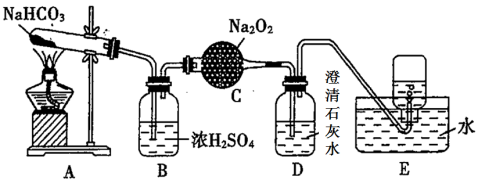
(1)A发生反应的化学方程式为_____________________________________ 。
(2)B装置的作用是________________________________________ 。
(3)C中发生反应的化学方程式为___________________________________ 。
(4)D中可能产生的现象是_________________________________________ 。
(5)若D中盛装的是NaOH溶液,则E中集气瓶内收到的气体是________ (填化学式,不考虑水蒸气)。

(1)A发生反应的化学方程式为
(2)B装置的作用是
(3)C中发生反应的化学方程式为
(4)D中可能产生的现象是
(5)若D中盛装的是NaOH溶液,则E中集气瓶内收到的气体是
您最近一年使用:0次
名校
解题方法
9 . 乙炔是一种无色无味的气体,微溶于水,易溶于有机溶剂。实验室常用如图所示装置制取乙炔,并验证乙炔的性质。完成实验,观察实验现象,回答下列问题:
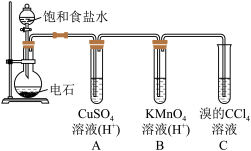
(1)写出电石(碳化钙CaC2)与水反应,制取乙炔的化学方程式_________________
(2)用饱和食盐水代替蒸馏水的目的是__________________
(3)装置A的作用是_______________ ,装置B中的现象是__________________
(4)如果要进行乙炔的可燃性实验,首先应该__________________ 。
(5)若乙炔加氢后得到乙烷,则乙烷在光照条件下与氯气反应,生成的一氯代烷最多有__________ 种。
(6)若称取a g CaC2,反应完全后,将生成的乙炔全部通入足量溴的CCl4溶液中溶液增重b g,则CaC2的纯度为___________ (用百分数表示)

(1)写出电石(碳化钙CaC2)与水反应,制取乙炔的化学方程式
(2)用饱和食盐水代替蒸馏水的目的是
(3)装置A的作用是
(4)如果要进行乙炔的可燃性实验,首先应该
(5)若乙炔加氢后得到乙烷,则乙烷在光照条件下与氯气反应,生成的一氯代烷最多有
(6)若称取a g CaC2,反应完全后,将生成的乙炔全部通入足量溴的CCl4溶液中溶液增重b g,则CaC2的纯度为
您最近一年使用:0次
2020-06-04更新
|
627次组卷
|
3卷引用:甘肃省静宁县第一中学2019-2020学年高二下学期期中考试(第二次月考)化学试题(实验班)
甘肃省静宁县第一中学2019-2020学年高二下学期期中考试(第二次月考)化学试题(实验班)西藏自治区山南市第二高级中学2019-2020学年高二下学期月考化学试题(已下线)【教材实验热点】18 乙炔的实验室制取及性质探究
10 . 如图所示是实验室制取SO2并验证SO2的某些性质的装置图。试回答:
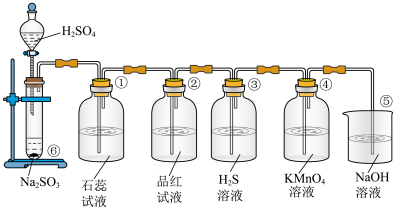
(1)①中的实验现象为石蕊试液___ ,此实验证明SO2是______ 气体。
(2)②中的品红溶液__________ ,证明SO2有________ 。
(3)③中的实验现象是____________ ,证明SO2有______ 性。
(4)④中的实验现象是____________ ,证明SO2有______ 性。
(5)⑤的作用是___________ 。

(1)①中的实验现象为石蕊试液
(2)②中的品红溶液
(3)③中的实验现象是
(4)④中的实验现象是
(5)⑤的作用是
您最近一年使用:0次



