名校
1 . 某小组取一定质量的硫酸亚铁固体,利用下图装置进行实验。
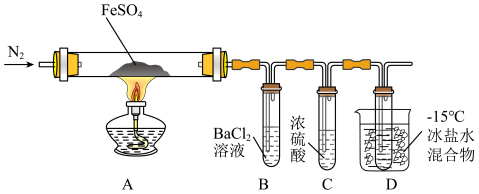
实验过程及现象如下:
①通一段时间氮气后加热,A中固体变为红棕色,B中有白色沉淀,D试管中有无色液体;
②用带火星的木条靠近装置D的导管口,木条复燃;
③充分反应后停止加热,冷却后取A中固体,加盐酸,固体溶解,溶液呈黄色;
④将③所得溶液滴入D试管中,溶液变为浅绿色。
已知:SO2熔点-72℃,沸点-10℃;SO3熔点16.8℃,沸点44.8℃。
(1)实验③反应的离子方程式是__________ 。
(2)分解过程除产生使木条复燃的气体外,仅由A中固体颜色变化推测,还一定有______ 气体,依据是_________ 。
(3)实验④反应的离子方程式是_________ 。

实验过程及现象如下:
①通一段时间氮气后加热,A中固体变为红棕色,B中有白色沉淀,D试管中有无色液体;
②用带火星的木条靠近装置D的导管口,木条复燃;
③充分反应后停止加热,冷却后取A中固体,加盐酸,固体溶解,溶液呈黄色;
④将③所得溶液滴入D试管中,溶液变为浅绿色。
已知:SO2熔点-72℃,沸点-10℃;SO3熔点16.8℃,沸点44.8℃。
(1)实验③反应的离子方程式是
(2)分解过程除产生使木条复燃的气体外,仅由A中固体颜色变化推测,还一定有
(3)实验④反应的离子方程式是
您最近一年使用:0次
2020-01-28更新
|
45次组卷
|
3卷引用:鲁教版高中化学必修1第二章《元素与物质世界》测试卷1
2 . 含氯消毒剂是指溶于水产生具有杀死微生物活性的次氯酸的消毒剂,无机含氯消毒剂包括液氯、次氯酸钠、次氯酸钙等。
(1)下列叙述正确的是____________ (填字母)。
A.液氯和新制氯水都是游离态氯,都能作杀菌消毒剂
B.因为Cl2能与水反应,所以自来水中不存在游离态氯
C.溶液中H+的浓度越大,次氯酸钠的消毒效果越好
D.含氯消毒剂应密封保存
(2)漂白粉是一种优良高效、价格低廉的常用杀菌消毒剂。实验室中有一瓶密封不严的漂白粉,其中肯定存在CaCl2,设计实验,探究该漂白粉中可能存在的其他物质。
[提出合理假设]
假设1:该漂白粉未变质,只含有__________ ;
假设2:该漂白粉全部变质,只含有__________ ;
假设3:该漂白粉部分变质,既含有Ca(ClO)2又含有CaCO3。
[设计实验方案]
限选用的仪器和药品:试管、胶头滴管、带导管的单孔塞、蒸馏水、自来水、1 mol·L-1稀盐酸、品红溶液、新制澄清石灰水(提示:不必检验Ca2+和Cl-,表格可以不填满)。
(1)下列叙述正确的是
A.液氯和新制氯水都是游离态氯,都能作杀菌消毒剂
B.因为Cl2能与水反应,所以自来水中不存在游离态氯
C.溶液中H+的浓度越大,次氯酸钠的消毒效果越好
D.含氯消毒剂应密封保存
(2)漂白粉是一种优良高效、价格低廉的常用杀菌消毒剂。实验室中有一瓶密封不严的漂白粉,其中肯定存在CaCl2,设计实验,探究该漂白粉中可能存在的其他物质。
[提出合理假设]
假设1:该漂白粉未变质,只含有
假设2:该漂白粉全部变质,只含有
假设3:该漂白粉部分变质,既含有Ca(ClO)2又含有CaCO3。
[设计实验方案]
限选用的仪器和药品:试管、胶头滴管、带导管的单孔塞、蒸馏水、自来水、1 mol·L-1稀盐酸、品红溶液、新制澄清石灰水(提示:不必检验Ca2+和Cl-,表格可以不填满)。
| 实验步骤 | 预期现象和结论 | |
| ① | 取少量上述漂白粉与试管中, | |
| ② |
您最近一年使用:0次
解题方法
3 . 为了探究氨气能否和氢气一样还原CuO,他根据所提供的如图装置进行实验(夹持装置未画)。(1)装置A产生氨气,按气流方向连接各仪器接口,顺序为a→________ →________ →________ →________ →________ →________ →h。
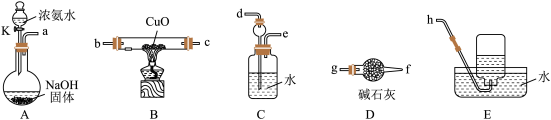
(2)实验开始时,打开分液漏斗的活塞K,发现浓氨水没有滴下,如果各仪器导管均没有堵塞,则可能的原因是________________________________________________________________________ ;
(3)实验结束后,装置B中固体由黑色变为红色,装置E中收集到无色无味的气体,在空气中无颜色变化,点燃的镁条可以在其中燃烧,则B装置中发生的化学方程式为_______________________________ ,装置C中的球形装置的作用是_________________________________________________ 。

(2)实验开始时,打开分液漏斗的活塞K,发现浓氨水没有滴下,如果各仪器导管均没有堵塞,则可能的原因是
(3)实验结束后,装置B中固体由黑色变为红色,装置E中收集到无色无味的气体,在空气中无颜色变化,点燃的镁条可以在其中燃烧,则B装置中发生的化学方程式为
您最近一年使用:0次
解题方法
4 . 过氧化钠(Na2O2)是一种淡黄色固体,有两个实验小组的同学为探究其与二氧化碳的反应,都用下图所示的装置进行实验。一段时间后,将带余烬的木条插入试管D中,木条复燃。
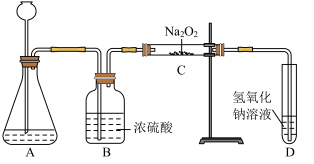
请回答下列问题:
(1)A是制取CO2的装置,写出A中发生反应的化学方程式:__________ 。
(2)第1小组同学认为Na2O2与CO2反应生成了Na2CO3和O2,该反应的化学方程式为________ 。
(3)第2小组同学认为除生成Na2CO3和O2外,还有可能生成NaHCO3,你认为呢?并简述原因_____ 。
(4)请设计一种实验方案证明Na2O2与CO2反应生成了Na2CO3:______ 。
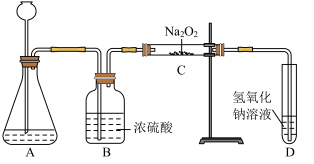
请回答下列问题:
(1)A是制取CO2的装置,写出A中发生反应的化学方程式:
(2)第1小组同学认为Na2O2与CO2反应生成了Na2CO3和O2,该反应的化学方程式为
(3)第2小组同学认为除生成Na2CO3和O2外,还有可能生成NaHCO3,你认为呢?并简述原因
(4)请设计一种实验方案证明Na2O2与CO2反应生成了Na2CO3:
您最近一年使用:0次
解题方法
5 . 某化学课外活动小组应用下图所示的方法研究物质的性质,其中气体E的主要成分是氯气,杂质是空气和水蒸气。回答下列问题:

(1)该项研究(实验)的主要目的是________ 。
(2)浓H2SO4的作用是_________ 。
(3)从物质性质的方面来看,这样的实验设计存在事故隐患,事故隐患是________ 。请在图中的D处以图像的形式表明消除事故隐患的措施_______ ,其中发生反应的化学方程式为__________ 。

(1)该项研究(实验)的主要目的是
(2)浓H2SO4的作用是
(3)从物质性质的方面来看,这样的实验设计存在事故隐患,事故隐患是
您最近一年使用:0次
解题方法
6 . 喷泉实验是中学化学的重要实验。
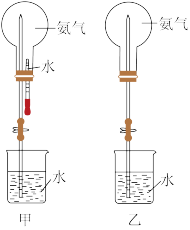
(1)实验室中常用图甲装置进行NH3的喷泉实验。用该装置完成喷泉实验的操作方法是_________ 。
(2)若用图乙装置进行NH3的喷泉实验,打开止水夹后,烧杯中的液体不能进入烧瓶。请写出引发喷泉实验的一种操作方法:____________ 。
(3)若将图甲装置中胶头滴管和烧杯中液体改为NaOH溶液,能用改动后的甲装置进行喷泉实验的一组气体是_________ (填字母)。
A.HCl和CO2 B.Cl2和CO C.O2和SO2 D.NO2和NO

(1)实验室中常用图甲装置进行NH3的喷泉实验。用该装置完成喷泉实验的操作方法是
(2)若用图乙装置进行NH3的喷泉实验,打开止水夹后,烧杯中的液体不能进入烧瓶。请写出引发喷泉实验的一种操作方法:
(3)若将图甲装置中胶头滴管和烧杯中液体改为NaOH溶液,能用改动后的甲装置进行喷泉实验的一组气体是
A.HCl和CO2 B.Cl2和CO C.O2和SO2 D.NO2和NO
您最近一年使用:0次
7 . 二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。
(1)简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作____ 。
(2)某学习小组设计用如下图装置验证二氧化硫的化学性质。
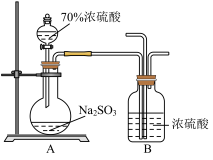

(3)能说明SO2具有氧化性的实验现象为_________________ 。
(4)为验证SO2的还原性,充分反应后,取试管b中溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色退去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是________ (填“Ⅰ”“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为__________________ 。
(1)简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作
(2)某学习小组设计用如下图装置验证二氧化硫的化学性质。


(3)能说明SO2具有氧化性的实验现象为
(4)为验证SO2的还原性,充分反应后,取试管b中溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色退去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是
您最近一年使用:0次
2020-01-28更新
|
147次组卷
|
2卷引用:鲁教版高中必修1化学第三章《自然界中的元素》测试卷
8 . 按下图要求完成实验,并回答问题:
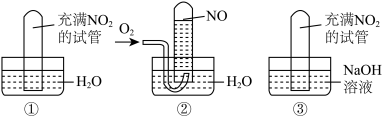
(1)实验①将充满二氧化氮的试管倒立水中,观察到的现象是__________________________ 。
(2)实验②将充满二氧化氮的试管倒立水中,再通入氧气时观察到的现象是_________ 。
(3)实验③将充满二氧化氮的试管倒立氢氧化钠溶液中,观察到的现象是_______________ 。

(1)实验①将充满二氧化氮的试管倒立水中,观察到的现象是
(2)实验②将充满二氧化氮的试管倒立水中,再通入氧气时观察到的现象是
(3)实验③将充满二氧化氮的试管倒立氢氧化钠溶液中,观察到的现象是
您最近一年使用:0次
9 . 为探究Na2SO3溶液的性质,在白色点滴板的a、b、c、d四个凹槽中滴入Na2SO3溶液,再分别滴加下图所示的试剂:
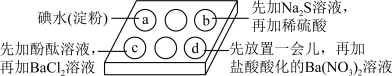
对实验现象的“解释或结论”错误的是( )

对实验现象的“解释或结论”错误的是( )
| 选项 | 实验现象 | 解释或结论 |
| A | a中溶液褪色 | 还原性: |
| B | b中加硫酸后产生淡黄色沉淀 | 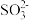 和 和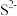 在酸性条件下发生反应 在酸性条件下发生反应 |
| C | c中滴入酚酞溶液变红,再加BaCl2溶液后产生白色沉淀且红色褪色 |  ,所以滴入酚酞变红; ,所以滴入酚酞变红; ,使水解平衡左移,红色褪去 ,使水解平衡左移,红色褪去 |
| D | d中产生白色沉淀 | Na2SO3溶液已变质 |
| A.A |
| B.B |
| C.C |
| D.D |
您最近一年使用:0次
解题方法
10 . 某课外活动小组研究金属钾的性质。他们首先通过分析钾与钠的原子结构示意图及查阅有关资料,知道钾与钠属于同一类物质,在性质上有许多相似之处。但在金属活动性顺序表中,钾排在钠的前面,钾在空气中燃烧的产物是超氧化钾(KO2)。
(1)预测钾的化学性质,完成下列反应的化学方程式:
①钾在氯气中燃烧____________________________ ;
②点燃钾剧烈燃烧_____________________________ ;
③将小块钾投入冷水中______________________________ ;
(2)推测钾在自然界中的存在方式是(填“游离态”或“化合态”)________ 。
(3)该小组研究钾的性质时用到的主要方法有____________________________________ 。
(4)他们研究金属钾性质的程序是__________________________________ 。
(1)预测钾的化学性质,完成下列反应的化学方程式:
①钾在氯气中燃烧
②点燃钾剧烈燃烧
③将小块钾投入冷水中
(2)推测钾在自然界中的存在方式是(填“游离态”或“化合态”)
(3)该小组研究钾的性质时用到的主要方法有
(4)他们研究金属钾性质的程序是
您最近一年使用:0次
2020-01-28更新
|
430次组卷
|
5卷引用:2020年春季人教版高中化学必修2第一章《物质结构 元素周期律》测试卷



