名校
解题方法
1 . 同学们探究不同金属和浓硫酸的反应。向三等份浓硫酸中分别加入大小相同的不同金属片,加热,用生成气体进行下表实验操作并记录实验现象。
已知: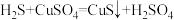 (CuS为黑色固体);
(CuS为黑色固体); 可燃
可燃
下列说法不正确 的是
| 实验操作 | 实验现象 | ||
| 金属为铜 | 金属为锌 | 金属为铝 | |
| 点燃 | 不燃烧 | 燃烧 | 燃烧 |
通入 酸性溶液 酸性溶液 | 褪色 | 褪色 | 褪色 |
通入 溶液 溶液 | 无明显变化 | 无明显变化 | 出现黑色沉淀 |
| 通入品红溶液 | 褪色 | 褪色 | 不褪色 |
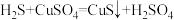 (CuS为黑色固体);
(CuS为黑色固体); 可燃
可燃下列说法
A.加入铜片的实验中,使 酸性溶液褪色的气体是 酸性溶液褪色的气体是 |
B.加入铝片的实验中,燃烧现象能证明生成气体中一定含 |
| C.加入锌片的实验中,生成的气体一定是混合气体 |
| D.金属与浓硫酸反应的还原产物与金属活动性强弱有关 |
您最近一年使用:0次
2021-05-10更新
|
1558次组卷
|
16卷引用:云南省昆明市第一中学2022-2023学年高一下学期期中考试化学试题
云南省昆明市第一中学2022-2023学年高一下学期期中考试化学试题趋势4 创新探究类实验(已下线)第四章 非金属及其化合物 第21练 硫酸 含硫物质的转化北京市房山区2022-2023学年高三二模化学试题广东省广州市番禺中学2022-2023学年高一下学期4月期中考试化学试题(已下线)第4讲 浓硫酸 不同价态含硫物质的转化北京市海淀区2021届高三二模化学试题(已下线)2021年高考化学押题预测卷(北京卷)(02)(已下线)第13讲 硫及其化合物(精练)-2022年高考化学一轮复习讲练测(已下线)专题12 硫及其化合物 (热点讲义)-2022年高三毕业班化学常考点归纳与变式演练北京首都师范大学附属中学2021-2022学年高三上学期10月月考化学试题辽宁省沈阳市东北育才学校2021-2022学年高三上学期学段考试化学试题北京市北京师范大学附属实验中学2021-2022学年高一下学期期中考试化学试题北京师范大学附属实验中学2021-2022学年高一下学期期中考试化学试题北京市中国人民大学附属中学2023-2024学年高三下学期一模模拟化学试题北京市第八十中学2023-2024学年高一下学期期中考试化学(选考)试题
名校
2 . 某同学用右图所示的装置及药品进行酸性强弱比较的实验,下列说法不正确的是


| A.①和②中发生的反应均为复分解反应 |
| B.向Na2SiO3饱和溶液中滴酚酞溶液无明显现象 |
| C.一段时间后②中有胶冻状物质生成 |
| D.该实验能证明酸性强弱的顺序是:硫酸>碳酸>硅酸 |
您最近一年使用:0次
2016-12-09更新
|
250次组卷
|
11卷引用:云南省玉溪师范学院附属中学2022-2023学年高一下学期期末考试化学试题
云南省玉溪师范学院附属中学2022-2023学年高一下学期期末考试化学试题云南省漾濞二中2019-2020学年高二上学期开学考试化学试题2015-2016学年北京市西城区高一上学期期末考试化学试卷2016-2017学年广东省汕头市金山中学高一上学期期末考试化学试卷(已下线)北京市第四中学2016-2017学年高一下学期期中考试化学试题贵州省遵义航天高级中学2017-2018学年高一上学期期末考试理科综合化学试题安徽省定远重点中学2018-2019学年高一下学期开学考试化学试题安徽省合肥市肥东县高级中学2019-2020学年高一上学期期末考试化学试题安徽省滁州市民办高中2019-2020学年高一上学期期末考试化学试题甘肃省玉门市油田第一中学2020-2021学年高一上学期期末考试化学试题四川省绵阳中学实验学校2019-2020学年高一下学期入学考试化学试题
名校
解题方法
3 . 某小组利用如下装置(夹持装置略),探究浓、稀硝酸与铜反应的气体产物。回答下列问题:___________ 。
(2)请写出稀硝酸与铜反应的离子方程式___________ 。
(3)为节约药品用量,有人建议用具支试管(下图)代替仪器X,用试管代替集气瓶。为方便控制铜与硝酸反应的发生和停止,改进措施是___________ ;用改进后的装置进行铜与浓硝酸反应的实验,具支试管中产生的气体和排水收集到的气体___________ (填“相同”“不相同”)。 ,
, 仅得到一个
仅得到一个 ,稀硝酸与铜反应生成NO,
,稀硝酸与铜反应生成NO, 得到三个
得到三个 ,但氧化性却是浓硝酸>稀硝酸。解释角度一:比较氧化剂的氧化性不是比较
,但氧化性却是浓硝酸>稀硝酸。解释角度一:比较氧化剂的氧化性不是比较___________ ;角度二:同一种还原剂能被浓硝酸氧化,不能被稀硝酸氧化。根据角度二设计了如下装置,用以证明浓硝酸和稀硝酸的氧化性强弱关系。 ,目的是
,目的是___________ ;滴加浓硝酸后,当③中为稀硝酸时,其液面上方气体仍为无色;当③中为浓硝酸时,其液面上方气体由无色变为红棕色,反应的化学方程式为___________ 。
(5)有人提出(4)中角度二的验证实验不够简约,可将之前排水集气收集满NO的两支试管用橡胶塞塞紧,为防止气体逸出产生污染,在不取下胶塞的情况下向试管中分别加入稀硝酸、浓硝酸,简述其加入稀硝酸、浓硝酸的方法___________ 。
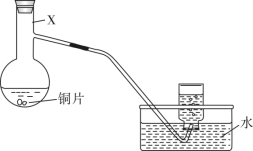
(2)请写出稀硝酸与铜反应的离子方程式
(3)为节约药品用量,有人建议用具支试管(下图)代替仪器X,用试管代替集气瓶。为方便控制铜与硝酸反应的发生和停止,改进措施是
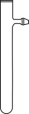
 ,
, 仅得到一个
仅得到一个 ,稀硝酸与铜反应生成NO,
,稀硝酸与铜反应生成NO, 得到三个
得到三个 ,但氧化性却是浓硝酸>稀硝酸。解释角度一:比较氧化剂的氧化性不是比较
,但氧化性却是浓硝酸>稀硝酸。解释角度一:比较氧化剂的氧化性不是比较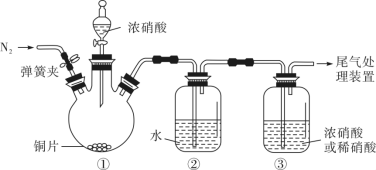
 ,目的是
,目的是(5)有人提出(4)中角度二的验证实验不够简约,可将之前排水集气收集满NO的两支试管用橡胶塞塞紧,为防止气体逸出产生污染,在不取下胶塞的情况下向试管中分别加入稀硝酸、浓硝酸,简述其加入稀硝酸、浓硝酸的方法
您最近一年使用:0次
解题方法
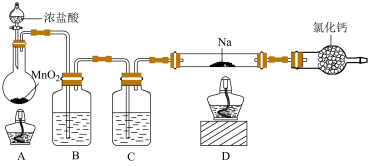
4 . 某同学利用如图所示装置(夹持装置已省略)制备氯气并探究其部分性质。
请回答下列问题:
(1)装置A中发生反应的离子方程式为___________ ;装置B的作用为___________ ;装置C中的试剂为___________ 。
(2)实验开始时,先点燃A处酒精灯,待观察到D中硬质玻璃管内充满黄绿色气体时,再点燃D处酒精灯,目的是___________ 。
(3)装置D中发生反应的化学方程式为___________ 。
(4)将装置E中出来的尾气通入滴有酚酞的NaOH溶液中,发生反应的离子方程式为___________ ;观察到溶液红色褪去,甲同学认为是反应生成了漂白性物质导致的,乙同学则认为是NOH被完全消耗导致的。指导老师做了如下实验对甲、乙同学的猜想进行验证:取适量反应后的溶液于试管1中,加入过量___________ ,溶液无明显现象,证明乙同学猜想错误;另取适量原反应后的溶液于试管2中,加入适量___________ ,溶液变红,证明甲同学猜想正确。(供选择的试剂:稀硫酸、NaOH溶液、紫色石蕊溶液、无色酚酞溶液、氯水)

请回答下列问题:
(1)装置A中发生反应的离子方程式为
(2)实验开始时,先点燃A处酒精灯,待观察到D中硬质玻璃管内充满黄绿色气体时,再点燃D处酒精灯,目的是
(3)装置D中发生反应的化学方程式为
(4)将装置E中出来的尾气通入滴有酚酞的NaOH溶液中,发生反应的离子方程式为
您最近一年使用:0次
2023-12-03更新
|
101次组卷
|
2卷引用:云南省楚雄州2023-2024学年高一上学期期中教育学业质量监测化学试题
解题方法
5 . 金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制钠的工业方法,其反应原理是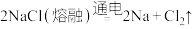 。请完成下列有关单质钠的问题。
。请完成下列有关单质钠的问题。
(1)保存金属钠的正确方法是___________ (填字母)。
(2)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应(如图所示),生成淡黄色固体,请写出该反应的化学方程式:___________ 。___________ 。
(4)将一小块金属钠投入 溶液中,发生反应的总化学方程式为
溶液中,发生反应的总化学方程式为___________ 。
(5)常温常压下,CO2和过氧化钠反应后,若固体质量增加了28g,反应中消耗的CO2的质量是___________ g。
(6)根据上述实验小组同学猜测过氧化钠可用作呼吸面具、潜水艇等中的供氧剂。请选择适当的化学试剂和实验仪器,用如图所示的实验装置进行实验,以证明过氧化钠可作供氧剂。请回答下列问题。___________ 。
②装置B中盛有饱和NaHCO3溶液,其作用是___________ 。
③装置D中盛放的试剂是___________ ,其目的是___________ 。
④当观察到试管F中收集满气体,为证明收集的气体是O2,还需要进行哪些实验操作?___________ 。
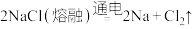 。请完成下列有关单质钠的问题。
。请完成下列有关单质钠的问题。(1)保存金属钠的正确方法是
| A.放在棕色瓶中 | B.放在石蜡油中 | C.放在水中 | D.放在煤油中 |
(2)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应(如图所示),生成淡黄色固体,请写出该反应的化学方程式:
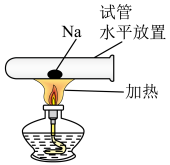
(4)将一小块金属钠投入
 溶液中,发生反应的总化学方程式为
溶液中,发生反应的总化学方程式为(5)常温常压下,CO2和过氧化钠反应后,若固体质量增加了28g,反应中消耗的CO2的质量是
(6)根据上述实验小组同学猜测过氧化钠可用作呼吸面具、潜水艇等中的供氧剂。请选择适当的化学试剂和实验仪器,用如图所示的实验装置进行实验,以证明过氧化钠可作供氧剂。请回答下列问题。
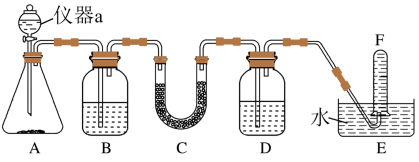
②装置B中盛有饱和NaHCO3溶液,其作用是
③装置D中盛放的试剂是
④当观察到试管F中收集满气体,为证明收集的气体是O2,还需要进行哪些实验操作?
您最近一年使用:0次
名校
解题方法
6 . 某兴趣小组设计如图所示装置制取SO2,研究其性质,并进一步探究在适当温度和催化剂的条件下,SO2与O2反应后混合气体的成分。
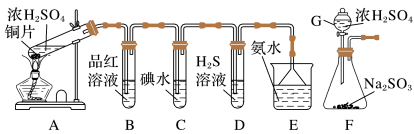
(1)仪器G的名称是___________ 。
(2)写出A中反应的化学方程式___________ 。
(3)装置B、C、D分别用于检验SO2的漂白性、还原性和氧化性。则装置C中反应的离子方程式为___________ 。证明SO2具有氧化性的实验现象是___________ 。
(4)为了实现绿色环保的目标,某同学设计装置F来代替装置A.与装置A相比,装置F的优点是___________ (写出一条即可)。
(5)若选用装置F制取O2可选用的试剂是___________ 。
(6)该小组同学设计如下装置来检验SO2与O2反应后混合气体的成分。
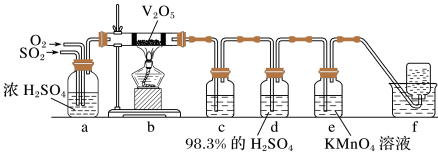
已知:SO3遇水剧烈反应,放出大量的热,产生酸雾。98.3%的H2SO4可以吸收SO3和酸雾。
供选择试剂:蒸馏水、0.5mol·L-1BaCl2溶液、98.3%的H2SO4、2.0mol·L-1NaOH溶液、KMnO4溶液。
①c中应选用的试剂是___________ ,e中试剂的作用是___________ ,f中收集的气体是___________ 。
②甲同学提出用饱和NaHSO3溶液代替98.3%的H2SO4,乙同学提出质疑,认为此方案不可行,请简述乙同学认为不可行的理由:___________ 。

(1)仪器G的名称是
(2)写出A中反应的化学方程式
(3)装置B、C、D分别用于检验SO2的漂白性、还原性和氧化性。则装置C中反应的离子方程式为
(4)为了实现绿色环保的目标,某同学设计装置F来代替装置A.与装置A相比,装置F的优点是
(5)若选用装置F制取O2可选用的试剂是
(6)该小组同学设计如下装置来检验SO2与O2反应后混合气体的成分。

已知:SO3遇水剧烈反应,放出大量的热,产生酸雾。98.3%的H2SO4可以吸收SO3和酸雾。
供选择试剂:蒸馏水、0.5mol·L-1BaCl2溶液、98.3%的H2SO4、2.0mol·L-1NaOH溶液、KMnO4溶液。
①c中应选用的试剂是
②甲同学提出用饱和NaHSO3溶液代替98.3%的H2SO4,乙同学提出质疑,认为此方案不可行,请简述乙同学认为不可行的理由:
您最近一年使用:0次
名校
解题方法
7 . 为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验。
实验I:反应产物的定性探究
按如图装置(固定装置已略去)进行实验:
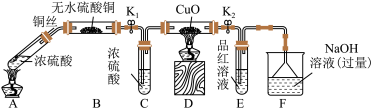
(1)A装置中发生反应的化学方程式为___________ 。F装置的烧杯中发生反应的离子方程式是___________ ,B装置中的现象是___________ 。
(2)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是___________ 。
(3)实验结束时,撤去所有酒精灯之前必须完成的实验操作是___________ 。
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是___________ 。
实验II:反应产物的定量探究
(5)在铜与浓硫酸反应的过程中,发现有黑色物质出现,且黑色物质为 。产生的
。产生的 反应为
反应为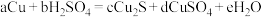 。则a:b=
。则a:b=___________ 。为测定硫酸铜的产率,将铜与浓硫酸反应所得溶液中和后配制成250.00mL溶液,取该溶液25.00mL加入足量KI溶液中振荡,以淀粉溶液为指示剂,用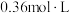 的
的 溶液滴定生成的
溶液滴定生成的 。3次实验平均消耗该
。3次实验平均消耗该 溶液25.00mL。若反应消耗铜的质量为6.4g,则硫酸铜的产率为
溶液25.00mL。若反应消耗铜的质量为6.4g,则硫酸铜的产率为___________ 。(已知: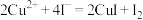 ,
, )
)
实验I:反应产物的定性探究
按如图装置(固定装置已略去)进行实验:

(1)A装置中发生反应的化学方程式为
(2)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是
(3)实验结束时,撤去所有酒精灯之前必须完成的实验操作是
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是
实验II:反应产物的定量探究
(5)在铜与浓硫酸反应的过程中,发现有黑色物质出现,且黑色物质为
 。产生的
。产生的 反应为
反应为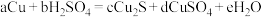 。则a:b=
。则a:b=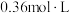 的
的 溶液滴定生成的
溶液滴定生成的 。3次实验平均消耗该
。3次实验平均消耗该 溶液25.00mL。若反应消耗铜的质量为6.4g,则硫酸铜的产率为
溶液25.00mL。若反应消耗铜的质量为6.4g,则硫酸铜的产率为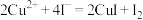 ,
, )
)
您最近一年使用:0次
8 . 某同学探究不同条件下氯气与二价锰化合物的反应。实验装置如下图(夹持装置略)
滴液漏斗
资料:i.Mn2+在一定条件下被Cl2或ClO-氧化成MnO2(棕黑色)、MnO (绿色)、MnO
(绿色)、MnO (紫色)。
(紫色)。
ii.浓碱条件下,MnO 可被OH-还原为MnO
可被OH-还原为MnO 。
。
iii.Cl2的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
(1)B中试剂是_______ ,装置D的作用为_______ 。
(2)滴液漏斗的弯管作用为_______ 。
(3)通入Cl2前,Ⅱ、Ⅲ中沉淀在空气中缓慢由白色变为棕黑色的化学方程式为_______ 。
(4)根据资料ii,Ⅲ中应得到绿色溶液,实验中得到的是紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl2导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将MnO 氧化为MnO
氧化为MnO 。
。
①用化学方程式表示可能导致溶液碱性减弱的原因:_______ ,但通过实验测定溶液的碱性变化很小。
②取Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为_______ ,溶液绿色缓慢加深,原因是MnO2被_______ (填“化学式”)氧化,可证明Ⅲ的悬浊液中氧化剂过量。
③取Ⅱ中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生反应的离子方程式是_______ 。
滴液漏斗

资料:i.Mn2+在一定条件下被Cl2或ClO-氧化成MnO2(棕黑色)、MnO
 (绿色)、MnO
(绿色)、MnO (紫色)。
(紫色)。ii.浓碱条件下,MnO
 可被OH-还原为MnO
可被OH-还原为MnO 。
。iii.Cl2的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
| 序号 | 物质a | C中实验现象 | |
| 通入Cl2前 | 通入Cl2后 | ||
| I | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
| Ⅱ | 5%NaOH溶液 | 产生白色沉淀Mn(OH)2,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
| Ⅲ | 40%NaOH溶液 | 产生白色沉淀Mn(OH)2,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
(2)滴液漏斗的弯管作用为
(3)通入Cl2前,Ⅱ、Ⅲ中沉淀在空气中缓慢由白色变为棕黑色的化学方程式为
(4)根据资料ii,Ⅲ中应得到绿色溶液,实验中得到的是紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl2导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将MnO
 氧化为MnO
氧化为MnO 。
。①用化学方程式表示可能导致溶液碱性减弱的原因:
②取Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为
③取Ⅱ中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生反应的离子方程式是
您最近一年使用:0次
9 . I.某化学兴趣小组利用如图装置进行“铁粉与水蒸气反应”的实验,并检验产物的性质(部分夹持装置已略去),请回答下列问题:
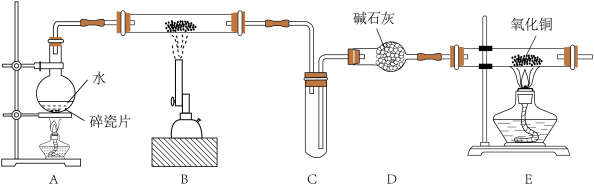
(1)A、B两个装置中应先点燃_______ (填序号)处的酒精(喷)灯。
(2)B装置硬质玻璃管中发生反应的化学方程式为_______ 。
(3)E装置中产生的现象是_______ 。
II.高铁酸钾 是一种新型净水剂,实验小组制备高铁酸钾
是一种新型净水剂,实验小组制备高铁酸钾 并探究其性质。
并探究其性质。
资料: 为紫色固体,微溶于
为紫色固体,微溶于 溶液;具有强氧化性,在酸性或中性溶液中快速产生
溶液;具有强氧化性,在酸性或中性溶液中快速产生 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。
(4)配平工业制备 反应的离子方程式:
反应的离子方程式:_______ 
(5)实验室制备 (夹持装置略):
(夹持装置略):
如图,A为氯气发生装置,其中反应方程式为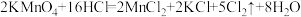 。
。
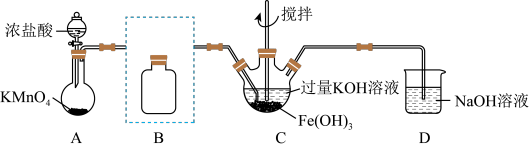
①B为未组装好的除杂装置,B中所用试剂的作用为_______ 。
②C中得到紫色固体, 发生的反应主要是
发生的反应主要是 ,除此之外C中
,除此之外C中 还会发生的反应有(用离子方程式表示)
还会发生的反应有(用离子方程式表示)_______ 。
(6)探究 的性质
的性质
取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有 。为证明
。为证明 是否氧化了
是否氧化了 而产生
而产生 ,设计以下方案:
,设计以下方案:
①由方案I中溶液变红可知a中含有_______ 。
②根据方案II得出:氧化性
_______  (填“>”或“<”),而此结论与
(填“>”或“<”),而此结论与 的制备实验证明的氧化性强弱关系相反,说明溶液的酸碱性会影响粒子的氧化性强弱。
的制备实验证明的氧化性强弱关系相反,说明溶液的酸碱性会影响粒子的氧化性强弱。

(1)A、B两个装置中应先点燃
(2)B装置硬质玻璃管中发生反应的化学方程式为
(3)E装置中产生的现象是
II.高铁酸钾
 是一种新型净水剂,实验小组制备高铁酸钾
是一种新型净水剂,实验小组制备高铁酸钾 并探究其性质。
并探究其性质。资料:
 为紫色固体,微溶于
为紫色固体,微溶于 溶液;具有强氧化性,在酸性或中性溶液中快速产生
溶液;具有强氧化性,在酸性或中性溶液中快速产生 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。(4)配平工业制备
 反应的离子方程式:
反应的离子方程式:
(5)实验室制备
 (夹持装置略):
(夹持装置略):如图,A为氯气发生装置,其中反应方程式为
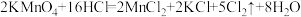 。
。
①B为未组装好的除杂装置,B中所用试剂的作用为
②C中得到紫色固体,
 发生的反应主要是
发生的反应主要是 ,除此之外C中
,除此之外C中 还会发生的反应有(用离子方程式表示)
还会发生的反应有(用离子方程式表示)(6)探究
 的性质
的性质取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有
 。为证明
。为证明 是否氧化了
是否氧化了 而产生
而产生 ,设计以下方案:
,设计以下方案:| 方案I | 取少量a,滴加 溶液至过量,溶液呈红色。 溶液至过量,溶液呈红色。 |
| 方案II | 用 溶液充分洗涤C中所得固体,再用 溶液充分洗涤C中所得固体,再用 溶液将 溶液将 溶出,得到紫色溶液b.取少量b,滴加盐酸,有 溶出,得到紫色溶液b.取少量b,滴加盐酸,有 产生。 产生。 |
②根据方案II得出:氧化性

 (填“>”或“<”),而此结论与
(填“>”或“<”),而此结论与 的制备实验证明的氧化性强弱关系相反,说明溶液的酸碱性会影响粒子的氧化性强弱。
的制备实验证明的氧化性强弱关系相反,说明溶液的酸碱性会影响粒子的氧化性强弱。
您最近一年使用:0次
名校
解题方法
10 . 实验表明,当乙醛加入到溴水中,溴水会褪色。针对此现象,某化学兴趣小组同学依据乙醛结构进行探究。
【实验假设】
(1)假设Ⅰ:醛基含有不饱和键,可与Br2发生_______ 反应(填反应类型)。
假设Ⅱ:乙醛具有α-H,可与溴水发生取代反应。无论乙醛发生几元取代反应,参加反应的Br2与生成的HBr的物质的量之比为_______ 。
假设Ⅲ:乙醛具有较强的还原性,可被溴水氧化,反应的化学方程式为_______ 。
【实验过程】针对以上假设,该小组同学设计了两组方案。
方案Ⅰ:通过对比反应现象判断反应类型。
结论:假设Ⅰ不成立。
(2)则试管2中的实验现象为_______ 。
方案Ⅱ:通过测定反应后混合液的pH判断反应类型。
注:苯酚和乙酸的电离及温度变化对混合液pH的影响可忽略不计。
(3)写出苯酚与溴水反应的化学方程式:_______ 。
(4)若试管4中反应后混合液的pH=1.85,则证明乙醛与溴水的反应为_______ 反应(填反应类型);若试管4中反应后混合液的pH_______ 1.85(填“大于”或“小于”),则证明乙醛与溴水的反应为氧化反应。
【实验假设】
(1)假设Ⅰ:醛基含有不饱和键,可与Br2发生
假设Ⅱ:乙醛具有α-H,可与溴水发生取代反应。无论乙醛发生几元取代反应,参加反应的Br2与生成的HBr的物质的量之比为
假设Ⅲ:乙醛具有较强的还原性,可被溴水氧化,反应的化学方程式为
【实验过程】针对以上假设,该小组同学设计了两组方案。
方案Ⅰ:通过对比反应现象判断反应类型。
| 序号 | 操作 | 现象 |
| 试管1 | 1mL溴水+1mL乙醛,充分振荡后静置 | 褪色 |
| 试管2 | 1mL溴的CCl4溶液+1mL乙醛,充分振荡后静置 |
(2)则试管2中的实验现象为
方案Ⅱ:通过测定反应后混合液的pH判断反应类型。
| 序号 | 操作 | pH |
| 试管3 | 加入20mL溴水,再加入10mL苯酚溶液,待完全反应后(苯酚过量),测定混合液pH | 1.85 |
| 试管4 | 加入20mL相同浓度的溴水,再加入10mL 20%的乙醛溶液(乙醛过量),3min后完全褪色,测定混合液pH |
(3)写出苯酚与溴水反应的化学方程式:
(4)若试管4中反应后混合液的pH=1.85,则证明乙醛与溴水的反应为
您最近一年使用:0次



