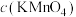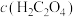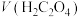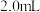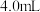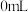1 . 从矿石中提取金(Au)是获取贵金属的主要来源,工业上常以 溶液、氨水和
溶液、氨水和 溶液为原料配制浸金液{含
溶液为原料配制浸金液{含 }。
}。
已知:① 在酸性环境中易分解,在碱性环境中较稳定,能与金形成稳定的
在酸性环境中易分解,在碱性环境中较稳定,能与金形成稳定的 。
。
②几种物质或离子的颜色如表所示:
回答下列问题:
(1) 中提供空轨道的为
中提供空轨道的为_______ (填名称,下同),配体为_______ 。配制过程中氨水需过量,其原因是_______ 。
某科研小组对该浸金液的浸金原理进行探究:
提出猜想:
猜想一: 吸附在金表面,在
吸附在金表面,在 的作用下生成
的作用下生成 和
和 ,
, 迅速被
迅速被 替换成
替换成 ,
, 被空气中的氧气氧化成
被空气中的氧气氧化成 参与循环。
参与循环。
猜想二: 吸附在金表面,在氧气作用下生成
吸附在金表面,在氧气作用下生成 和
和 ,
, 迅速被
迅速被 替换成
替换成 ,
, 与
与 生成的
生成的 参与循环。
参与循环。
验证猜想:
(2)俗话说“真金不怕火炼”,从化学性质的角度说明:_______ 。据此有人得出结论:猜想二不成立,但有人觉得溶液的酸碱性对物质的性质有一定影响,为验证猜想二是否成立,设计如下实验:
步骤一:用pH试纸测浸金液的pH,其操作为_______ 。
步骤二:配制与浸金液pH相同的 溶液。用
溶液。用 固体配制一定物质的量浓度的
固体配制一定物质的量浓度的 溶液所用的玻璃仪器包括量筒、烧杯、玻璃棒、
溶液所用的玻璃仪器包括量筒、烧杯、玻璃棒、_______ 。
步骤三:将一块金片放入配制的 溶液中,并通入空气,一段时间后,若观察到
溶液中,并通入空气,一段时间后,若观察到_______ ,则猜想二可能成立。
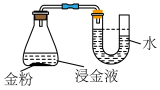
(3)某小组设计如图所示实验验证猜想一。_______ (填锥形瓶中出现的实验现象),则猜想一可能成立;打开瓶塞后的现象用离子方程式表示为_______ 。
 溶液、氨水和
溶液、氨水和 溶液为原料配制浸金液{含
溶液为原料配制浸金液{含 }。
}。已知:①
 在酸性环境中易分解,在碱性环境中较稳定,能与金形成稳定的
在酸性环境中易分解,在碱性环境中较稳定,能与金形成稳定的 。
。②几种物质或离子的颜色如表所示:
| 物质或离子 | Au | 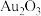 |  |  |  |
| 颜色 | 黄色 | 棕黑 | 蓝色 | 无色 | 无色 |
(1)
 中提供空轨道的为
中提供空轨道的为某科研小组对该浸金液的浸金原理进行探究:
提出猜想:
猜想一:
 吸附在金表面,在
吸附在金表面,在 的作用下生成
的作用下生成 和
和 ,
, 迅速被
迅速被 替换成
替换成 ,
, 被空气中的氧气氧化成
被空气中的氧气氧化成 参与循环。
参与循环。猜想二:
 吸附在金表面,在氧气作用下生成
吸附在金表面,在氧气作用下生成 和
和 ,
, 迅速被
迅速被 替换成
替换成 ,
, 与
与 生成的
生成的 参与循环。
参与循环。验证猜想:
(2)俗话说“真金不怕火炼”,从化学性质的角度说明:
步骤一:用pH试纸测浸金液的pH,其操作为
步骤二:配制与浸金液pH相同的
 溶液。用
溶液。用 固体配制一定物质的量浓度的
固体配制一定物质的量浓度的 溶液所用的玻璃仪器包括量筒、烧杯、玻璃棒、
溶液所用的玻璃仪器包括量筒、烧杯、玻璃棒、步骤三:将一块金片放入配制的
 溶液中,并通入空气,一段时间后,若观察到
溶液中,并通入空气,一段时间后,若观察到(3)某小组设计如图所示实验验证猜想一。
您最近半年使用:0次
名校
解题方法
2 . 喷泉实验装置如图所示。应用下列各组气体和溶液,能出现喷泉现象的是

| 选项 | 气体 | 溶液 |
| A |  | 饱和氯水 |
| B | NO | 稀硫酸 |
| C |  | NaOH溶液 |
| D | Cl2 | 饱和NaHCO3溶液 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
3 . 某兴趣小组同学将 的酸性
的酸性 溶液和
溶液和 溶液按如下比例混合,探究浓度对反应速率的影响。
溶液按如下比例混合,探究浓度对反应速率的影响。
现象:实验①溶液很快由紫色变为青绿色,而实验②慢一点;变为青绿色后,实验②溶液很快褪至无色,而实验①褪色慢一点。
资料: 与
与 很难形成配合物;
很难形成配合物;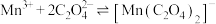 (青绿色),
(青绿色), 有强氧化性,而
有强氧化性,而 氧化性极弱。
氧化性极弱。
下列说法错误的是
 的酸性
的酸性 溶液和
溶液和 溶液按如下比例混合,探究浓度对反应速率的影响。
溶液按如下比例混合,探究浓度对反应速率的影响。序号 | 温度 |
|
|
|
|
|
① | 20℃ |
|
|
|
|
|
② | 20℃ |
|
|
|
|
|
资料:
 与
与 很难形成配合物;
很难形成配合物;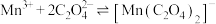 (青绿色),
(青绿色), 有强氧化性,而
有强氧化性,而 氧化性极弱。
氧化性极弱。下列说法错误的是
A. |
B. 溶液中能通过加盐酸酸化调 溶液中能通过加盐酸酸化调 |
C.溶液由青绿色褪至无色过程中,实验①中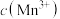 较小,导致褪色速率较慢 较小,导致褪色速率较慢 |
D.由实验可知,加入 越多, 越多, 溶液由紫色褪至无色的速率越快 溶液由紫色褪至无色的速率越快 |
您最近半年使用:0次
2023-06-02更新
|
229次组卷
|
2卷引用:河北省2022-2023学年高三下学期1月大联考化学试题
名校
解题方法
4 . 某小组利用硫代硫酸钠溶液与稀硫酸反应:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O,探究反应条件对速率的影响,下列有关说法正确的是
| 选项 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
| ① | 25 | 10 | 0.1 | 10 | 0.1 | 0 |
| ② | 25 | 5 | 0.1 | 10 | 0.1 | X |
| ③ | 50 | 10 | 0.1 | 5 | 0.2 | 5 |
| A.可通过产生浑浊的时间判断反应的快慢 |
| B.①③两组实验可探究硫酸浓度对反应速率的影响 |
| C.①②两组实验可探究Na2S2O3浓度对反应速率的影响,则x=5 |
| D.实验结束后,有少量S附着在试管上,可以用水冲洗干净 |
您最近半年使用:0次
2023-05-28更新
|
113次组卷
|
2卷引用:安徽省六安第一中学2022-2023学年高一下学期期中考试化学试题
5 . 探究银镜实验后溶解Ag的实验方案,如下表所示。
已知:Fe3+的氧化性与Ag+接近。下列有关叙述正确的是
| 实验方案 | 实验现象 | |
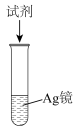 | 试剂 | |
| 实验①:稀硝酸 | 银逐渐溶解,试管口有浅红棕色气体生成 | |
| 实验②:Fe(NO3)3溶液(pH=2) | 银镜慢慢消失,溶液澄清 | |
| 实验③:FeCl3溶液(pH=2) | 银镜快速溶解,反应后溶液中有明显灰色沉淀 | |
| 实验④:HI溶液 | 银镜溶解,有黄色沉淀产生,且有气泡产生 | |
A.实验①发生反应的离子方程式为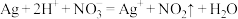 |
| B.对比分析实验②和③表明:Cl-具有催化作用 |
C.实验④发生反应的类型为置换反应,说明氧化性;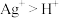 |
| D.综合上述实验说明溶解银的关键在于试剂的氧化性和能否生成银盐沉淀 |
您最近半年使用:0次
6 . 科学的假设是实验探究的先导与价值所在。下列在假设引导下的探究肯定没有 意义的是
A.探究 与 与 反应可能生成 反应可能生成 |
B.探究Na与乙醇反应可能有 生成 生成 |
C.探究 与 与 反应可能有 反应可能有 生成 生成 |
D.探究Mg与 溶液反应产生的气体中可能含有 溶液反应产生的气体中可能含有 |
您最近半年使用:0次
2023-05-20更新
|
100次组卷
|
2卷引用:北京市第十五中学2022-2023学年高一下学期期中考试化学试题
名校
7 . 某学习小组用酸性KMnO4溶液和H2C2O4(草酸)溶液之间的反应来研究“影响反应速率的因素”,设计实验方案如下:(假设溶液混合时体积可以加和)
(1)该实验探究的是_______ 因素对化学反应速率的影响,上述实验设计表: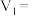
______ ,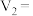
_______ 。
(2)利用实验1中数据计算,平均反应速率: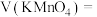
______  。
。
(3)该小组同学查阅已有的实验资料发现,该实验过程中Mn2+对反应有催化作用,并继续进行实验探究。请你帮助该小组同学完成实验方案。所加试剂X最好选用___________
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 溶液褪色至无色所需时间/min | |||
0.6mol/L  溶液 溶液 |  | 0.1mol/L  溶液 溶液 | 3mol/L  溶液 溶液 | ||
| 1 | 3.0 | 13.0 | 2.0 | 2.0 | 10.0 |
| 2 | 1.0 |  |  | 2.0 | 12.8 |
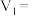
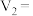
(2)利用实验1中数据计算,平均反应速率:
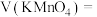
 。
。(3)该小组同学查阅已有的实验资料发现,该实验过程中Mn2+对反应有催化作用,并继续进行实验探究。请你帮助该小组同学完成实验方案。所加试剂X最好选用___________
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 少量 | 溶液褪色至无色所需时间/min | |||
0.6mol/L  溶液 溶液 |  | 0.1mol/L  溶液 溶液 | 3mol/L  溶液 溶液 | |||
| 3 | 3.0 | 13.0 | 2.0 | 2.0 | X | t |
A.0.1mol/L  | B.0.1mol/L  |
C. 粉末 粉末 | D. 粉末 粉末 |
您最近半年使用:0次
8 . 通过下列实验操作和现象能得出相应结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 取适量火柴头的浸泡液于试管中,滴加AgNO3溶液和稀HNO3 | 无白色沉淀 | 火柴头一定不含氯元素 |
| B | 向 样品溶液中先加入 样品溶液中先加入 溶液,然后再加入稀盐酸 溶液,然后再加入稀盐酸 | 生成白色沉淀,加入稀盐酸,沉淀不溶解 |  样品溶液已经变质 样品溶液已经变质 |
| C | 向盛有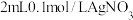 溶液的试管中滴加5滴 溶液的试管中滴加5滴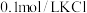 溶液,待生成白色沉淀后,再向其中滴加 溶液,待生成白色沉淀后,再向其中滴加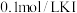 溶液 溶液 | 先有白色沉淀生成,后有黄色沉淀出现 | 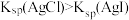 |
| D | 向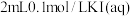 中加入 中加入 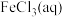 ,充分反应,用四氯化碳充分萃取后取上层溶液滴加 ,充分反应,用四氯化碳充分萃取后取上层溶液滴加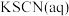 | 四氯化碳层显紫色,上层溶液试样变红 |  和 和 的反应存在限度 的反应存在限度 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
9 . 某小组通过分析镁与酸反应时pH的变化,探究镁与醋酸溶液反应的实质。
【实验】在常温水浴条件下,进行实验Ⅰ~Ⅲ,记录生成气体体积和溶液pH的变化:
Ⅰ.取0.1g光亮的镁屑(过量)放入10mL 0.10mol/L HCl溶液中;
Ⅱ.取0.1g光亮的镁屑放入10mL 0.10
 溶液
溶液 中;
中;
Ⅲ.取0.1g光亮的镁屑放入10mL pH=2.9 HCl溶液中。
【数据】
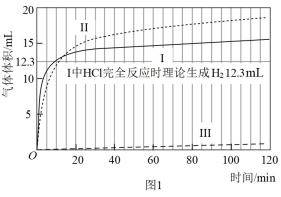
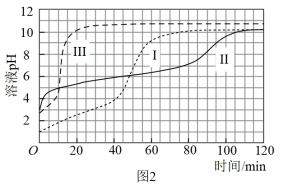
(1)起始阶段,Ⅰ中主要反应的离子方程式是___________ 。
(2)Ⅱ起始溶液中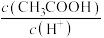 约为
约为___________ 。(选填“1”、“10”或“102”)
(3)起始阶段,导致Ⅱ、Ⅲ气体产生速率差异的主要因素不是 ,实验证据是
,实验证据是___________ 。
(4)探究Ⅱ的反应速率大于Ⅲ的原因。
提出假设: 能直接与Mg反应。
能直接与Mg反应。
进行实验Ⅳ:___________ 。
实验现象:___________ 。
得出结论:该假设成立。
(5)探究醋酸溶液中与Mg反应的主要微粒,进行实验Ⅴ。
与Ⅱ相同的条件和试剂用量,将溶液换成含0.10 的
的 与0.10
与0.10
 的混合溶液pH=4.8,气体产生速率与Ⅱ对比如下。
的混合溶液pH=4.8,气体产生速率与Ⅱ对比如下。
对比a~c中的微粒浓度,解释其a与b、a与c气体产生速率差异的原因:___________ 。
(6)综合以上实验得出2个结论:镁与醋酸溶液反应时, 、
、 、
、 均能与镁反应产生氢气:
均能与镁反应产生氢气:___________ 。
【实验】在常温水浴条件下,进行实验Ⅰ~Ⅲ,记录生成气体体积和溶液pH的变化:
Ⅰ.取0.1g光亮的镁屑(过量)放入10mL 0.10mol/L HCl溶液中;
Ⅱ.取0.1g光亮的镁屑放入10mL 0.10

 溶液
溶液 中;
中;Ⅲ.取0.1g光亮的镁屑放入10mL pH=2.9 HCl溶液中。
【数据】


(1)起始阶段,Ⅰ中主要反应的离子方程式是
(2)Ⅱ起始溶液中
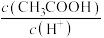 约为
约为(3)起始阶段,导致Ⅱ、Ⅲ气体产生速率差异的主要因素不是
 ,实验证据是
,实验证据是(4)探究Ⅱ的反应速率大于Ⅲ的原因。
提出假设:
 能直接与Mg反应。
能直接与Mg反应。进行实验Ⅳ:
实验现象:
得出结论:该假设成立。
(5)探究醋酸溶液中与Mg反应的主要微粒,进行实验Ⅴ。
与Ⅱ相同的条件和试剂用量,将溶液换成含0.10
 的
的 与0.10
与0.10
 的混合溶液pH=4.8,气体产生速率与Ⅱ对比如下。
的混合溶液pH=4.8,气体产生速率与Ⅱ对比如下。| a.实验Ⅴ起始速率 | b.实验Ⅱ起始速率 | c.实验ⅡpH=4.8时速率 |
2.1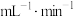 | 2.3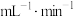 | 0.8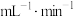 |
(6)综合以上实验得出2个结论:镁与醋酸溶液反应时,
 、
、 、
、 均能与镁反应产生氢气:
均能与镁反应产生氢气:
您最近半年使用:0次
10 . 甲醛是有毒气体,某实验小组探究能否用氨水吸收甲醛。
Ⅰ.甲醛溶液的制备与浓度测定
已知制备甲醛的反应原理如下:
①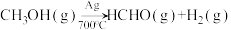
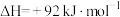
②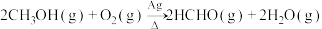
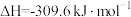
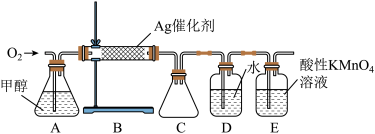
实验室制备甲醛溶液的装置如图所示。(加热装置已略去)
回答下列问题:
(1)装置A中盛放甲醇的仪器名称为___________ 。
(2)从能量利用的角度说明 的作用是
的作用是___________ ;为了防止高温下甲醛在催化剂表面吸附太久被 进一步氧化为甲酸,可采取的措施是
进一步氧化为甲酸,可采取的措施是___________ 。
(3)实验结束后,取5mL新制 悬浊液,滴入适量的装置D的溶液,加热,有砖红色沉淀生成,反应的化学方程式为
悬浊液,滴入适量的装置D的溶液,加热,有砖红色沉淀生成,反应的化学方程式为___________ 。
(4)甲醛溶液的浓度测定:装置D的溶液经预处理后,取10.00mL稀释至200mL,移取20.00mL稀释液于碘量瓶中,加入 溶液和指示剂,振荡,静置5分钟后用0.1000
溶液和指示剂,振荡,静置5分钟后用0.1000
 标准溶液滴定生成的NaOH至终点,重复三次实验,平均消耗
标准溶液滴定生成的NaOH至终点,重复三次实验,平均消耗 标准溶液体积为20.00mL。则所制得的溶液中甲醛浓度为
标准溶液体积为20.00mL。则所制得的溶液中甲醛浓度为___________  (计算结果保留四位有效数字)。(已知:
(计算结果保留四位有效数字)。(已知: )
)
Ⅱ.甲醛与氨水反应的实验探究
实验探究(ⅰ)
(5)实验1的目的是___________ 。
关于实验3褪色的原因,小组成员提出了以下猜想:
猜想①:甲醛与氨水发生反应,溶液碱性减弱,酚酞溶液褪色。
猜想②:甲醛与酚酞溶液发生反应,指示剂失效,溶液褪色。
实验探究(ⅱ)
(6)实验5的操作为___________ 。由实验4、5说明猜想___________ (填标号)正确。
Ⅰ.甲醛溶液的制备与浓度测定
已知制备甲醛的反应原理如下:
①
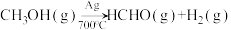
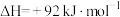
②
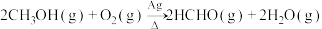
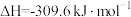
实验室制备甲醛溶液的装置如图所示。(加热装置已略去)

回答下列问题:
(1)装置A中盛放甲醇的仪器名称为
(2)从能量利用的角度说明
 的作用是
的作用是 进一步氧化为甲酸,可采取的措施是
进一步氧化为甲酸,可采取的措施是(3)实验结束后,取5mL新制
 悬浊液,滴入适量的装置D的溶液,加热,有砖红色沉淀生成,反应的化学方程式为
悬浊液,滴入适量的装置D的溶液,加热,有砖红色沉淀生成,反应的化学方程式为(4)甲醛溶液的浓度测定:装置D的溶液经预处理后,取10.00mL稀释至200mL,移取20.00mL稀释液于碘量瓶中,加入
 溶液和指示剂,振荡,静置5分钟后用0.1000
溶液和指示剂,振荡,静置5分钟后用0.1000
 标准溶液滴定生成的NaOH至终点,重复三次实验,平均消耗
标准溶液滴定生成的NaOH至终点,重复三次实验,平均消耗 标准溶液体积为20.00mL。则所制得的溶液中甲醛浓度为
标准溶液体积为20.00mL。则所制得的溶液中甲醛浓度为 (计算结果保留四位有效数字)。(已知:
(计算结果保留四位有效数字)。(已知: )
)Ⅱ.甲醛与氨水反应的实验探究
实验探究(ⅰ)
| 实验编号 | 操作 | 现象 |
| 1 | 取适量D的溶液,用pH计测溶液的pH | pH≈7.0 |
| 2 | 取2mL2%氨水(滴有酚酞),逐滴加入3mL10%甲醇溶液 | 没有明显变化 |
| 3 | 取2mL2%氨水(滴有酚酞),逐滴加入装置D的溶液 | 红色褪去 |
关于实验3褪色的原因,小组成员提出了以下猜想:
猜想①:甲醛与氨水发生反应,溶液碱性减弱,酚酞溶液褪色。
猜想②:甲醛与酚酞溶液发生反应,指示剂失效,溶液褪色。
实验探究(ⅱ)
| 实验编号 | 操作 | 现象 |
| 4 | 取实验3的无色溶液1mL,滴入几滴氨水 | 溶液变红 |
| 5 | 无明显变化 |
您最近半年使用:0次