名校
解题方法
1 . 利用如图的装置(省略部分加热装置)制备 (铋酸钠),已知
(铋酸钠),已知 不溶于冷水且在酸性溶液中迅速分解,
不溶于冷水且在酸性溶液中迅速分解, 是一种难溶于水的白色沉淀。下列说法正确的是
是一种难溶于水的白色沉淀。下列说法正确的是
 (铋酸钠),已知
(铋酸钠),已知 不溶于冷水且在酸性溶液中迅速分解,
不溶于冷水且在酸性溶液中迅速分解, 是一种难溶于水的白色沉淀。下列说法正确的是
是一种难溶于水的白色沉淀。下列说法正确的是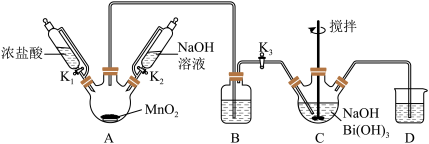
A.装置B应放入饱和 溶液,目的是吸收A中挥发的盐酸 溶液,目的是吸收A中挥发的盐酸 |
B.为使 完全转化为 完全转化为 ,反应过程中应向装置C通入过量 ,反应过程中应向装置C通入过量 |
C.拆除装置前必须进行的操作是关闭 、 、 ,打开 ,打开 |
D.上述反应中若消耗22.4L  则理论上可制得280g 则理论上可制得280g  |
您最近半年使用:0次
名校
解题方法
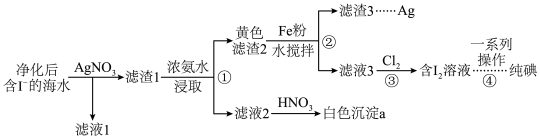
2 . 碘及其化合物在生产、生活等方面都有广泛的应用,下图是从海水提取单质碘的一种工艺流程图。回答下列问题:___________ 。白色沉淀a的化学式___________ 。
(2)滤渣1用浓氨水浸取,滤渣部分溶解,用平衡移动的原理进行合理解释:___________ (要求写出可逆反应,并适当进行文字说明)。
(3)步骤②发生反应的离子方程式___________ 。
(4)步骤③通入 后,若生成两种氧化产物且物质的量的比为1:1,则发生反应的离子方程式
后,若生成两种氧化产物且物质的量的比为1:1,则发生反应的离子方程式___________ 。
(5)步骤④中一系列操作包括___________ (填实验操作名称)。
(6)硝酸银是高中重要的检验用试剂,写出净化后含 海水(碘元素含量较高)中含有
海水(碘元素含量较高)中含有 的检验方法
的检验方法___________ 。
(7)银盐大部分不溶于水,现在有两种银盐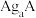 和
和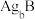 均难溶于水,在含有
均难溶于水,在含有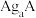 和
和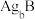 的悬浊液中加入
的悬浊液中加入 的
的 溶液,混合溶液中
溶液,混合溶液中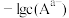 或
或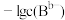 与
与 的关系如图所示:
的关系如图所示:
___________ 。
② 点饱和溶液中加入硝酸银溶液,
点饱和溶液中加入硝酸银溶液,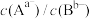 将
将___________ (填增大、減小、不变、不能确定)。
(2)滤渣1用浓氨水浸取,滤渣部分溶解,用平衡移动的原理进行合理解释:
(3)步骤②发生反应的离子方程式
(4)步骤③通入
 后,若生成两种氧化产物且物质的量的比为1:1,则发生反应的离子方程式
后,若生成两种氧化产物且物质的量的比为1:1,则发生反应的离子方程式(5)步骤④中一系列操作包括
(6)硝酸银是高中重要的检验用试剂,写出净化后含
 海水(碘元素含量较高)中含有
海水(碘元素含量较高)中含有 的检验方法
的检验方法(7)银盐大部分不溶于水,现在有两种银盐
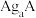 和
和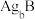 均难溶于水,在含有
均难溶于水,在含有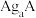 和
和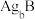 的悬浊液中加入
的悬浊液中加入 的
的 溶液,混合溶液中
溶液,混合溶液中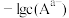 或
或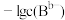 与
与 的关系如图所示:
的关系如图所示: 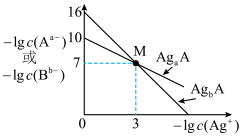

②
 点饱和溶液中加入硝酸银溶液,
点饱和溶液中加入硝酸银溶液,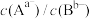 将
将
您最近半年使用:0次
3 . 硝酸镍、硝酸钠在陶瓷、玻璃工业应用广泛。以废弃镍板(含有少量的氧化铝杂质)生产硝酸镍、硝酸钠工艺流程如下:
(1)工业生产普通玻璃的主要原料有石英砂、__________ 、__________ 。
(2)“反应器”中需控制反应温度50~60℃,若温度太低,可能导致的后果是__________ ;若温度太高,可能导致的后果是__________ 。
(3)假如Ni与浓硝酸反应产生的混合气体中 ,该反应的离子方程式为
,该反应的离子方程式为__________ 。
(4)向“浸取液”中加入 调节pH至5~6,能除去浸取液中的
调节pH至5~6,能除去浸取液中的 ,相应原理为
,相应原理为_______ 。__________ 。
(6)向“转化器”中加入稀硝酸的目的是__________ 。
(7)已知:①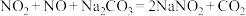 ;
;
②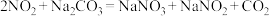 。
。
若将一定体积的 、NO混合气体,通入
、NO混合气体,通入 溶液中恰好被完全吸收,则反应中被氧化的氮原子与被还原的氮原子的质量之比为
溶液中恰好被完全吸收,则反应中被氧化的氮原子与被还原的氮原子的质量之比为__________ 。

(1)工业生产普通玻璃的主要原料有石英砂、
(2)“反应器”中需控制反应温度50~60℃,若温度太低,可能导致的后果是
(3)假如Ni与浓硝酸反应产生的混合气体中
 ,该反应的离子方程式为
,该反应的离子方程式为(4)向“浸取液”中加入
 调节pH至5~6,能除去浸取液中的
调节pH至5~6,能除去浸取液中的 ,相应原理为
,相应原理为__________+
 +
+ __________
__________ +
+ _________+
_________+
 。
。
(6)向“转化器”中加入稀硝酸的目的是
(7)已知:①
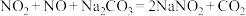 ;
;②
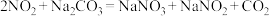 。
。若将一定体积的
 、NO混合气体,通入
、NO混合气体,通入 溶液中恰好被完全吸收,则反应中被氧化的氮原子与被还原的氮原子的质量之比为
溶液中恰好被完全吸收,则反应中被氧化的氮原子与被还原的氮原子的质量之比为
您最近半年使用:0次
4 . 碲(Te)是半导体、红外探测等领域的重要战略元素。从阳极泥或冶炼烟尘中提取的粗二氧化碲中含有 、PbO、CuO等杂质。一种由粗二氧化碲提取纯碲的工艺流程如图所示。
、PbO、CuO等杂质。一种由粗二氧化碲提取纯碲的工艺流程如图所示。
(1)“浸出”步骤中,碲和硒两种元素分别转化为 和
和 。浸出温度控制在65℃左右,当温度超过80℃时,碲的浸出率会小幅降低。降低的主要原因是
。浸出温度控制在65℃左右,当温度超过80℃时,碲的浸出率会小幅降低。降低的主要原因是___________ 。
(2) 的沸点(387℃)高于
的沸点(387℃)高于 的沸点(191.4℃),原因是
的沸点(191.4℃),原因是___________ 。
(3)“净化”步骤中产生的滤渣主要含___________ (写化学式)和少量硒单质。
(4)化学反应的吉布斯自由能变 。
。 还原
还原 和
和 的
的 随温度T的变化曲线如图所示。则“还原除杂”步骤的温度不宜超过
随温度T的变化曲线如图所示。则“还原除杂”步骤的温度不宜超过___________ K,该步骤控制在此温度以下的原因是___________ 。___________ 。
(6)“还原”后的酸性还原尾液中含有少量未被还原的碲,加入还原剂R进行“尾还原”,可以产生粗碲,提高碲的回收率。综合还原效率、工艺成本和环保因素,最合适的还原剂是___________ (填标号)。
A.铁粉 B.氢气 C.硫化钠
 、PbO、CuO等杂质。一种由粗二氧化碲提取纯碲的工艺流程如图所示。
、PbO、CuO等杂质。一种由粗二氧化碲提取纯碲的工艺流程如图所示。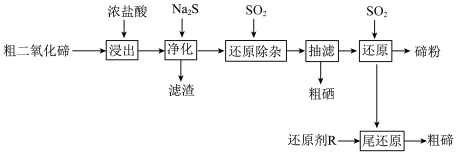
(1)“浸出”步骤中,碲和硒两种元素分别转化为
 和
和 。浸出温度控制在65℃左右,当温度超过80℃时,碲的浸出率会小幅降低。降低的主要原因是
。浸出温度控制在65℃左右,当温度超过80℃时,碲的浸出率会小幅降低。降低的主要原因是(2)
 的沸点(387℃)高于
的沸点(387℃)高于 的沸点(191.4℃),原因是
的沸点(191.4℃),原因是(3)“净化”步骤中产生的滤渣主要含
(4)化学反应的吉布斯自由能变
 。
。 还原
还原 和
和 的
的 随温度T的变化曲线如图所示。则“还原除杂”步骤的温度不宜超过
随温度T的变化曲线如图所示。则“还原除杂”步骤的温度不宜超过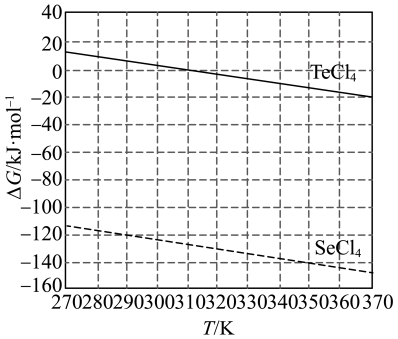
(6)“还原”后的酸性还原尾液中含有少量未被还原的碲,加入还原剂R进行“尾还原”,可以产生粗碲,提高碲的回收率。综合还原效率、工艺成本和环保因素,最合适的还原剂是
A.铁粉 B.氢气 C.硫化钠
您最近半年使用:0次
昨日更新
|
180次组卷
|
2卷引用:河南省周口市2024届高三二模理综-化学试题
名校
5 . 氯化亚铁在冶金、医药制造、媒染剂等方面有着较为广泛的用途,氯化亚铁可以对许多分子进行激活反应,成为一种新型“明星分子”。回答下列问题:
(1)由 固体粗略配制
固体粗略配制 溶液,称取
溶液,称取___________ g 固体在
固体在___________ (填试剂)中溶解后,加水稀释为 ,最后加入少量铁粉。
,最后加入少量铁粉。
(2)“无汞定铁法”标定 溶液浓度:
溶液浓度:
①将___________ (填酸式或碱式)滴定管先水洗,再润洗,最后盛装 标准
标准 溶液,其下一步操作是
溶液,其下一步操作是___________ ,……正确安装滴定管。
②用移液管准确量取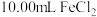 溶液注入锥形瓶中,并加入
溶液注入锥形瓶中,并加入 硫酸和几滴二苯胺磺酸钠。二苯胺磺酸钠的作用是
硫酸和几滴二苯胺磺酸钠。二苯胺磺酸钠的作用是___________ 。
③用 标准溶液滴定,当锥形瓶中溶液颜色从绿色变为紫红色即为滴定终点,平行滴定三次,平均消耗
标准溶液滴定,当锥形瓶中溶液颜色从绿色变为紫红色即为滴定终点,平行滴定三次,平均消耗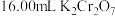 标准溶液,写出滴定反应的离子方程式
标准溶液,写出滴定反应的离子方程式___________ 。 溶液的标定浓度为
溶液的标定浓度为___________ 。
(3)取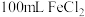 溶液加热、蒸干、灼烧至质量不变。固体质量为
溶液加热、蒸干、灼烧至质量不变。固体质量为___________ 。
(4)已知:亚硫酰氯( )沸点为
)沸点为 ,遇水极易水解。实验室利用
,遇水极易水解。实验室利用 固体和亚硫酰氯(
固体和亚硫酰氯( )制备新型“明星分子”
)制备新型“明星分子” 固体的装置如下图所示:
固体的装置如下图所示: 后,先加热装置
后,先加热装置___________ (填“a”或“b”)。
②装置c、d连接在一起共同起到的作用___________ 。
③硬质玻璃试管b中发生反应的化学方程式___________ 。
④装置e中试剂为 的酸性
的酸性 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为___________ 。
(1)由
 固体粗略配制
固体粗略配制 溶液,称取
溶液,称取 固体在
固体在 ,最后加入少量铁粉。
,最后加入少量铁粉。(2)“无汞定铁法”标定
 溶液浓度:
溶液浓度:①将
 标准
标准 溶液,其下一步操作是
溶液,其下一步操作是②用移液管准确量取
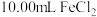 溶液注入锥形瓶中,并加入
溶液注入锥形瓶中,并加入 硫酸和几滴二苯胺磺酸钠。二苯胺磺酸钠的作用是
硫酸和几滴二苯胺磺酸钠。二苯胺磺酸钠的作用是③用
 标准溶液滴定,当锥形瓶中溶液颜色从绿色变为紫红色即为滴定终点,平行滴定三次,平均消耗
标准溶液滴定,当锥形瓶中溶液颜色从绿色变为紫红色即为滴定终点,平行滴定三次,平均消耗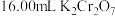 标准溶液,写出滴定反应的离子方程式
标准溶液,写出滴定反应的离子方程式 溶液的标定浓度为
溶液的标定浓度为(3)取
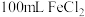 溶液加热、蒸干、灼烧至质量不变。固体质量为
溶液加热、蒸干、灼烧至质量不变。固体质量为(4)已知:亚硫酰氯(
 )沸点为
)沸点为 ,遇水极易水解。实验室利用
,遇水极易水解。实验室利用 固体和亚硫酰氯(
固体和亚硫酰氯( )制备新型“明星分子”
)制备新型“明星分子” 固体的装置如下图所示:
固体的装置如下图所示: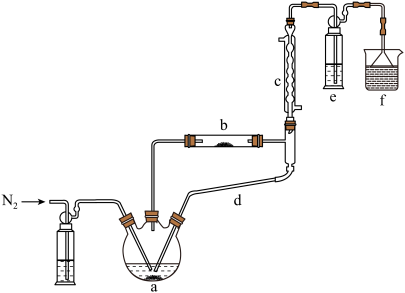
 后,先加热装置
后,先加热装置②装置c、d连接在一起共同起到的作用
③硬质玻璃试管b中发生反应的化学方程式
④装置e中试剂为
 的酸性
的酸性 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为
您最近半年使用:0次
6 . 利用废旧锂电池可回收金属元素。已知废旧锂离子电池的主要成分为 以及
以及 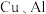 等单质,回收工艺流程如图:
等单质,回收工艺流程如图:
(1)“反萃取”中主要用到的玻璃仪器是_______(填字母)。
(2)“生化反应”后溶液中存在的主要阳离子有 、
、_______ 。“生化反应”最初使用的是 和
和  ,该过程中反应的
,该过程中反应的  与还原剂的物质的量之比为
与还原剂的物质的量之比为_______ ,使用细菌的优点是_______ 。
(3) 萃取率随温度变化如图所示,请解释变化的原因:
萃取率随温度变化如图所示,请解释变化的原因:_______ 。_______ 。
(5) (相对分子质量为183)经过反复洗涤、干燥后,进行灼烧,加热到
(相对分子质量为183)经过反复洗涤、干燥后,进行灼烧,加热到 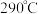 过程中,若生成两种气体,剩余固体的质量为
过程中,若生成两种气体,剩余固体的质量为 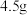 ,所得固体成分为
,所得固体成分为_______ (填化学式)。
(6)金属铜的晶胞如图所示,此晶胞的边长为 ,设
,设  为阿伏加德罗常数的值,则铜晶胞的密度ρ=
为阿伏加德罗常数的值,则铜晶胞的密度ρ=_______ g∙cm-3 (用含  的代数式表示)。
的代数式表示)。
 以及
以及 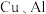 等单质,回收工艺流程如图:
等单质,回收工艺流程如图: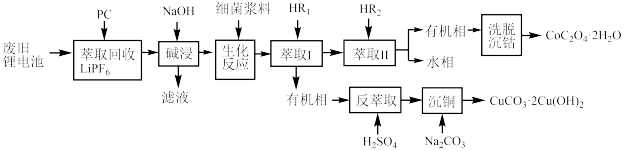
(1)“反萃取”中主要用到的玻璃仪器是_______(填字母)。
| A.漏斗 | B.胶头滴管 | C.分液漏斗 | D.蒸馏烧瓶 |
(2)“生化反应”后溶液中存在的主要阳离子有
 、
、 和
和  ,该过程中反应的
,该过程中反应的  与还原剂的物质的量之比为
与还原剂的物质的量之比为(3)
 萃取率随温度变化如图所示,请解释变化的原因:
萃取率随温度变化如图所示,请解释变化的原因: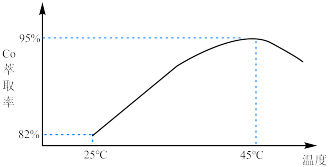
(5)
 (相对分子质量为183)经过反复洗涤、干燥后,进行灼烧,加热到
(相对分子质量为183)经过反复洗涤、干燥后,进行灼烧,加热到 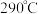 过程中,若生成两种气体,剩余固体的质量为
过程中,若生成两种气体,剩余固体的质量为 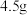 ,所得固体成分为
,所得固体成分为(6)金属铜的晶胞如图所示,此晶胞的边长为
 ,设
,设  为阿伏加德罗常数的值,则铜晶胞的密度ρ=
为阿伏加德罗常数的值,则铜晶胞的密度ρ= 的代数式表示)。
的代数式表示)。
您最近半年使用:0次
名校
解题方法
7 . 过二硫酸钠(Na2S2O8)是白色晶状粉末,易溶于水,不溶于乙醇,加热至65℃就会发生分解,常用作漂白剂,金属表面处理剂等。实验室以过氧化氢、浓硫酸和碳酸钠为原料制备过二硫酸钠。
I.过一硫酸(H2SO5)的合成
原理:H2O2+H2SO4=H2SO5+H2O。________ 。
(2)水槽中盛放的试剂C是________ (填“冰水”或“热水”)。
Ⅱ.过二硫酸钠(Na2S2O8)的合成
取下球形冷凝管A,在适当搅拌的条件下,沿瓶口a向仪器B中加入一定量的无水碳酸钠,控制加入速度,并控制反应温度在60℃左右,待碳酸钠完全溶解后继续恒温搅拌20min使之反应完全,这个过程中瓶口a不能封闭。
(3)合成反应分两步完成:________ ,2Na2SO4+H2SO5=2Na2S2O8+H2O。
(4)反应完毕,将仪器B中的溶液减压浓缩;结晶过滤、洗涤干燥,可得过硫酸钠,减压浓缩的原因是_________________ 。
(5)1mol Na2S2O8中存在的-O-O-数目为________ 。
(6)Na2S2O8具有强氧化性,可将I-氧化为I2: +2I-=2
+2I-=2 +I2↓,可用Fe2+作催化剂改变上述反应途径。试用离子方程式表示Fe2+对上述反应催化的历程:
+I2↓,可用Fe2+作催化剂改变上述反应途径。试用离子方程式表示Fe2+对上述反应催化的历程:_____________ 、__________ 。
(7)取适量过二硫酸钠,装入硬质玻璃管中,加热,将分解产物依次通过装置B、C、D,实验中发现B中U形管内产生无色液体,接着无色液体慢慢变成固体,C中溶液颜色无明显变化,D中溶液逐渐变蓝色。取硬质玻璃管少量残留固体于试管中,加入蒸馏水,溶解后滴加BaCl2溶液和盐酸,产生白色沉淀。写出A装置中发生反应的化学方程式:____________ 。
I.过一硫酸(H2SO5)的合成
原理:H2O2+H2SO4=H2SO5+H2O。
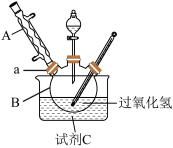
(2)水槽中盛放的试剂C是
Ⅱ.过二硫酸钠(Na2S2O8)的合成
取下球形冷凝管A,在适当搅拌的条件下,沿瓶口a向仪器B中加入一定量的无水碳酸钠,控制加入速度,并控制反应温度在60℃左右,待碳酸钠完全溶解后继续恒温搅拌20min使之反应完全,这个过程中瓶口a不能封闭。
(3)合成反应分两步完成:
(4)反应完毕,将仪器B中的溶液减压浓缩;结晶过滤、洗涤干燥,可得过硫酸钠,减压浓缩的原因是
(5)1mol Na2S2O8中存在的-O-O-数目为
(6)Na2S2O8具有强氧化性,可将I-氧化为I2:
 +2I-=2
+2I-=2 +I2↓,可用Fe2+作催化剂改变上述反应途径。试用离子方程式表示Fe2+对上述反应催化的历程:
+I2↓,可用Fe2+作催化剂改变上述反应途径。试用离子方程式表示Fe2+对上述反应催化的历程:(7)取适量过二硫酸钠,装入硬质玻璃管中,加热,将分解产物依次通过装置B、C、D,实验中发现B中U形管内产生无色液体,接着无色液体慢慢变成固体,C中溶液颜色无明显变化,D中溶液逐渐变蓝色。取硬质玻璃管少量残留固体于试管中,加入蒸馏水,溶解后滴加BaCl2溶液和盐酸,产生白色沉淀。写出A装置中发生反应的化学方程式:

您最近半年使用:0次
名校
解题方法
8 . 焦亚硫酸钠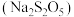 是一种抗氧化剂,受热易分解。某研究小组用下述方法制备少量
是一种抗氧化剂,受热易分解。某研究小组用下述方法制备少量 :在不断搅拌下,控制反应温度在
:在不断搅拌下,控制反应温度在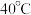 左右,向
左右,向 过饱和溶液中通入适量
过饱和溶液中通入适量 ,在
,在 左右静置结晶。实验装置如图所示。
左右静置结晶。实验装置如图所示。 的化学方程式为
的化学方程式为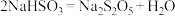 ,该反应是否为氧化还原反应
,该反应是否为氧化还原反应_______ (填“是”或“否”)。
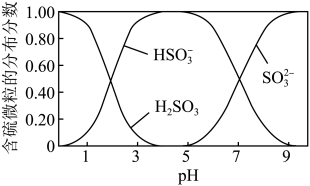
(2)已知平衡时含硫微粒的分布系数(分布系数 )与
)与 的关系如图所示。装置
的关系如图所示。装置 中,
中, 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为_______ ;判定可停止通 的实验操作为
的实验操作为_______ 。
(3)装置 的作用是
的作用是_______ 。
(4)制得的 中混有
中混有 和
和 杂质,其可能的原因是
杂质,其可能的原因是_______ 。
(5)测定某葡萄酒中 残留量,取
残留量,取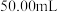 样品,用
样品,用 的碘标准液滴定至终点,消耗
的碘标准液滴定至终点,消耗 标准液。滴定反应为
标准液。滴定反应为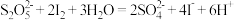 。该样品中
。该样品中 的残留量为
的残留量为_______  ;以下操作会造成
;以下操作会造成 残留量测定值偏高的是
残留量测定值偏高的是_______ (填字母)。
A.滴定终点读数时,俯视滴定管的刻度
B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
 是一种抗氧化剂,受热易分解。某研究小组用下述方法制备少量
是一种抗氧化剂,受热易分解。某研究小组用下述方法制备少量 :在不断搅拌下,控制反应温度在
:在不断搅拌下,控制反应温度在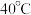 左右,向
左右,向 过饱和溶液中通入适量
过饱和溶液中通入适量 ,在
,在 左右静置结晶。实验装置如图所示。
左右静置结晶。实验装置如图所示。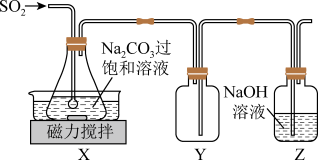
 的化学方程式为
的化学方程式为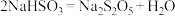 ,该反应是否为氧化还原反应
,该反应是否为氧化还原反应(2)已知平衡时含硫微粒的分布系数(分布系数
 )与
)与 的关系如图所示。装置
的关系如图所示。装置 中,
中, 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为 的实验操作为
的实验操作为(3)装置
 的作用是
的作用是(4)制得的
 中混有
中混有 和
和 杂质,其可能的原因是
杂质,其可能的原因是(5)测定某葡萄酒中
 残留量,取
残留量,取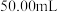 样品,用
样品,用 的碘标准液滴定至终点,消耗
的碘标准液滴定至终点,消耗 标准液。滴定反应为
标准液。滴定反应为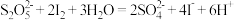 。该样品中
。该样品中 的残留量为
的残留量为 ;以下操作会造成
;以下操作会造成 残留量测定值偏高的是
残留量测定值偏高的是A.滴定终点读数时,俯视滴定管的刻度
B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
您最近半年使用:0次
解题方法
9 . 草酸 是一种白色粉末,
是一种白色粉末,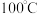 左右开始少量升华,熔点为
左右开始少量升华,熔点为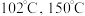 左右分解产生
左右分解产生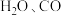 和
和 ;可与酸性
;可与酸性 溶液反应;其钠盐易溶于水,钙盐难溶于水;电离平衡常数为
溶液反应;其钠盐易溶于水,钙盐难溶于水;电离平衡常数为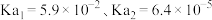 。
。
1.草酸可用于实验室制备少量 气体,应选择的发生装置为
气体,应选择的发生装置为___________ 。
常温下,向某浓度的草酸溶液中加入一定量等浓度的 溶液。
溶液。
3.当 时,溶液呈___________。
时,溶液呈___________。
A.酸性 B.碱性 C.中性 D.无法判断
此时,溶液中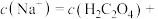
___________ 。
4.当 时,计算该溶液的
时,计算该溶液的
___________ 。(结果保留两位小数)计算过程。
 是一种白色粉末,
是一种白色粉末,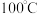 左右开始少量升华,熔点为
左右开始少量升华,熔点为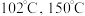 左右分解产生
左右分解产生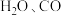 和
和 ;可与酸性
;可与酸性 溶液反应;其钠盐易溶于水,钙盐难溶于水;电离平衡常数为
溶液反应;其钠盐易溶于水,钙盐难溶于水;电离平衡常数为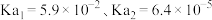 。
。1.草酸可用于实验室制备少量
 气体,应选择的发生装置为
气体,应选择的发生装置为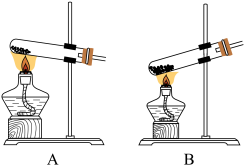
A.用足量的 溶液充分吸收后,可收集得到纯净的 溶液充分吸收后,可收集得到纯净的 |
| B.通过灼热的氧化铜,若出现黑色变红色现象,则产生的气体中一定有CO |
C.通入足量的澄清石灰水中,若能产生白色沉淀,则产生的气体中一定有 |
D.通入酸性 溶液中,若能使溶液褪色,说明草酸具有还原性 溶液中,若能使溶液褪色,说明草酸具有还原性 |
常温下,向某浓度的草酸溶液中加入一定量等浓度的
 溶液。
溶液。3.当
 时,溶液呈___________。
时,溶液呈___________。A.酸性 B.碱性 C.中性 D.无法判断
此时,溶液中
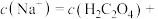
4.当
 时,计算该溶液的
时,计算该溶液的
您最近半年使用:0次
解题方法
10 . 过硫酸铵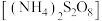 被广泛用于金属及半导体材料的表面处理剂和印刷线路的刻蚀剂。实验室选用下列装置制备
被广泛用于金属及半导体材料的表面处理剂和印刷线路的刻蚀剂。实验室选用下列装置制备 ,反应原理为
,反应原理为 。
。
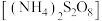 被广泛用于金属及半导体材料的表面处理剂和印刷线路的刻蚀剂。实验室选用下列装置制备
被广泛用于金属及半导体材料的表面处理剂和印刷线路的刻蚀剂。实验室选用下列装置制备 ,反应原理为
,反应原理为 。
。
A.装置 中固体药品为 中固体药品为 |
B.装置 的作用是干燥氨气 的作用是干燥氨气 |
C.制备 时仪器的连接顺序为 时仪器的连接顺序为 |
| D.装置D的作用是收集氨气 |
您最近半年使用:0次



