名校
1 . 有机合成是有机化学的重要组成部分,如图是关于气体A制备和性质的合成路线图。已知C是一种塑料,D是一种植物生长调节剂,可以催熟果实。
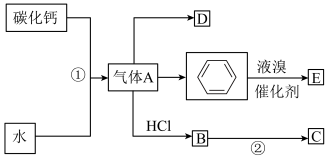
(1)①的化学方程式为______ 。
(2)②的化学方程式为______ ,该反应属于______ 反应(填反应类型)。
(3)D中的官能团为______ (填名称),写出实验室制D的化学方程式为______ ,该反应属于______ 反应(填反应类型)。
(4)与链烃相比,苯的化学性质的主要特征是 (单选)。
(5)证明苯制备E为取代反应的实验方案是______ 。已知硝基为间位定位基团,溴原子为邻、对位定位基团,写出以苯原料,制各间溴硝基苯的合成路线_____ 。
(合成路线的表示方式为:甲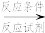 乙
乙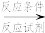 目标产物)
目标产物)
(6)与上述物质有关的化学实验的说法中,正确的是 (单选)。

(1)①的化学方程式为
(2)②的化学方程式为
(3)D中的官能团为
(4)与链烃相比,苯的化学性质的主要特征是 (单选)。
| A.难氧化、难取代、难加成 | B.易氧化、易取代、易加成 |
| C.难氧化、能加成、易取代 | D.易氧化、易加成、难取代 |
(合成路线的表示方式为:甲
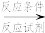 乙
乙 目标产物)
目标产物)(6)与上述物质有关的化学实验的说法中,正确的是 (单选)。
| A.实验室制备乙烯时,产生的气体使溴水褪色,能证明有乙烯生成 |
| B.除去溴苯中的溴,可用稀NaOH溶液反复洗涤,并用分液漏斗分液 |
| C.实验室制乙炔,反应物为固体和液体,且常温条件下反应,可以用启普发生器 |
| D.制取硝基苯时,试管中先加入浓H2SO4,再逐滴滴入浓HNO3和苯 |
您最近一年使用:0次
名校
2 . 某化学兴趣小组查阅文献资料了解到湿法合成高铁酸钾(K2FeO4)是目前人工成本最低、产品纯度最高的合成方法,其合成路线如图:
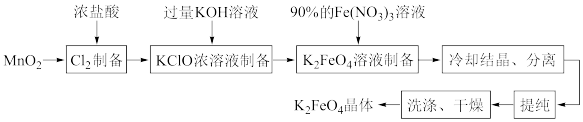
该兴趣小组根据文献资料设计了如图所示装置(部分夹持仪器已省略)制取K2FeO4。
已知:K2FeO4为紫色固体,具有强氧化性;在酸性或中性溶液中快速产生O2,在0℃~5℃、强碱性溶液中较稳定。
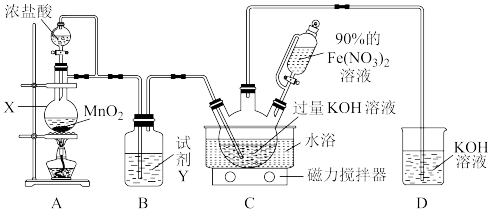
(1)仪器X的名称是_______ 。试剂Y的作用为_______ 。
(2)水浴方式是_______ (填“冷水浴”或“热水浴”)。
(3)装置C中KOH过量的原因是_______ 。
(4)上述流程中,“提纯”所用的方法是_______ 。
(5)称取1.98 g高铁酸钾样品,完全溶解于浓KOH溶液中,再加入足量亚铬酸钾{K[Cr(OH)4]}反应后配成100.00 mL溶液;取上述溶液20.00 mL于锥形瓶中,加入稀硫酸调至pH=2,并加入1 mL苯二胺磺酸钠作指示剂,用1.00 mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定,消耗(NH4)2Fe(SO4)2溶液5.76 mL。测定过程中发生反应:
a. Cr(OH) +FeO
+FeO =Fe(OH)3+CrO
=Fe(OH)3+CrO +OH-
+OH-
b. 2CrO +2H+=Cr2O
+2H+=Cr2O +H2O
+H2O
c. Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O
+6Fe2++14H+=2Cr3++6Fe3++7H2O
则K2FeO4样品的纯度是_______ 。
(6)K2FeO4是一种新型、高效、多功能水处理剂,既能杀菌消毒,又能净化水中悬浮杂质,请解释K2FeO4作为多功能水处理剂的原理:_______ 。
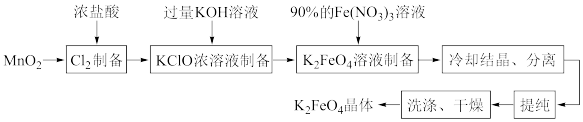
该兴趣小组根据文献资料设计了如图所示装置(部分夹持仪器已省略)制取K2FeO4。
已知:K2FeO4为紫色固体,具有强氧化性;在酸性或中性溶液中快速产生O2,在0℃~5℃、强碱性溶液中较稳定。

(1)仪器X的名称是
(2)水浴方式是
(3)装置C中KOH过量的原因是
(4)上述流程中,“提纯”所用的方法是
(5)称取1.98 g高铁酸钾样品,完全溶解于浓KOH溶液中,再加入足量亚铬酸钾{K[Cr(OH)4]}反应后配成100.00 mL溶液;取上述溶液20.00 mL于锥形瓶中,加入稀硫酸调至pH=2,并加入1 mL苯二胺磺酸钠作指示剂,用1.00 mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定,消耗(NH4)2Fe(SO4)2溶液5.76 mL。测定过程中发生反应:
a. Cr(OH)
 +FeO
+FeO =Fe(OH)3+CrO
=Fe(OH)3+CrO +OH-
+OH-b. 2CrO
 +2H+=Cr2O
+2H+=Cr2O +H2O
+H2Oc. Cr2O
 +6Fe2++14H+=2Cr3++6Fe3++7H2O
+6Fe2++14H+=2Cr3++6Fe3++7H2O则K2FeO4样品的纯度是
(6)K2FeO4是一种新型、高效、多功能水处理剂,既能杀菌消毒,又能净化水中悬浮杂质,请解释K2FeO4作为多功能水处理剂的原理:
您最近一年使用:0次
2022-01-12更新
|
158次组卷
|
4卷引用:福建省泉州市永春第一中学2022-2023学年高二下学期6月期末考试化学试题
福建省泉州市永春第一中学2022-2023学年高二下学期6月期末考试化学试题(已下线)江苏省南京市盐城市2023届高三3月第二次模拟考试化学试题变式题(工业流程题)(已下线)工业流程题吉林省长春吉大附中实验学校2021-2022学年高三上学期第三次摸底考试化学试题
解题方法
3 . 苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一、下面是它的一种实验室合成路线:
 +2H2O+H2SO4
+2H2O+H2SO4
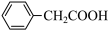 +NH4HSO4
+NH4HSO4
2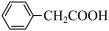 +Cu(OH)2→(
+Cu(OH)2→(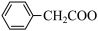 )2Cu+2H2O
)2Cu+2H2O
如图为制备苯乙酸的装置示意图(加热和夹持装置等略):已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇。
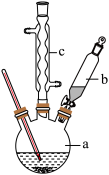
回答下列问题:
(1)在 三口瓶a中加入
三口瓶a中加入 硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是___________ 。
(2)将a中的溶液加热至 ,缓缓滴加
,缓缓滴加 苯乙腈到硫酸溶液中然后升温至
苯乙腈到硫酸溶液中然后升温至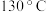 充分反应。在装置中,仪器b的作用是
充分反应。在装置中,仪器b的作用是___________ ;仪器c的名称是___________ ,其作用是___________ 。
(3)反应结束后加适量冷水,再分离出苯乙酸粗品。下列仪器中可用于分离苯乙酸粗品的是___________ (填标号)。
A.分液漏斗 B.漏斗 C.烧杯 D.直形冷凝管 E.玻璃棒
(4)提纯粗苯乙酸的具体操作步骤是___________ 、冷却结晶、过滤、洗涤、干燥。最终得到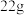 纯品,则苯乙酸的产率是
纯品,则苯乙酸的产率是___________ (保留三位有效数字)
(5)用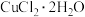 和
和 溶液制备适量
溶液制备适量 沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是
沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是___________ 。
(6)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入 搅拌
搅拌 ,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是
,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是___________ 。
 +2H2O+H2SO4
+2H2O+H2SO4
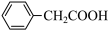 +NH4HSO4
+NH4HSO42
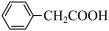 +Cu(OH)2→(
+Cu(OH)2→(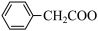 )2Cu+2H2O
)2Cu+2H2O如图为制备苯乙酸的装置示意图(加热和夹持装置等略):已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇。

回答下列问题:
(1)在
 三口瓶a中加入
三口瓶a中加入 硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是(2)将a中的溶液加热至
 ,缓缓滴加
,缓缓滴加 苯乙腈到硫酸溶液中然后升温至
苯乙腈到硫酸溶液中然后升温至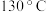 充分反应。在装置中,仪器b的作用是
充分反应。在装置中,仪器b的作用是(3)反应结束后加适量冷水,再分离出苯乙酸粗品。下列仪器中可用于分离苯乙酸粗品的是
A.分液漏斗 B.漏斗 C.烧杯 D.直形冷凝管 E.玻璃棒
(4)提纯粗苯乙酸的具体操作步骤是
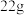 纯品,则苯乙酸的产率是
纯品,则苯乙酸的产率是(5)用
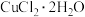 和
和 溶液制备适量
溶液制备适量 沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是
沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是(6)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入
 搅拌
搅拌 ,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是
,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是
您最近一年使用:0次
名校
4 . 亚硫酰氯( )和硫酰氯(
)和硫酰氯( )都是重要的化工原料,均易水解
)都是重要的化工原料,均易水解
I.亚硫酰氯( )又名氯化亚钒,熔点为-105℃,沸点为77℃,遇水剧烈反应,产生大量白雾,并生成刺激性气味的气体。
)又名氯化亚钒,熔点为-105℃,沸点为77℃,遇水剧烈反应,产生大量白雾,并生成刺激性气味的气体。
(1)用硫磺、液氯和 为原料,在一定条件下合成
为原料,在一定条件下合成 ,原子利用率可达100%,则三者的物质的量之比为
,原子利用率可达100%,则三者的物质的量之比为_______ 。
(2) 水解后无残留物,是较好的脱水剂。某同学设计实验将
水解后无残留物,是较好的脱水剂。某同学设计实验将 和
和 混合物加热来制取无水
混合物加热来制取无水 。
。
① 在该实验中作脱水剂的作用是
在该实验中作脱水剂的作用是_______ (写出两点)。
②实验室常用NaOH溶液吸收 ,该反应的离子方程式是
,该反应的离子方程式是_______ 。
II.硫酰氯( )的熔点为-54.1℃,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量白雾,100℃以上分解生成
)的熔点为-54.1℃,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量白雾,100℃以上分解生成 和
和 ,实验室合成
,实验室合成 的原理:
的原理:
 ,实验装置如图所示(部分夹持装置略去),请回答下列问题:
,实验装置如图所示(部分夹持装置略去),请回答下列问题:

(3)A、B干燥管中盛有的物质可以分别是下列_______(填标号)。
(4)去除丙装置可能会发生的副反应是_______ (用化学方程式表示)。
(5)为了测定 产品纯度(杂质不参与反应),称取m g
产品纯度(杂质不参与反应),称取m g  产品于锥形瓶中,加入足量蒸馏水,充分反应。滴加几滴指示剂,用c
产品于锥形瓶中,加入足量蒸馏水,充分反应。滴加几滴指示剂,用c 
 溶液滴定反应后的溶液中
溶液滴定反应后的溶液中 的含量,终点时消耗
的含量,终点时消耗 溶液的平均体积为V mL。已知:
溶液的平均体积为V mL。已知:
①根据上表中各种物质的 ,该实验应选择的指示剂为
,该实验应选择的指示剂为_______ (从下列选项中选择,填标号),滴定终点的现象是_______ 。
A. B.
B. C.
C. D.KBr
D.KBr
②该 产品的纯度为
产品的纯度为_______ %。
 )和硫酰氯(
)和硫酰氯( )都是重要的化工原料,均易水解
)都是重要的化工原料,均易水解I.亚硫酰氯(
 )又名氯化亚钒,熔点为-105℃,沸点为77℃,遇水剧烈反应,产生大量白雾,并生成刺激性气味的气体。
)又名氯化亚钒,熔点为-105℃,沸点为77℃,遇水剧烈反应,产生大量白雾,并生成刺激性气味的气体。(1)用硫磺、液氯和
 为原料,在一定条件下合成
为原料,在一定条件下合成 ,原子利用率可达100%,则三者的物质的量之比为
,原子利用率可达100%,则三者的物质的量之比为(2)
 水解后无残留物,是较好的脱水剂。某同学设计实验将
水解后无残留物,是较好的脱水剂。某同学设计实验将 和
和 混合物加热来制取无水
混合物加热来制取无水 。
。①
 在该实验中作脱水剂的作用是
在该实验中作脱水剂的作用是②实验室常用NaOH溶液吸收
 ,该反应的离子方程式是
,该反应的离子方程式是II.硫酰氯(
 )的熔点为-54.1℃,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量白雾,100℃以上分解生成
)的熔点为-54.1℃,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量白雾,100℃以上分解生成 和
和 ,实验室合成
,实验室合成 的原理:
的原理:
 ,实验装置如图所示(部分夹持装置略去),请回答下列问题:
,实验装置如图所示(部分夹持装置略去),请回答下列问题:
(3)A、B干燥管中盛有的物质可以分别是下列_______(填标号)。
| A.碱石灰、浓硫酸 | B.氯化钙、碱石灰 | C.碱石灰、五氧化二磷 | D.碱石灰、碱石灰 |
(5)为了测定
 产品纯度(杂质不参与反应),称取m g
产品纯度(杂质不参与反应),称取m g  产品于锥形瓶中,加入足量蒸馏水,充分反应。滴加几滴指示剂,用c
产品于锥形瓶中,加入足量蒸馏水,充分反应。滴加几滴指示剂,用c 
 溶液滴定反应后的溶液中
溶液滴定反应后的溶液中 的含量,终点时消耗
的含量,终点时消耗 溶液的平均体积为V mL。已知:
溶液的平均体积为V mL。已知:| 物质 |  | AgCl |  |  | AgBr |
 | 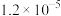 |  |  | 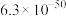 |  |
| 颜色 | 白色 | 白色 | 砖红色 | 黑色 | 浅黄色 |
 ,该实验应选择的指示剂为
,该实验应选择的指示剂为A.
 B.
B. C.
C. D.KBr
D.KBr②该
 产品的纯度为
产品的纯度为
您最近一年使用:0次
2022-11-08更新
|
493次组卷
|
3卷引用:陕西省西安市西北工业大学附属中学2023-2024学年高二上学期期中考试化学试题
5 . 苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:
 + H2O+H2SO4
+ H2O+H2SO4
 +NH4HSO4
+NH4HSO4
 +Cu(OH)2→(
+Cu(OH)2→( )2Cu+H2O
)2Cu+H2O
制备苯乙酸的装置示意图如下(加热和夹持装置等略):

已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
__________________________ 。
(2)将a中的溶液加热至100℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130℃继续反应。在装置中,仪器b的作用是_____________________ ;仪器c的名称是______________ ,其作用是___________________________________________ 。
反应结束后加适量冷水,再分离出苯乙酸粗品。加入冷水的目的是____________ 。下列仪器中可用于分离苯乙酸粗品的是________________ (填标号)。
(3)提纯粗苯乙酸的方法是_____________ ,最终得到44 g纯品,则苯乙酸的产率是________ 。
(4)用CuCl2• 2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是____________________________________________ 。
(5)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是___________________ 。
 + H2O+H2SO4
+ H2O+H2SO4
 +NH4HSO4
+NH4HSO4 +Cu(OH)2→(
+Cu(OH)2→( )2Cu+H2O
)2Cu+H2O制备苯乙酸的装置示意图如下(加热和夹持装置等略):

已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
(2)将a中的溶液加热至100℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130℃继续反应。在装置中,仪器b的作用是
反应结束后加适量冷水,再分离出苯乙酸粗品。加入冷水的目的是
| A.分液漏斗 | B.漏斗 | C.烧杯 | D.直形冷凝管E.玻璃棒 |
(3)提纯粗苯乙酸的方法是
(4)用CuCl2• 2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是
(5)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是
您最近一年使用:0次
2019-01-30更新
|
3820次组卷
|
18卷引用:湖北省武汉中学2022-2023学年高二下学期5月月考化学试题
湖北省武汉中学2022-2023学年高二下学期5月月考化学试题2015-2016学年陕西西安铁一中学高二下开学考试化学试卷2015-2016学年山西省怀仁一中高二下第二次月考化学试卷2014-2015学年湖南省双峰一中高二下期中理科化学试卷广西南宁市第三中学2019-2020学年高二上学期期中考试化学(理)试题第三章 烃的含氧衍生物——B 拓展区 综合拓展(人教版选修5)重庆市主城区七校2019-2020学年高二下学期期末联考化学试题黑龙江省哈尔滨市哈师大附中2020-2021学年高二下学期期中考试化学试题(已下线)第一章 有机化合物的结构特点与研究方法 章末测试(A)-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修3)福建省莆田第一中学2021-2022学年高二上学期期中考试化学试题甘肃省永昌县第一高级中学2021-2022学年高二下学期期末考试化学试题2014年全国普通高等学校招生统一考试理科综合能力测试化学(全国大纲卷)(已下线)2013-2014江西省临川一中高一下学期期末考试化学试卷(已下线)2013-2014学年江西省临川一中高一(下)期末考试化学试卷2016届黑龙江省哈尔滨三中高三上第三次检测理综化学试卷会做实验2020届高三化学实验复习——过滤、蒸馏、冷凝、洗气装置的创新应用【选择15+有机工艺10题突破】(已下线)解密12 实验化学(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密13 实验化学(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)
6 . 叠氮化钠(NaN3)是一种重要的化工产品,可用于合成抗生素头孢菌素药物和用作汽车安全气囊的气源。实验室可通过以下流程制备叠氮化钠并测定其纯度。
Ⅰ.制备氨基钠(反应原理为:2Na+2NH3 2NaNH2+H2)实验装置如图。
2NaNH2+H2)实验装置如图。

已知:氨基钠极易与水剧烈反应生成氨气,且其易被空气氧化。
(1)仪器a的名称为___________ ,实验开始时,应先打开分液漏斗使浓氨水流下,目的是_________ 。
(2)B装置中的药品可选用___________。
(3)若无B装置,C中生成的氨基钠会发生的反应为___________ (用化学方程式表示)。
(4)某同学认为上述实验设计有缺陷,请指出问题,并对装置提出改正措施___________ 。
Ⅱ.制备NaN3
(5)将Ⅰ中制备的NaNH2与N2O在210-220℃的条件下反应生成NaN3、NaOH和氨气,反应容器不选用玻璃材质(SiO2),请用化学方程式说明不选用玻璃材质的原因___________ 。
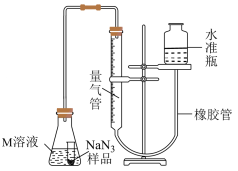
Ⅲ.测定NaN3的纯度水
精确称量0.1500g NaN3样品,设计如图乙所示装置,连接好装置后使锥形瓶倾斜,使小试管中的NaN3样品与M溶液接触,测量产生的气体体积从而测定其纯度(不考虑溶剂的挥发),已知:2NaN3~3N2(其他产物略),反应中放出大量的热。
(6)反应后对水量气管读数时,应注意
①___________
②调节量气管和水准瓶中的液面相平
③视线平视凹液面
(7)常温下测得产生气体的体积为54.00mL(N2的密度为1.400g/L),计算NaN3样品的纯度为(质量分数)___________ 。
(8)假定其他操作均正确,分析下列因素对实验结果的影响。
①读取初始体积时,量气管中的液面低于水准瓶中的液面___________ (填“偏大”、“偏小”或“无影响”,下同);
②实验前未将装置内的空气排出___________ ;
③读取最终体积时仰视___________ 。
Ⅰ.制备氨基钠(反应原理为:2Na+2NH3
 2NaNH2+H2)实验装置如图。
2NaNH2+H2)实验装置如图。
已知:氨基钠极易与水剧烈反应生成氨气,且其易被空气氧化。
(1)仪器a的名称为
(2)B装置中的药品可选用___________。
| A.P2O5 | B.碱石灰 | C.无水硫酸铜 | D.无水氯化钙 |
(3)若无B装置,C中生成的氨基钠会发生的反应为
(4)某同学认为上述实验设计有缺陷,请指出问题,并对装置提出改正措施
Ⅱ.制备NaN3
(5)将Ⅰ中制备的NaNH2与N2O在210-220℃的条件下反应生成NaN3、NaOH和氨气,反应容器不选用玻璃材质(SiO2),请用化学方程式说明不选用玻璃材质的原因

Ⅲ.测定NaN3的纯度水
精确称量0.1500g NaN3样品,设计如图乙所示装置,连接好装置后使锥形瓶倾斜,使小试管中的NaN3样品与M溶液接触,测量产生的气体体积从而测定其纯度(不考虑溶剂的挥发),已知:2NaN3~3N2(其他产物略),反应中放出大量的热。
(6)反应后对水量气管读数时,应注意
①
②调节量气管和水准瓶中的液面相平
③视线平视凹液面
(7)常温下测得产生气体的体积为54.00mL(N2的密度为1.400g/L),计算NaN3样品的纯度为(质量分数)
(8)假定其他操作均正确,分析下列因素对实验结果的影响。
①读取初始体积时,量气管中的液面低于水准瓶中的液面
②实验前未将装置内的空气排出
③读取最终体积时仰视
您最近一年使用:0次
7 . 据公安部统计,截至2023年6月底,成都汽车保有量超过600万辆,仅次于北京,居全国第二、高密度的车辆行驶,容易引发交通事故,若车辆受到相对较大撞击,就会引起安全气囊弹出,从而保护车内乘客。叠氮化钠是汽车安全气囊内的重要填充物质。某化学兴趣小组根据工业制备叠氮化钠(NaN3)的方法在实验室设计出制备该物质的装置如下:
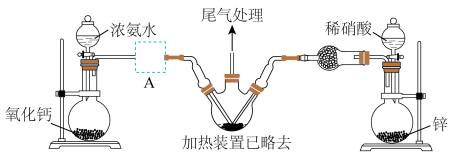
已知:ⅰ.工业上制备 的原理分两步进行:
的原理分两步进行:
①将 通入熔融状态的Na中先制得
通入熔融状态的Na中先制得 ,
,
②将 与
与 加热至
加热至 左右合成
左右合成 ,在合成过程中,易发生副反应:
,在合成过程中,易发生副反应: ;
;
ⅱ. 和
和 的性质如下表:
的性质如下表:
ⅲ. 属于危险化学药品,工业上一般用NaClO销毁剩余
属于危险化学药品,工业上一般用NaClO销毁剩余 ;
;
ⅳ. 与
与 离子反应产生鲜明的血红色,此反应非常灵敏。
离子反应产生鲜明的血红色,此反应非常灵敏。
回答下列问题:
(1)盛装浓氨水的仪器的名称是___________ 。
(2)连接好装置之后,应进行的操作是___________ 。
(3)实验室用 和稀硝酸反应制备
和稀硝酸反应制备 ,其离子方程式为
,其离子方程式为___________ 。
(4)图中虚线框处应选用的装置是___________ (填标号)。

(5)安全气囊中填充 的理由是
的理由是___________ 。
(6)在销毁多余 时会有
时会有 和
和 生成,该反应的化学方程式为
生成,该反应的化学方程式为___________ ;如何检测销毁是否彻底,请提供一种检测方法:___________ 。

已知:ⅰ.工业上制备
 的原理分两步进行:
的原理分两步进行:①将
 通入熔融状态的Na中先制得
通入熔融状态的Na中先制得 ,
,②将
 与
与 加热至
加热至 左右合成
左右合成 ,在合成过程中,易发生副反应:
,在合成过程中,易发生副反应: ;
;ⅱ.
 和
和 的性质如下表:
的性质如下表:| 物质 |  |  |
| 性质 | 白色固体,易溶于水,有一定危险性,受撞击易快速分解出一种无色、无味、无毒的气体,且有固体Na生成。 | 无色、有甜味的气体,有轻微麻醉作用,常用于医疗,有一定氧化性。 |
 属于危险化学药品,工业上一般用NaClO销毁剩余
属于危险化学药品,工业上一般用NaClO销毁剩余 ;
;ⅳ.
 与
与 离子反应产生鲜明的血红色,此反应非常灵敏。
离子反应产生鲜明的血红色,此反应非常灵敏。回答下列问题:
(1)盛装浓氨水的仪器的名称是
(2)连接好装置之后,应进行的操作是
(3)实验室用
 和稀硝酸反应制备
和稀硝酸反应制备 ,其离子方程式为
,其离子方程式为(4)图中虚线框处应选用的装置是

(5)安全气囊中填充
 的理由是
的理由是(6)在销毁多余
 时会有
时会有 和
和 生成,该反应的化学方程式为
生成,该反应的化学方程式为
您最近一年使用:0次
解题方法
8 . 阿司匹林(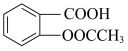 )是被广泛应用的解热镇痛和抗凝药。在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O] 为主要原料合成阿司匹林,设计如下实验步骤:
)是被广泛应用的解热镇痛和抗凝药。在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O] 为主要原料合成阿司匹林,设计如下实验步骤:
①取反应物:取适量水杨酸、醋酸酐、浓硫酸加入反应容器,混合摇匀;
②合成:控制温度为85°C ~90°C加热10分钟后,冷却反应液、过滤、洗涤得粗产品;
③提纯。
已知:
请根据以上信息回答下列问题:
(1)取反应物前应先向反应容器中加入_______ 。
(2)合成应在_______ (填“无水”或“有水”)条件下进行,最合适的加热方法是_______ 。
(3)冷却反应液后,发现无晶体析出,此时可采取的措施是_______ 。
(4)I.提纯时,先加入少量的NaHCO3溶液后过滤,再向固体中加盐酸酸化,冷却、过滤、洗涤、干燥后得到较纯的阿司匹林。判断洗涤干净的方法是_______ 。
II.另一种提纯方法是将粗产品与乙酸乙酯、沸石混合后加热回流,趁热过滤、冷却过滤、洗涤干燥。其中回流的装置如图所示:

①使用温度计的目的是_______ 。
②乙酸乙酯的作用是_______ ,该方法所得产品中有机杂质要比方案I少,原因是_______ 。
 )是被广泛应用的解热镇痛和抗凝药。在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O] 为主要原料合成阿司匹林,设计如下实验步骤:
)是被广泛应用的解热镇痛和抗凝药。在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O] 为主要原料合成阿司匹林,设计如下实验步骤:①取反应物:取适量水杨酸、醋酸酐、浓硫酸加入反应容器,混合摇匀;
②合成:控制温度为85°C ~90°C加热10分钟后,冷却反应液、过滤、洗涤得粗产品;
③提纯。
已知:
| 名称 | 相对分子质量 | 相关性质 |
| 水杨酸 | 138 | 熔点15°C,微溶于水 |
| 醋酸酐 | 102 | 沸点139.4°C,与水激烈反应生成醋酸 |
| 乙酰水杨酸 | 180 | 熔点135°C,128~ 135°C分解,微溶于水 |
(1)取反应物前应先向反应容器中加入
(2)合成应在
(3)冷却反应液后,发现无晶体析出,此时可采取的措施是
(4)I.提纯时,先加入少量的NaHCO3溶液后过滤,再向固体中加盐酸酸化,冷却、过滤、洗涤、干燥后得到较纯的阿司匹林。判断洗涤干净的方法是
II.另一种提纯方法是将粗产品与乙酸乙酯、沸石混合后加热回流,趁热过滤、冷却过滤、洗涤干燥。其中回流的装置如图所示:

①使用温度计的目的是
②乙酸乙酯的作用是
您最近一年使用:0次
2023-05-03更新
|
1005次组卷
|
5卷引用:第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)
(已下线)第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)云南省“3+3+3”2023届高三下学期诊断性联考二模理综化学试题(已下线)考点巩固卷13 化学实验基础(二)(3个考点30题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)第33讲认识有机化合物(已下线)考点1 认识有机化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
名校
解题方法
9 . 甲基丙烯酸甲酯是合成有机玻璃的单体,有关物质的性质如下:
某小组拟制备甲基丙烯酸甲酯并探究其性质,装置如图所示(夹持及加热仪器略)。

向三颈瓶中依次加入20 mL甲醇、5 mL浓硫酸、30 mL甲基丙烯酸及沸石少许,充分搅拌,加热。
(1)向其中加入沸石的目的是___________ 。
(2)使用油水分离器的作用是___________ 。
(3)实验结束后,提纯产品的流程如下:
混合液 产品
产品
①水洗2的目的是___________ 。
②加入硫酸钠粉末的作用是___________ 。
③蒸馏操作中收集产品的温度约为___________ 。
(4)设计简单实验检验产品中含碳碳双键:___________ 。
(5)甲基丙烯酸甲酯另一种合成方法为 ,已知该反应的原子利用率为100%,则A的结构简式为
,已知该反应的原子利用率为100%,则A的结构简式为___________ 。
| 物质 | 沸点/℃ | 溶解性 |
| 甲醇 | 64.7 | 易溶于水和有机溶剂 |
甲基丙烯酸 | 161 | 溶于水,易溶于有机溶剂 |
| 甲基丙烯酸甲酯 | 100 | 易溶于有机溶剂,微溶于水 |

向三颈瓶中依次加入20 mL甲醇、5 mL浓硫酸、30 mL甲基丙烯酸及沸石少许,充分搅拌,加热。
(1)向其中加入沸石的目的是
(2)使用油水分离器的作用是
(3)实验结束后,提纯产品的流程如下:
混合液
 产品
产品①水洗2的目的是
②加入硫酸钠粉末的作用是
③蒸馏操作中收集产品的温度约为
(4)设计简单实验检验产品中含碳碳双键:
(5)甲基丙烯酸甲酯另一种合成方法为
 ,已知该反应的原子利用率为100%,则A的结构简式为
,已知该反应的原子利用率为100%,则A的结构简式为
您最近一年使用:0次
解题方法
10 . 乳酸薄荷醇酯广泛应用于化妆品和食品等行业中。实验室以薄荷醇( )和乳酸(
)和乳酸( )为原料直接反应制备乳酸薄荷醇酯的化学方程式为
)为原料直接反应制备乳酸薄荷醇酯的化学方程式为 。
。
主要实验装置示意图和有关数据如表:

实验步骤如下:
I.合成:在带有温度计、分水器、搅拌器的250mL三颈烧瓶中加入薄荷醇15.6g、90%乳酸23.5g、浓硫酸0.1g、甲苯50g,加热到100℃,加热回流2.5h。
Ⅱ.分离与提纯:降温冷却后放出水层,有机层与反应液合并,将合并液分别用20mL10%碳酸钠溶液洗涤两次、去离子水洗涤两次,干燥,减压蒸馏,得到产品13.7g。回答下列问题:
(1)仪器a的名称是__________ ,在以上“合成”步骤中需控制反应温度为100℃的原因可能是__________ 。
(2)实验中加入过量乳酸的目的是__________ 。
(3)在“分离与提纯”步骤中,水层应从分液漏斗的__________ (填“上口”或“下口”)放出,用碳酸钠溶液洗涤的主要目的是__________ 。
(4)“减压蒸馏”的目的是__________ 。
 )和乳酸(
)和乳酸( )为原料直接反应制备乳酸薄荷醇酯的化学方程式为
)为原料直接反应制备乳酸薄荷醇酯的化学方程式为 。
。主要实验装置示意图和有关数据如表:

| 物质 | 乳酸 | 薄荷醇 | 乳酸薄荷醇酯 | 甲苯 |
| 相对分子质量 | 90 | 156 | 228 | 92 |
| 密度/(g·cm-3) | 1.25 | 0.89 | 0.976 | 0.89 |
| 熔点/℃ | 16.8 | 43 | -47 | -94.9 |
| 沸点/℃ | 122 | 103 | 142 | 110.6 |
| 溶解性 | 易溶水和有机溶剂 | 微溶于水,易溶于有机溶剂 | 微溶于水,易溶于有机溶剂 | 不溶于水 |
I.合成:在带有温度计、分水器、搅拌器的250mL三颈烧瓶中加入薄荷醇15.6g、90%乳酸23.5g、浓硫酸0.1g、甲苯50g,加热到100℃,加热回流2.5h。
Ⅱ.分离与提纯:降温冷却后放出水层,有机层与反应液合并,将合并液分别用20mL10%碳酸钠溶液洗涤两次、去离子水洗涤两次,干燥,减压蒸馏,得到产品13.7g。回答下列问题:
(1)仪器a的名称是
(2)实验中加入过量乳酸的目的是
(3)在“分离与提纯”步骤中,水层应从分液漏斗的
(4)“减压蒸馏”的目的是
您最近一年使用:0次



