名校
解题方法
1 . 海带中既含有有机碘化合物又含有碘化钠等无机碘化合物。某课题组探究了海带提碘的优化条件,并用色度计测定了某海带样品中碘的含量。实验步骤:
I.预处理:将干海带刷净,剪成 大小的方块,准确称量
大小的方块,准确称量 样品。
样品。
II.灰化:在仪器A中加热干海带,并用玻璃棒不断搅拌,记录加热时间,停止加热,冷却。
III.过滤:将冷却后的海带灰转移到 烧杯中,加入
烧杯中,加入 蒸馏水,静置后过滤。
蒸馏水,静置后过滤。
IV.氧化:向滤液中加入稀 和
和 溶液,充分反应后将滤液转移到分液漏斗中。
溶液,充分反应后将滤液转移到分液漏斗中。
V.萃取:向分液漏斗中加入 ,振荡,静置。待溶液完全分层后,取下层溶液。
,振荡,静置。待溶液完全分层后,取下层溶液。
VI.含量测定:用色度计测定出所得溶液中碘的含量。
VII.回收处理:蒸馏碘的 溶液,回收
溶液,回收
已知:海带灰化后,碘元素以 的形式存在。
的形式存在。
回答下列问题:
(1)第II步中的仪器A是___________ 。
(2)证明第III步滤液中存在 的实验方法是
的实验方法是___________ ,实验现象是___________ 。
(3)第IV步氧化过程中发生反应的离子方程式为___________ 。
(4)第V步可得到 的
的 溶液,也可用如下流程从其中回收
溶液,也可用如下流程从其中回收 :
:
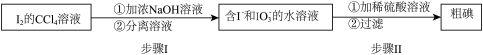
请写出步骤II的离子方程式:___________ 。
(5)碘浓度越大吸光度越大。用色度计测得某碘溶液的吸光度后,利用以溶液吸光度为纵坐标,碘浓度(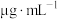 )为横坐标的标准曲线图,可以得出被测溶液碘浓度。为了绘制标准曲线图,取
)为横坐标的标准曲线图,可以得出被测溶液碘浓度。为了绘制标准曲线图,取 碘单质,用
碘单质,用 容量瓶配成碘的
容量瓶配成碘的 溶液,取出
溶液,取出 加入一定量
加入一定量 中配得第一份碘的标准溶液
中配得第一份碘的标准溶液 。用色度计测其吸光度,得到标准曲线的第一个坐标点,该坐标点的横坐标是
。用色度计测其吸光度,得到标准曲线的第一个坐标点,该坐标点的横坐标是___________ 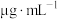 。
。
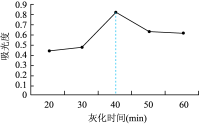
(6)课题组在其他实验条件相同情况下,研究了不同灰化时间对碘提取效果的影响,其结果如图所示。灰化时间超过40min,测得碘的含量逐渐降低,原因是___________ 。
I.预处理:将干海带刷净,剪成
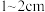 大小的方块,准确称量
大小的方块,准确称量 样品。
样品。II.灰化:在仪器A中加热干海带,并用玻璃棒不断搅拌,记录加热时间,停止加热,冷却。
III.过滤:将冷却后的海带灰转移到
 烧杯中,加入
烧杯中,加入 蒸馏水,静置后过滤。
蒸馏水,静置后过滤。IV.氧化:向滤液中加入稀
 和
和 溶液,充分反应后将滤液转移到分液漏斗中。
溶液,充分反应后将滤液转移到分液漏斗中。V.萃取:向分液漏斗中加入
 ,振荡,静置。待溶液完全分层后,取下层溶液。
,振荡,静置。待溶液完全分层后,取下层溶液。VI.含量测定:用色度计测定出所得溶液中碘的含量。
VII.回收处理:蒸馏碘的
 溶液,回收
溶液,回收
已知:海带灰化后,碘元素以
 的形式存在。
的形式存在。回答下列问题:
(1)第II步中的仪器A是
(2)证明第III步滤液中存在
 的实验方法是
的实验方法是(3)第IV步氧化过程中发生反应的离子方程式为
(4)第V步可得到
 的
的 溶液,也可用如下流程从其中回收
溶液,也可用如下流程从其中回收 :
:
请写出步骤II的离子方程式:
(5)碘浓度越大吸光度越大。用色度计测得某碘溶液的吸光度后,利用以溶液吸光度为纵坐标,碘浓度(
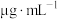 )为横坐标的标准曲线图,可以得出被测溶液碘浓度。为了绘制标准曲线图,取
)为横坐标的标准曲线图,可以得出被测溶液碘浓度。为了绘制标准曲线图,取 碘单质,用
碘单质,用 容量瓶配成碘的
容量瓶配成碘的 溶液,取出
溶液,取出 加入一定量
加入一定量 中配得第一份碘的标准溶液
中配得第一份碘的标准溶液 。用色度计测其吸光度,得到标准曲线的第一个坐标点,该坐标点的横坐标是
。用色度计测其吸光度,得到标准曲线的第一个坐标点,该坐标点的横坐标是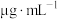 。
。(6)课题组在其他实验条件相同情况下,研究了不同灰化时间对碘提取效果的影响,其结果如图所示。灰化时间超过40min,测得碘的含量逐渐降低,原因是

您最近半年使用:0次
2023-07-03更新
|
139次组卷
|
2卷引用:山西省运城市2022-2023学年高一下学期期末考试化学试题
解题方法
2 . 碘和碘的化合物在有机化学中十分重要,另外在医药和照相方面的用途也很广泛。海带提碘的相关流程如下所示,已知 ,请回答下列问题:
,请回答下列问题:
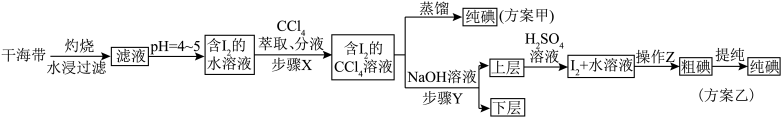
(1)海带灼烧的目的是_______ ;实验室进行此操作用到的主要仪器名称为_______ 。
(2)滤液得到含 的水溶液,除了调节
的水溶液,除了调节 ,还需要加入臭氧或过氧化氢,所加试剂在反应中作
,还需要加入臭氧或过氧化氢,所加试剂在反应中作_______ 剂(填“氧化”或“还原”),写出加入过氧化氢时发生反应的离子方程式:_______ 。
(3)步骤 是否可以用酒精代替
是否可以用酒精代替 ,并说明理由
,并说明理由_______ 。
(4)步骤 的操作为
的操作为_______ 。
(5)上层液体加入 溶液后发生反应的离子方程式为
溶液后发生反应的离子方程式为_______ 。
(6)以上流程中可以循环使用的试剂是_______ 。
(7)加碘食盐中的碘以碘酸钾 形式存在,根据以上信息,可用试纸和一些常见试剂进行检验,证明食盐中存在
形式存在,根据以上信息,可用试纸和一些常见试剂进行检验,证明食盐中存在 。可供选用的物质有:①
。可供选用的物质有:① 试纸、②蓝色石蕊试纸、③碘化钾淀粉试纸、④蒸馏水、⑤食醋、⑥醇,进行上述实验时必须使用的物质是
试纸、②蓝色石蕊试纸、③碘化钾淀粉试纸、④蒸馏水、⑤食醋、⑥醇,进行上述实验时必须使用的物质是_______ (填序号)。
 ,请回答下列问题:
,请回答下列问题:
(1)海带灼烧的目的是
(2)滤液得到含
 的水溶液,除了调节
的水溶液,除了调节 ,还需要加入臭氧或过氧化氢,所加试剂在反应中作
,还需要加入臭氧或过氧化氢,所加试剂在反应中作(3)步骤
 是否可以用酒精代替
是否可以用酒精代替 ,并说明理由
,并说明理由(4)步骤
 的操作为
的操作为(5)上层液体加入
 溶液后发生反应的离子方程式为
溶液后发生反应的离子方程式为(6)以上流程中可以循环使用的试剂是
(7)加碘食盐中的碘以碘酸钾
 形式存在,根据以上信息,可用试纸和一些常见试剂进行检验,证明食盐中存在
形式存在,根据以上信息,可用试纸和一些常见试剂进行检验,证明食盐中存在 。可供选用的物质有:①
。可供选用的物质有:① 试纸、②蓝色石蕊试纸、③碘化钾淀粉试纸、④蒸馏水、⑤食醋、⑥醇,进行上述实验时必须使用的物质是
试纸、②蓝色石蕊试纸、③碘化钾淀粉试纸、④蒸馏水、⑤食醋、⑥醇,进行上述实验时必须使用的物质是
您最近半年使用:0次
名校
3 . 从海产品中提取碘是我国工业上获取碘的重要途径,实验室证明海带中存在碘元素的方法如下:
Ⅰ.取3g左右的干海带,把干海带表面的附着物用刷子刷净,用剪刀剪碎后,用酒精润湿,灼烧至完全变成灰烬。
Ⅱ.将海带灰转移到小烧杯中,向其中加10mL蒸馏水,搅拌、煮沸2~3min,过滤。
Ⅲ.向滤液中加氧化剂氧化,最后检验碘单质的存在。
回答下列问题:
(1)“步骤1”中,灼烧时会用到下列仪器中的_______ (填标号)。
a. b.
b.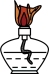 c.
c. d.
d.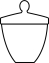
(2)某兴趣小组在实验室完成“步骤Ⅲ”中氧化剂氧化过程,装置如图所示。
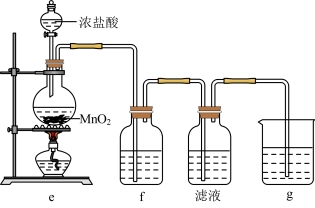
①装置e中发生反应的化学方程式是_______ 。
②装置f、g中所装的试剂分别是_______ 、_______ 。
③检验“滤液”中有碘单质生成的方法是_______ 。若通入 过量,检验发现“滤液”中无碘单质,其原因是
过量,检验发现“滤液”中无碘单质,其原因是_______ 。
(3)“步骤Ⅲ”氧化剂氧化时,用 在pH<2的酸性介质中反应效果最佳。已知还原产物是NO,则反应的离子方程式是
在pH<2的酸性介质中反应效果最佳。已知还原产物是NO,则反应的离子方程式是_______ 。
(4)若“步骤Ⅲ”所得溶液经过分离提纯获得 ,其物质的量是
,其物质的量是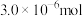 。则干海带中碘元素的含量是
。则干海带中碘元素的含量是_______ mg/kg。
Ⅰ.取3g左右的干海带,把干海带表面的附着物用刷子刷净,用剪刀剪碎后,用酒精润湿,灼烧至完全变成灰烬。
Ⅱ.将海带灰转移到小烧杯中,向其中加10mL蒸馏水,搅拌、煮沸2~3min,过滤。
Ⅲ.向滤液中加氧化剂氧化,最后检验碘单质的存在。
回答下列问题:
(1)“步骤1”中,灼烧时会用到下列仪器中的
a.
 b.
b. c.
c. d.
d.
(2)某兴趣小组在实验室完成“步骤Ⅲ”中氧化剂氧化过程,装置如图所示。

①装置e中发生反应的化学方程式是
②装置f、g中所装的试剂分别是
③检验“滤液”中有碘单质生成的方法是
 过量,检验发现“滤液”中无碘单质,其原因是
过量,检验发现“滤液”中无碘单质,其原因是(3)“步骤Ⅲ”氧化剂氧化时,用
 在pH<2的酸性介质中反应效果最佳。已知还原产物是NO,则反应的离子方程式是
在pH<2的酸性介质中反应效果最佳。已知还原产物是NO,则反应的离子方程式是(4)若“步骤Ⅲ”所得溶液经过分离提纯获得
 ,其物质的量是
,其物质的量是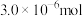 。则干海带中碘元素的含量是
。则干海带中碘元素的含量是
您最近半年使用:0次
2022-07-20更新
|
504次组卷
|
3卷引用:山西省大同市第二中学校2023届高三上学期开学考试化学试题
4 . 某学习小组做了如下实验探究海带中碘元素的存在形式,探究过程如图:
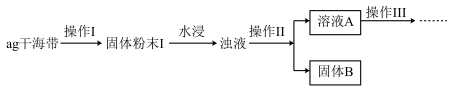
(1)操作I为灼烧,则灼烧时应该用___ (仪器名称)盛装海带,操作II为___ ;
(2)水浸时通常要将悬浊液煮沸2-3min,目的是___ 。
(3)操作III,是同学们对溶液A中碘元素的存在形式进行的探究实验。
推测:①以IO 形式存在②以I-形式存在
形式存在②以I-形式存在
查阅资料:IO 具有较强的氧化性将上述溶液稀释配制成200mL溶液,请完成下列实验探究。
具有较强的氧化性将上述溶液稀释配制成200mL溶液,请完成下列实验探究。
限选试剂:3%H2O2溶液、KSCN溶液、FeC12溶液、稀硫酸
(4)取20mL稀释后溶液A于锥形瓶,滴加0.01mol/LKMnO4溶液至溶液刚显浅红色,将I-氧化为I2并得到溶液B;已知在酸性条件下,MnO 的还原产物为Mn2+,写出离子方程式
的还原产物为Mn2+,写出离子方程式___ 。

(1)操作I为灼烧,则灼烧时应该用
(2)水浸时通常要将悬浊液煮沸2-3min,目的是
(3)操作III,是同学们对溶液A中碘元素的存在形式进行的探究实验。
推测:①以IO
 形式存在②以I-形式存在
形式存在②以I-形式存在查阅资料:IO
 具有较强的氧化性将上述溶液稀释配制成200mL溶液,请完成下列实验探究。
具有较强的氧化性将上述溶液稀释配制成200mL溶液,请完成下列实验探究。限选试剂:3%H2O2溶液、KSCN溶液、FeC12溶液、稀硫酸
| 序号 | 实验操作 | 实验现象 | 结论 |
| ① | 取少量稀释后的溶液A加入淀粉后再 用硫酸酸化,分装于试管I、II | 无现象 | |
| ② | 往试管I中加入FeC12溶液,然后加入2滴KSCN溶液并振荡; | 证明不是以IO 形式存在 形式存在 | |
| ③ | 往试管II中加入 | 证明以I-形式存在 |
(4)取20mL稀释后溶液A于锥形瓶,滴加0.01mol/LKMnO4溶液至溶液刚显浅红色,将I-氧化为I2并得到溶液B;已知在酸性条件下,MnO
 的还原产物为Mn2+,写出离子方程式
的还原产物为Mn2+,写出离子方程式
您最近半年使用:0次
解题方法
5 . 海带提碘过程中以 为溶剂将
为溶剂将 从碘水溶液中提取出来,通过下列实验可从
从碘水溶液中提取出来,通过下列实验可从 的
的 溶液中回收
溶液中回收 。
。

下列说法错误的是
 为溶剂将
为溶剂将 从碘水溶液中提取出来,通过下列实验可从
从碘水溶液中提取出来,通过下列实验可从 的
的 溶液中回收
溶液中回收 。
。
下列说法错误的是
| A.以海带为原料得到碘水溶液的主要实验步骤:取样→灼烧→溶解→过滤 |
B.NaOH溶液与 反应的离子方程式: 反应的离子方程式: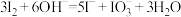 |
| C.过滤需要用到的玻璃仪器有玻璃棒、烧杯和漏斗 |
| D.回收的粗碘可通过升华进行纯化 |
您最近半年使用:0次
6 . 下列自然资源的开发利用中,说法正确的是
A.海水经萃取、蒸馏可提取 |
B.海带  I2 I2 |
C.从海水中可以得到NaCl,电解熔融NaCl可制备 |
| D.石油经分馏、裂解得到苯、甲苯、二甲苯、酚等 |
您最近半年使用:0次
7 . 从海产品(如海带)中提取碘是工业获取碘的重要途径。其流程如下:

下列说法中不正确的是

下列说法中不正确的是
| A.碘元素在海带中以游离态存在 |
| B.使海带中的碘进入水中也可将海带灼烧成灰再加水浸取 |
C.用 代替 代替 不会产生污染,且能防止 不会产生污染,且能防止 被进一步氧化 被进一步氧化 |
| D.碘单质容易华,可以利用升华法提纯含有氯化钠杂质的碘单质 |
您最近半年使用:0次
名校
8 . 下列说法不正确 的是
| A.工业制备硝酸的主要设备为热交换器、接触室和吸收塔 |
| B.工业炼铁时,铁矿石和焦炭从炼铁高炉的上口加入 |
| C.从海带中提取碘的工业生产步骤:浸泡→碱化→过滤→氧化→结晶→过滤→提纯 |
| D.玻璃是将石灰石、纯碱、石英在玻璃熔炉中高温熔融制得的 |
您最近半年使用:0次
2022-05-23更新
|
1460次组卷
|
4卷引用:山西省晋中市祁县中学2022-2023学年高三上学期10月月考化学试题
山西省晋中市祁县中学2022-2023学年高三上学期10月月考化学试题浙江省宁波市鄞州中学2021~2022学年高三下学期高考考前测试化学试题(已下线)第16讲 金属材料与合金(讲义)-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )(已下线)化学预测卷(八)-预测卷(浙江专版)
9 . 下列有关说法错误的是
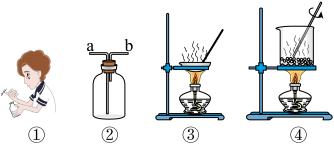

| A.图①是表示嗅闻某种气体气味的方法 |
| B.图②既可用于收集SO2也可用于收集H2 |
| C.图③可用于从Na2CO3溶液中分离出溶质 |
| D.图④可用于灼烧海带 |
您最近半年使用:0次
2020-10-28更新
|
149次组卷
|
3卷引用:山西省运城市高中联合体2021届高三上学期10月阶段检测化学试题
名校
10 . 用高分子吸附树脂提取卤水中的碘(主要以I-形式存在)的工艺流程如图,说法错误的是
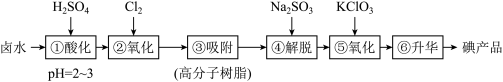

| A.流程②的反应说明Ⅰ的非金属性弱于Cl |
| B.经①和④所得溶液中,I-的浓度后者大于前者 |
| C.氯元素的相对原子质量是35.5,则存在的35Cl、37Cl所占的百分比约为3:1 |
| D.若在流程②和⑤中要得到等量的I2,则需消耗的n(Cl2):n(KClO3)=5:2 |
您最近半年使用:0次



