名校
1 . 碘是国防、工业、农业、医药等部门和行业所依赖的重要原料,海水提碘是从海藻中提取元素碘的技术。
Ⅰ.海带提碘(海带中碘元素以I-形式存在)
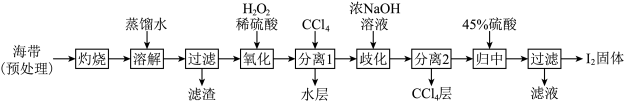
(1)“氧化”过程涉及到的离子方程式是________ ,请设计一种检验氧化后所得溶液含I2的方法:________ 。
(2)加入浓NaOH溶液充分振荡,发生的歧化反应中氧化剂和还原剂物质的量之比为________ ;向分离得到的含I-和 的水溶液中加入45%硫酸,发生归中反应的离子方程式为
的水溶液中加入45%硫酸,发生归中反应的离子方程式为________ 。
Ⅱ.获取重要的还原剂-HI
(3)H2和I2反应生成HI过程能量变化如图所示,1molH2(g)、1molHI(g)分子中化学键断裂时分别要吸收能量436kJ、299kJ,则1molI2(g)分子中化学键断裂时需吸收的能量为________ kJ。

(4)Bodensteins研究了反应: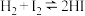 。温度为T时,在体积均为10L的密闭容器中进行实验,测得气体混合物中氢气的物质的量与反应时间t的关系如表:
。温度为T时,在体积均为10L的密闭容器中进行实验,测得气体混合物中氢气的物质的量与反应时间t的关系如表:
前40min的平均速率v(HI)=________ 。
Ⅲ.生命延续-心脏起搏器中的Li-I2电池
(5)优质的锂碘电池可用于心脏起搏器延续患者的生命,它的正极材料是聚2-乙烯吡啶(简写P2VP)和I2的复合物,电解质是固态薄膜状的碘化锂,电池的总反应为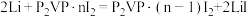 ,其工作原理如图所示:
,其工作原理如图所示:
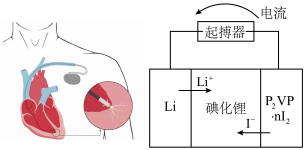
①正极发生的电极反应式为________ ;
②放电时,转移0.6×6.02×1023个电子,负极质量减少________ g。
Ⅰ.海带提碘(海带中碘元素以I-形式存在)

(1)“氧化”过程涉及到的离子方程式是
(2)加入浓NaOH溶液充分振荡,发生的歧化反应中氧化剂和还原剂物质的量之比为
 的水溶液中加入45%硫酸,发生归中反应的离子方程式为
的水溶液中加入45%硫酸,发生归中反应的离子方程式为Ⅱ.获取重要的还原剂-HI
(3)H2和I2反应生成HI过程能量变化如图所示,1molH2(g)、1molHI(g)分子中化学键断裂时分别要吸收能量436kJ、299kJ,则1molI2(g)分子中化学键断裂时需吸收的能量为

(4)Bodensteins研究了反应:
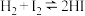 。温度为T时,在体积均为10L的密闭容器中进行实验,测得气体混合物中氢气的物质的量与反应时间t的关系如表:
。温度为T时,在体积均为10L的密闭容器中进行实验,测得气体混合物中氢气的物质的量与反应时间t的关系如表:| 起始物质 | t/min | 0 | 20 | 40 | 60 | 80 |
| 1molH2(g)、1molI2(g) | n(H2)mol | 1 | 0.5 | 0.32 | 0.24 | 0.20 |
Ⅲ.生命延续-心脏起搏器中的Li-I2电池
(5)优质的锂碘电池可用于心脏起搏器延续患者的生命,它的正极材料是聚2-乙烯吡啶(简写P2VP)和I2的复合物,电解质是固态薄膜状的碘化锂,电池的总反应为
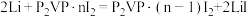 ,其工作原理如图所示:
,其工作原理如图所示:
①正极发生的电极反应式为
②放电时,转移0.6×6.02×1023个电子,负极质量减少
您最近一年使用:0次
名校
2 . 海带、紫菜等藻类植物富含以碘化物形式存在的碘元素,以保护自身在退潮时不受空气中少量臭氧(O3)的影响。下列流程可以从海带中提取碘单质:

(1)灼烧的目的是___________ ;操作③名称是___________ ;
(2)④中发生反应的离子方程式为___________ ;除了H2O2外,还能完成此步转化的有___________ ;
a.Cl2 b.SO2 c.O2 d.FeCl2溶液
(3)⑤需要用的主要玻璃仪器有___________ ,静置分层后,可以看到上层溶液呈___________ 色,下层溶液呈___________ 色,若想尽可能多地将I2从水中提取到有机层中,下列操作可行的有___________ ;
a.充分振荡 b.多次萃取 c.换用酒精作为萃取剂
(4)我省深居内陆,居民可通过食用加碘食盐的方式补充碘元素的摄入,要测定食盐中的碘元素(以KIO3形式存在),可在酸性条件下加入KI将其转化为I2进行定量检测,该转化的离子方程式为___________ 。

(1)灼烧的目的是
(2)④中发生反应的离子方程式为
a.Cl2 b.SO2 c.O2 d.FeCl2溶液
(3)⑤需要用的主要玻璃仪器有
a.充分振荡 b.多次萃取 c.换用酒精作为萃取剂
(4)我省深居内陆,居民可通过食用加碘食盐的方式补充碘元素的摄入,要测定食盐中的碘元素(以KIO3形式存在),可在酸性条件下加入KI将其转化为I2进行定量检测,该转化的离子方程式为
您最近一年使用:0次



