名校
1 . 海水化学资源开发利用中的提碘、提溴的部分过程如图所示。下列说法正确的是
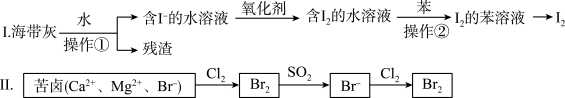
| A.I中操作①用到的玻璃仪器只有烧杯、玻璃棒、胶头滴管 |
| B.I中操作②的苯可用酒精代替 |
C.Ⅱ中SO2与Br2反应的化学方程式为: |
D.Ⅱ中还原性: |
您最近一年使用:0次
2023-04-08更新
|
618次组卷
|
3卷引用:安徽师范大学附属中学2023-2024学年高一下学期3月阶段性教学质量监测化学试题
2 . 溴、碘在科研与生活中有重要作用。
Ⅰ.实验室按如下实验流程提取海带中的碘。
海带→灼烧→溶解→过滤→氧化→萃取、分液→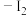 的
的 溶液
溶液
(1)上述实验流程中灼烧用到的仪器是_______ (从下列图中选择,写出名称,下同),萃取分液在_______ 中进行。

(2)“氧化”时加入 和
和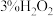 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为_______ 。
(3)检验氧化后的溶液中存在碘单质,可选用的试剂是_______ (填名称)溶液。
Ⅱ.某化学兴趣小组模拟工业上以浓缩海水为原料提取溴的流程设计了如图所示装置进行实验(所有橡胶制品均已被保护,夹持装置已略去)。
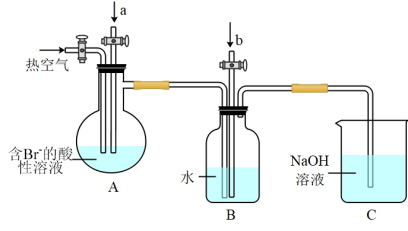
(4)A装置中通入a气体通常为_______ ,发生反应的离子方程式为_______ 。
(5)A装置中通入a气体一段时间后,停止通入,改通入热空气。通入热空气的目的是_______ 。
(6)B装置的作用是收集并还原溴,则气体b为_______ 。
(7)C装置的作用是_______ 。
Ⅰ.实验室按如下实验流程提取海带中的碘。
海带→灼烧→溶解→过滤→氧化→萃取、分液→
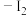 的
的 溶液
溶液(1)上述实验流程中灼烧用到的仪器是

(2)“氧化”时加入
 和
和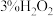 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为(3)检验氧化后的溶液中存在碘单质,可选用的试剂是
Ⅱ.某化学兴趣小组模拟工业上以浓缩海水为原料提取溴的流程设计了如图所示装置进行实验(所有橡胶制品均已被保护,夹持装置已略去)。

(4)A装置中通入a气体通常为
(5)A装置中通入a气体一段时间后,停止通入,改通入热空气。通入热空气的目的是
(6)B装置的作用是收集并还原溴,则气体b为
(7)C装置的作用是
您最近一年使用:0次
名校
解题方法
3 . 海带提碘过程为海带灼烧为海带灰、用水浸取、过滤,所得浸取液中加氧化剂氧化、萃取分液、加NaOH浓溶液反萃取、酸化后过滤得碘单质。上述过程中,用到的玻璃仪器有
①酒精灯、②烧杯、、③坩埚、④分液漏斗、⑤250mL容量瓶、⑥玻璃棒、⑦漏斗、⑧蒸发皿
①酒精灯、②烧杯、、③坩埚、④分液漏斗、⑤250mL容量瓶、⑥玻璃棒、⑦漏斗、⑧蒸发皿
| A.②③④⑦ | B.①②④⑥⑦ | C.②④⑥⑦ | D.①②③④⑥⑦ |
您最近一年使用:0次
2023-09-23更新
|
199次组卷
|
6卷引用:安徽省灵璧中学2024届高三上学期一轮复习联考(一)化学试题
名校
解题方法
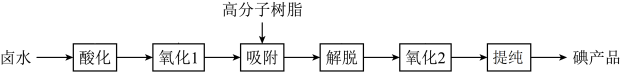
4 . 工业上以卤水(富含 )为原料用高分子树脂提取碘的工艺流程如图。下列说法不正确的是
)为原料用高分子树脂提取碘的工艺流程如图。下列说法不正确的是
 )为原料用高分子树脂提取碘的工艺流程如图。下列说法不正确的是
)为原料用高分子树脂提取碘的工艺流程如图。下列说法不正确的是
| A.“氧化1”过程既可以用氯气,也可以用过氧化氢溶液 |
B.“解脱”可以用亚硫酸钠将碘单质还原为 ,离子方程式为 ,离子方程式为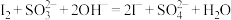 |
| C.用高分子树脂“吸附”,再“解脱”是为了便于分离富集碘元素 |
| D.“提纯”过程包括萃取分液、蒸馏得到粗产品,再利用升华法纯化 |
您最近一年使用:0次
2022-09-03更新
|
183次组卷
|
2卷引用:安徽省江淮十校2022-2023学年高三上学期第一次联考化学试题
解题方法
5 . 下列实验操作或实验仪器使用正确的是


| A.图1装置可用于比较MnO2、Cl2、S的氧化性 |
| B.图2既可以防止倒吸,又可以检查实验时后续装置是否发生堵塞 |
| C.图3 可组装启普发生器 |
| D.图4用来灼烧海带 |
您最近一年使用:0次
名校
6 . 某学习小组拟在实验室从海带中提取碘单质,设计流程如图所示。下列说法正确的是
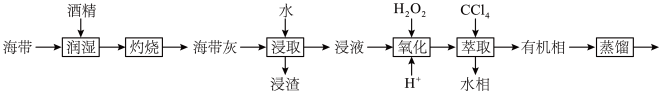

| A.“灼烧”海带应在蒸发皿中进行,并且用玻璃棒搅拌 |
B.海带灰中除了含有较多的 外,还有其他无机质 外,还有其他无机质 |
C.“氧化”时用足量 代替 代替 ,可获得较多的 ,可获得较多的 |
| D.蒸馏和萃取均需用到的玻璃仪器是分液漏斗 |
您最近一年使用:0次
2022-11-28更新
|
295次组卷
|
5卷引用:安徽省铜陵市等5地2022届高三下学期二模统考化学试题
名校
解题方法
7 . 海带中含有丰富的碘,某校化学兴趣小组的同学们设计联合氯碱工业,以海带灰为原料提碘的工艺流程如图:
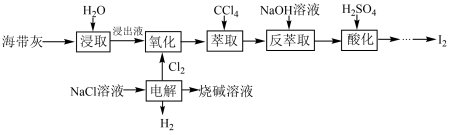
回答下列问题:
(1)“浸取”操作需要进行2~3次,将所得浸取液合并后进入下一流程,其目的是_____ ;请你设计实验证明“浸取”已经进行完全:_____ (需要用到的实验药品有:淀粉溶液、硫酸酸化的H2O2溶液,写出具体实验操作和现象)。
(2)“电解”反应的化学方程式为_____ 。
(3)“萃取”时,CCl4层的颜色为______ 色;“反萃取”时生成NaI和NaIO3,写出该反应的离子方程式:______ 。
(4)“酸化”后生成含I2的悬浊液,需要经过_____ (填操作名称)操作得到I2。
(5)该工艺流程实际操作中,碘的损失率为23.8%。若以2.5t海带灰为原料,最终制得I2物质的量为3×103mol,则该原料中含碘量为______ %
(6)该工艺流程中,除了H2O和NaCl以外,可以循环利用的物质有_____ (填化学式)。

回答下列问题:
(1)“浸取”操作需要进行2~3次,将所得浸取液合并后进入下一流程,其目的是
(2)“电解”反应的化学方程式为
(3)“萃取”时,CCl4层的颜色为
(4)“酸化”后生成含I2的悬浊液,需要经过
(5)该工艺流程实际操作中,碘的损失率为23.8%。若以2.5t海带灰为原料,最终制得I2物质的量为3×103mol,则该原料中含碘量为
(6)该工艺流程中,除了H2O和NaCl以外,可以循环利用的物质有
您最近一年使用:0次
8 . 碘元素被称为“智力元素”,海洋植物如海带、海藻中存在丰富的碘元素,一般以碘离子形式存在。某小组设计实验从20.00g海藻中提取碘单质,实验流程如下:
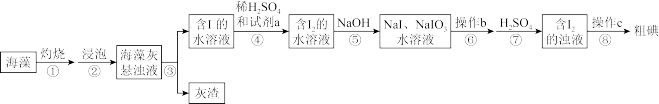
试回答下列问题:
(1)灼烧海藻时,将海藻用___________ (填化学式)润湿后,置于___________ (填装置名称)中烧成灰烬。
(2)从下列试剂中选择可做试剂a的是___________ (填序号)。
A.H2O2 B.MnO2 C.FeCl2 D.SO2
有人提出试剂a可以是Cl2,但是使用时必须控制用量,否则生成的I2,又被Cl2氧化为+5价,该反应的化学方程式为___________
(3)操作b是___________ ,滴加稀硫酸时发生的离子反应方程式为___________ 操作c为过滤,滤液可返回至___________ (填步骤序号)操作后溶液中循环利用。
(4)碘量法常用于测量草药中可能残余的有毒元素As的含量:
①取1000g草药样品进行前期处理制得待测溶液1000mL,此时样品中含有的砷元素转化为H3AsO3;
②转移100mL待测液至250mL锥形瓶中,加入1.000×10-3mol·L-1标准I2溶液20.00mL(H3AsO3转化为H3AsO4),并加入少量的淀粉溶液;
③用1.000×103mol·L-1的硫代硫酸钠标准溶液滴定过量的碘(已知:2 +I2=2I-+
+I2=2I-+ )。滴定终点时消耗22.00mL硫代硫酸钠标准溶液,则草药中砷的含量为
)。滴定终点时消耗22.00mL硫代硫酸钠标准溶液,则草药中砷的含量为___________ mg/kg;若滴定时溶液酸性过强,会导致测量结果___________ (填“偏高”或“偏低”)。

试回答下列问题:
(1)灼烧海藻时,将海藻用
(2)从下列试剂中选择可做试剂a的是
A.H2O2 B.MnO2 C.FeCl2 D.SO2
有人提出试剂a可以是Cl2,但是使用时必须控制用量,否则生成的I2,又被Cl2氧化为+5价,该反应的化学方程式为
(3)操作b是
(4)碘量法常用于测量草药中可能残余的有毒元素As的含量:
①取1000g草药样品进行前期处理制得待测溶液1000mL,此时样品中含有的砷元素转化为H3AsO3;
②转移100mL待测液至250mL锥形瓶中,加入1.000×10-3mol·L-1标准I2溶液20.00mL(H3AsO3转化为H3AsO4),并加入少量的淀粉溶液;
③用1.000×103mol·L-1的硫代硫酸钠标准溶液滴定过量的碘(已知:2
 +I2=2I-+
+I2=2I-+ )。滴定终点时消耗22.00mL硫代硫酸钠标准溶液,则草药中砷的含量为
)。滴定终点时消耗22.00mL硫代硫酸钠标准溶液,则草药中砷的含量为
您最近一年使用:0次
解题方法
9 .  常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备
常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备 的一种流程如下:
的一种流程如下:
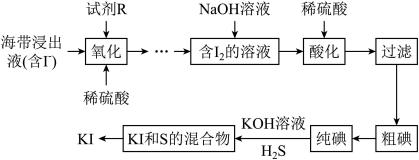
回答下列问题:
(1)“酸化”时稀硫酸的作用是___________ 。
(2)分离 和S的混合物得到
和S的混合物得到 溶液的试剂和方法如下,正确的是
溶液的试剂和方法如下,正确的是___________ (填标号)。
(3)利用下图装置完成 与
与 反应制备
反应制备 。
。

① 溶液的作用是
溶液的作用是___________ (用离子方程式表示)。
②三颈烧瓶中产生 的正确操作顺序为
的正确操作顺序为___________ (填标号)。
a.旋开活塞K,通入 b.加入稀硫酸 c.加入
b.加入稀硫酸 c.加入 溶液
溶液
(4)产品纯度测定。
准确称取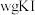 样品溶于水配成
样品溶于水配成 溶液,量取
溶液,量取 溶液于锥形瓶中,加入足量用稀硫酸酸化的
溶液于锥形瓶中,加入足量用稀硫酸酸化的 溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用
溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用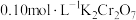 标准溶液反应至完全(还原产物只有
标准溶液反应至完全(还原产物只有 ),消耗标准溶液
),消耗标准溶液 。该
。该 产品的纯度为
产品的纯度为___________ (用含w,V的式子表示)。
 常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备
常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备 的一种流程如下:
的一种流程如下:
回答下列问题:
(1)“酸化”时稀硫酸的作用是
(2)分离
 和S的混合物得到
和S的混合物得到 溶液的试剂和方法如下,正确的是
溶液的试剂和方法如下,正确的是| 选项 | 试剂 | 方法 |
| a | 二硫化碳 | 分液 |
| b | 酒精 | 分液 |
| c |  溶液 溶液 | 过滤 |
(3)利用下图装置完成
 与
与 反应制备
反应制备 。
。
①
 溶液的作用是
溶液的作用是②三颈烧瓶中产生
 的正确操作顺序为
的正确操作顺序为a.旋开活塞K,通入
 b.加入稀硫酸 c.加入
b.加入稀硫酸 c.加入 溶液
溶液(4)产品纯度测定。
准确称取
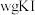 样品溶于水配成
样品溶于水配成 溶液,量取
溶液,量取 溶液于锥形瓶中,加入足量用稀硫酸酸化的
溶液于锥形瓶中,加入足量用稀硫酸酸化的 溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用
溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用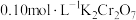 标准溶液反应至完全(还原产物只有
标准溶液反应至完全(还原产物只有 ),消耗标准溶液
),消耗标准溶液 。该
。该 产品的纯度为
产品的纯度为
您最近一年使用:0次



