名校
解题方法
1 . 某同学检验海带中是否含有碘元素,进行了如下实验。
步骤Ⅰ:灼烧干海带得到海带灰;
步骤Ⅱ:将海带灰加蒸馏水溶解、过滤,得到海带灰浸取液;
步骤Ⅲ:取少量浸取液于试管中,加入淀粉溶液,溶液未变蓝;再加入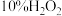 溶液(硫酸酸化),溶液变为蓝色;
溶液(硫酸酸化),溶液变为蓝色;
步骤Ⅳ:将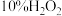 溶液(硫酸酸化)替换为氯水,重复步骤Ⅲ,溶液未变蓝;
溶液(硫酸酸化)替换为氯水,重复步骤Ⅲ,溶液未变蓝;
步骤Ⅴ:向步骤Ⅳ所得溶液中通入 ,溶液迅速变为蓝色。
,溶液迅速变为蓝色。
下列说法不正确的是
步骤Ⅰ:灼烧干海带得到海带灰;
步骤Ⅱ:将海带灰加蒸馏水溶解、过滤,得到海带灰浸取液;
步骤Ⅲ:取少量浸取液于试管中,加入淀粉溶液,溶液未变蓝;再加入
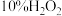 溶液(硫酸酸化),溶液变为蓝色;
溶液(硫酸酸化),溶液变为蓝色;步骤Ⅳ:将
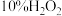 溶液(硫酸酸化)替换为氯水,重复步骤Ⅲ,溶液未变蓝;
溶液(硫酸酸化)替换为氯水,重复步骤Ⅲ,溶液未变蓝;步骤Ⅴ:向步骤Ⅳ所得溶液中通入
 ,溶液迅速变为蓝色。
,溶液迅速变为蓝色。下列说法不正确的是
| A.步骤Ⅰ中,灼烧干海带的目的是除去有机化合物,获得可溶性碘化物 |
B.步骤Ⅲ中,反应的离子方程式: |
C.若将步骤Ⅴ中的 替换为 替换为 溶液,也可能观察到溶液变为蓝色 溶液,也可能观察到溶液变为蓝色 |
D.对比步骤Ⅲ、Ⅳ和Ⅴ中实验现象,说明该条件下 氧化性比氯水强 氧化性比氯水强 |
您最近一年使用:0次
2023-04-29更新
|
553次组卷
|
4卷引用:北京市丰台区2023届高三下学期二模考试化学试题
2 . 海带中含有碘元素,从海带中提取碘的实验过程如下图所示。

(1)步骤①会用到下列仪器中的_______(填字母)。
(2)海带灰悬浊液含有 。步骤④的试剂选用
。步骤④的试剂选用 、稀硫酸,离子方程式是
、稀硫酸,离子方程式是_______ 。
(3)检验步骤④产生了 的方法是
的方法是_______ 。
(4)步骤⑤“提取”包含以下四个过程。
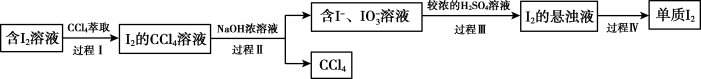
a.过程Ⅰ使用的 体积明显小于含
体积明显小于含 溶液,即可使
溶液,即可使 几乎完全地转移至
几乎完全地转移至 中,推测
中,推测 在
在_______ (填“ ”或“
”或“ ”)中的溶解度更大。
”)中的溶解度更大。
b. 与
与 浓溶液反应的离子方程式是
浓溶液反应的离子方程式是_______ 。
c.过程Ⅰ→过程Ⅲ的目的是_______ 。
d.过程Ⅳ的操作是_______ 。

(1)步骤①会用到下列仪器中的_______(填字母)。
| A.酒精灯 | B.漏斗 | C.坩埚 | D.泥三角 |
 。步骤④的试剂选用
。步骤④的试剂选用 、稀硫酸,离子方程式是
、稀硫酸,离子方程式是(3)检验步骤④产生了
 的方法是
的方法是(4)步骤⑤“提取”包含以下四个过程。

a.过程Ⅰ使用的
 体积明显小于含
体积明显小于含 溶液,即可使
溶液,即可使 几乎完全地转移至
几乎完全地转移至 中,推测
中,推测 在
在 ”或“
”或“ ”)中的溶解度更大。
”)中的溶解度更大。b.
 与
与 浓溶液反应的离子方程式是
浓溶液反应的离子方程式是c.过程Ⅰ→过程Ⅲ的目的是
d.过程Ⅳ的操作是
您最近一年使用:0次
名校
3 . 下列叙述不正确的是
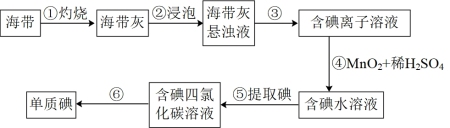

| A.步骤③的分离操作为过滤 |
| B.步骤④中理论上每产生1molI2,需要1molMnO2被氧化 |
| C.步骤⑥操作可以为先加入浓碱过滤,向水层再加入45%硫酸溶液分液,将碘提取出来 |
| D.步骤⑤中加入萃取剂后现象是溶液分层,下层为四氯化碳层呈紫色 |
您最近一年使用:0次
2022-05-15更新
|
195次组卷
|
3卷引用:北京市昌平区第一中学2021-2022学年高一下学期线上期中学情调研化学试题
北京市昌平区第一中学2021-2022学年高一下学期线上期中学情调研化学试题北京市昌平区第一中学2022-2023学年高一上学期期中考试化学试题(已下线)第13练 自然资源的开发利用-2022年【暑假分层作业】高一化学(人教版2019必修第二册)
名校
4 . 碘是人体必须的微量元素之一,海洋植物如海带、海藻中含有丰富的碘元素。在实验室中,从海藻里提取碘的流程如下:
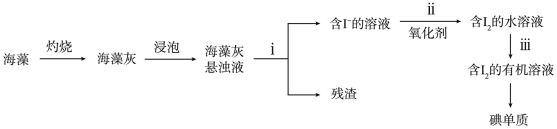
(1)指出上述过程中有关实验操作的名称,步骤i:___________ ,步骤iii:___________ 。
(2)步骤ii中可使用 ,从原子结构角度说明理由:
,从原子结构角度说明理由:___________ 。 过量时,可能无法获得
过量时,可能无法获得 ,原因是
,原因是 会被继续氧化为
会被继续氧化为 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(3)当使用 做氧化剂时,
做氧化剂时, 的转化率受外界因素的影响如下图所示。
的转化率受外界因素的影响如下图所示。
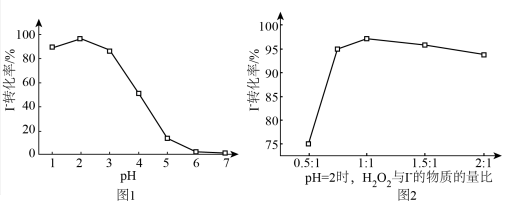
①图1中, 时
时 转化率几乎为0,结合离子方程式解释原因:
转化率几乎为0,结合离子方程式解释原因:___________ 。
②图2中, 与
与 物质的量之比从0.5﹕1提高至1﹕1时,
物质的量之比从0.5﹕1提高至1﹕1时, 的转化率明显增大,可能的原因是
的转化率明显增大,可能的原因是___________ (写出2条)。

(1)指出上述过程中有关实验操作的名称,步骤i:
(2)步骤ii中可使用
 ,从原子结构角度说明理由:
,从原子结构角度说明理由: 过量时,可能无法获得
过量时,可能无法获得 ,原因是
,原因是 会被继续氧化为
会被继续氧化为 ,该反应的离子方程式为
,该反应的离子方程式为(3)当使用
 做氧化剂时,
做氧化剂时, 的转化率受外界因素的影响如下图所示。
的转化率受外界因素的影响如下图所示。
①图1中,
 时
时 转化率几乎为0,结合离子方程式解释原因:
转化率几乎为0,结合离子方程式解释原因:②图2中,
 与
与 物质的量之比从0.5﹕1提高至1﹕1时,
物质的量之比从0.5﹕1提高至1﹕1时, 的转化率明显增大,可能的原因是
的转化率明显增大,可能的原因是
您最近一年使用:0次
2021-11-04更新
|
202次组卷
|
4卷引用:北京市海淀区2021-2022学年高三上学期期中考试化学试题
名校
5 . 海洋植物如海带,海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下:(已知: )。
)。
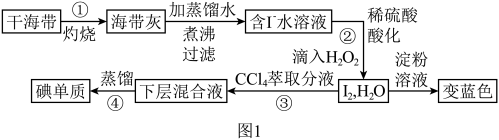
(1)以上步骤不需要用到的仪器是_______。
(2)选用试剂 的理由是_______。
的理由是_______。
(3)写出步骤②中反应的离子方程式_______ 。
(4)工业制备过程中,步骤④很难达到目的,常对图1步骤④进行如下改进:
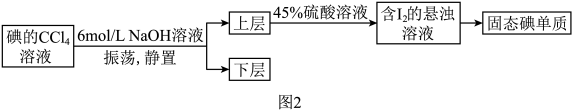
写出上述流程中加入45%硫酸溶液一步反应的离子方程式_______ 。
(5)向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
①已知碘元素最终变为无色HIO3。上述整个过程中的还原剂有_______ 。
②若把KI成KBr,则CCl4层变为_______ 色,继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是_______ 。
 )。
)。
(1)以上步骤不需要用到的仪器是_______。
A. | B. | C. | D. |
 的理由是_______。
的理由是_______。A. 不溶于水 不溶于水 | B. 的密度比水大 的密度比水大 |
C.碘在 中比在水中溶解度更大 中比在水中溶解度更大 | D. 与碘水不反应 与碘水不反应 |
(4)工业制备过程中,步骤④很难达到目的,常对图1步骤④进行如下改进:

写出上述流程中加入45%硫酸溶液一步反应的离子方程式
(5)向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
①已知碘元素最终变为无色HIO3。上述整个过程中的还原剂有
②若把KI成KBr,则CCl4层变为
您最近一年使用:0次
6 . 从海带浸泡液(碘元素主要以 存在)中获取
存在)中获取 ,含碘物质的转化过程如下。
,含碘物质的转化过程如下。 的作用为
的作用为_______ (填“氧化剂”或“还原剂”)。
(2)为提高①的化学反应速率,可采取的措施是_______ (写出一条即可)。
(3)补全②的离子方程式:_______ 。
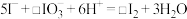
(4)②中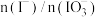 和pH对碘离子的氧化率的影响如下图所示。
和pH对碘离子的氧化率的影响如下图所示。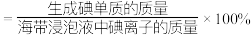
分析图中信息,选择最佳条件:_______ 。
 存在)中获取
存在)中获取 ,含碘物质的转化过程如下。
,含碘物质的转化过程如下。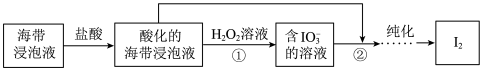
 的作用为
的作用为(2)为提高①的化学反应速率,可采取的措施是
(3)补全②的离子方程式:
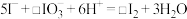
(4)②中
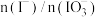 和pH对碘离子的氧化率的影响如下图所示。
和pH对碘离子的氧化率的影响如下图所示。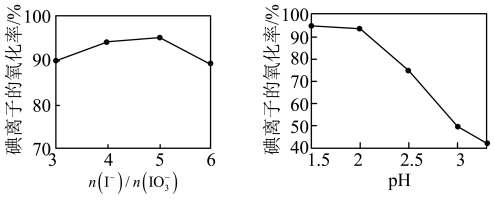
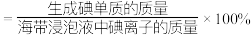
分析图中信息,选择最佳条件:
您最近一年使用:0次



