1 . 海洋资源的利用具有非常广阔的前景。回答下列问题:
Ⅰ.海水提溴
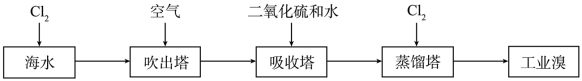
(1)溴元素在元素周期表中的位置为_______ 。
(2)吸收塔用二氧化硫和水吸收Br2的离子反应方程式:_______ 。
(3)蒸馏塔的蒸馏温度应控制在80-90°C最有利于生产,原因可能为:温度过高,_______ ;温度过低,_______ 。
Ⅱ.海水提镁
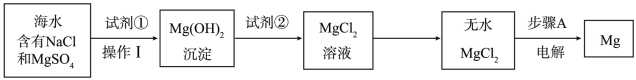
(4)工业上常用于沉淀Mg2+的廉价试剂①的俗名是_______ 。操作Ⅰ的名称是_______ 。
(5)步骤A的化学方程式为_______ 。
Ⅲ.海带提碘

(6)步骤B需搅拌、加热煮沸的目的是_______ 。步骤C中反应的离子方程式为_______ 。
Ⅰ.海水提溴

(1)溴元素在元素周期表中的位置为
(2)吸收塔用二氧化硫和水吸收Br2的离子反应方程式:
(3)蒸馏塔的蒸馏温度应控制在80-90°C最有利于生产,原因可能为:温度过高,
Ⅱ.海水提镁

(4)工业上常用于沉淀Mg2+的廉价试剂①的俗名是
(5)步骤A的化学方程式为
Ⅲ.海带提碘

(6)步骤B需搅拌、加热煮沸的目的是
您最近一年使用:0次
2022-07-10更新
|
304次组卷
|
2卷引用:四川省泸县第四中学2022-2023学年高一下学期6月期末考试化学试题
2 . 碘是人体的必需微量元素之一,海带提取碘的部分实验流程如下
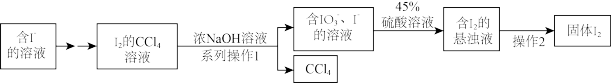
(1)系列操作1中需用到的玻璃仪器有烧杯、玻璃棒和___________ ,操作2的实验方法是___________ 。
(2)氧化 通常用
通常用 作为氧化剂,写出反应的离子方程式
作为氧化剂,写出反应的离子方程式___________ 。
(3)某实验小组研究 的氧化,将
的氧化,将 通入KI溶液中,出现黄色,查阅资料,发生了以下反应:
通入KI溶液中,出现黄色,查阅资料,发生了以下反应: 。为了探究该反应的影响因素,设计以下实验:
。为了探究该反应的影响因素,设计以下实验:
①用水吸收 制取
制取 水溶液,吸收装置最佳的是
水溶液,吸收装置最佳的是___________ 。

②实验1和2探究___________ 对实验的影响,实验2和3探究___________ 对实验的影响,实验2加蒸馏水的体积为___________ (用表中字母或字母的表达式作答)。
③添加药品的合理顺序为: 水溶液、
水溶液、___________ 、稀盐酸、___________ (填“KI溶液”或“蒸馏水”)。
④往三组实验中滴加淀粉溶液,均没有出现蓝色,你认为原因是___________ (用化学方程式解释)。检验该反应发生的实验试剂是___________ 。
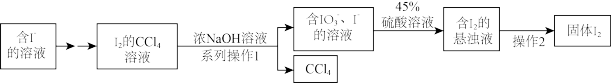
(1)系列操作1中需用到的玻璃仪器有烧杯、玻璃棒和
(2)氧化
 通常用
通常用 作为氧化剂,写出反应的离子方程式
作为氧化剂,写出反应的离子方程式(3)某实验小组研究
 的氧化,将
的氧化,将 通入KI溶液中,出现黄色,查阅资料,发生了以下反应:
通入KI溶液中,出现黄色,查阅资料,发生了以下反应: 。为了探究该反应的影响因素,设计以下实验:
。为了探究该反应的影响因素,设计以下实验:| 实验序号 |  水溶液(mL) 水溶液(mL) |  溶液(mL) 溶液(mL) | 稀盐酸(mL) | 蒸馏水(mL) | 实验现象 |
| 1 | a(过量) | b | 0 | d | 溶液逐渐变浅黄色 |
| 2 | a(过量) | b | c | ___________ | 溶液变黄,有浑浊 |
| 3 | a(过量) | 2b | c | 0 | 溶液变黄,比实验2出现浑浊更快 |
 制取
制取 水溶液,吸收装置最佳的是
水溶液,吸收装置最佳的是
②实验1和2探究
③添加药品的合理顺序为:
 水溶液、
水溶液、④往三组实验中滴加淀粉溶液,均没有出现蓝色,你认为原因是
您最近一年使用:0次
2021-08-04更新
|
586次组卷
|
3卷引用:四川省凉山州西昌天立学校2022届高三上学期入学考试理综化学试题
解题方法
3 . 海洋是巨大的资源宝库,孕育着丰富的矿产。海水资源的综合利用对人类的生产生活有重要意义。回答下列问题:
Ⅰ.从海带中提取碘的工艺流程如图所示:

(1)灼烧干海带需在仪器________ (填“蒸发皿”“坩埚”或“烧杯”)内进行。
(2)用蒸馏水浸取海带灰时,为提高浸取率,可采用的方法有_________ (填一种即可);
(3)将溶液中的I-氧化成I2,最佳选用试剂为_________(填标号)。
(4)欲证明水溶液中含有I2,实验方法为________________ 。
Ⅱ.空气吹出法是目前“海水提溴”的主要方法之一,其主要工艺流程如图所示:

(5)步骤①的离子方程式为___________ 。
(6)步骤②说明溴单质具有_________ 性,步骤③④的目的是______________ 。
(7)步骤③的还原剂若为 溶液,则其离子方程式为
溶液,则其离子方程式为____________ 。
Ⅰ.从海带中提取碘的工艺流程如图所示:

(1)灼烧干海带需在仪器
(2)用蒸馏水浸取海带灰时,为提高浸取率,可采用的方法有
(3)将溶液中的I-氧化成I2,最佳选用试剂为_________(填标号)。
| A.稀硝酸 | B.酸性 | C.浓硫酸 | D.稀硫酸、 |
Ⅱ.空气吹出法是目前“海水提溴”的主要方法之一,其主要工艺流程如图所示:

(5)步骤①的离子方程式为
(6)步骤②说明溴单质具有
(7)步骤③的还原剂若为
 溶液,则其离子方程式为
溶液,则其离子方程式为
您最近一年使用:0次
4 . 从海带中提取碘的一种实验流程如图所示,下列说法错误的是
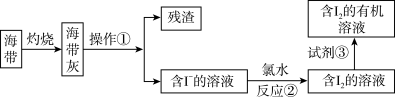

| A.灼烧海带可在坩埚中进行 |
| B.操作①为加水浸泡、过滤、洗涤残渣 |
C.反应②中发生的主要反应为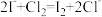 |
| D.试剂③可以选用无水乙醇 |
您最近一年使用:0次
2022-05-17更新
|
183次组卷
|
2卷引用:四川省凉山州2022-2023学年高二下学期期末考试化学试题
5 . 我国拥有很长的海岸线,海洋资源的开发利用具有广阔前景。
(1)工业上海水淡化的方法有___________ 、___________ 。(填两种)
(2)空气吹出法是用于工业规模海水提溴的常用方法。其工艺流程如下:
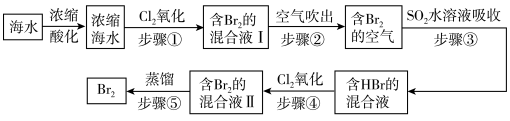
①步骤①中获得 的离子方程式为
的离子方程式为___________ 。
②根据上述反应可判断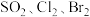 三种物质氧化性由强到弱的顺序是
三种物质氧化性由强到弱的顺序是___________ 。
③步骤③中若吸收剂为饱和 溶液(足量),则完全吸收
溶液(足量),则完全吸收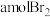 共有
共有___________ 个电子转移(用a和 的代数式表示)。
的代数式表示)。
(3)某化学兴趣小组按如下实验流程提取海带中的碘,请回答相关问题。
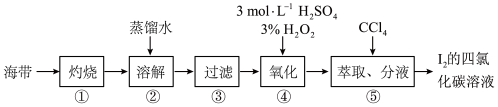
i.第①步是将海带放入_______ (填仪器名称)中,用酒精灯充分加热灰化。
ii.实验第④步骤后应检验碘单质的存在,具体方法是________ 。
iii.海带灰中还含有其他无机盐类(硫酸盐、硝酸盐、碳酸盐等),这些盐类是在流程图中的第_____ 步(填编号)与碘分离的。
iv.写出④中在酸性溶液下反应的离子方程式_______ 。
(1)工业上海水淡化的方法有
(2)空气吹出法是用于工业规模海水提溴的常用方法。其工艺流程如下:

①步骤①中获得
 的离子方程式为
的离子方程式为②根据上述反应可判断
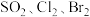 三种物质氧化性由强到弱的顺序是
三种物质氧化性由强到弱的顺序是③步骤③中若吸收剂为饱和
 溶液(足量),则完全吸收
溶液(足量),则完全吸收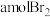 共有
共有 的代数式表示)。
的代数式表示)。(3)某化学兴趣小组按如下实验流程提取海带中的碘,请回答相关问题。

i.第①步是将海带放入
ii.实验第④步骤后应检验碘单质的存在,具体方法是
iii.海带灰中还含有其他无机盐类(硫酸盐、硝酸盐、碳酸盐等),这些盐类是在流程图中的第
iv.写出④中在酸性溶液下反应的离子方程式
您最近一年使用:0次
名校
解题方法
6 . 海洋是巨大的资源宝库,可以制取多种物质。
I.海水提溴
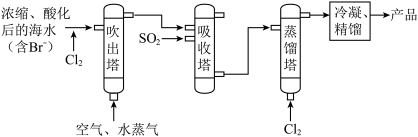
(1)吹出塔中采用气-液逆流的方式(液体从塔顶喷淋,气体从塔底进入),其目的是_______ 。
(2)请写出吸收塔中反应的离子方程式___________ 。
II.海带提碘(海带中碘元素以I-形式存在)
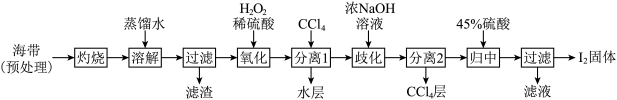
(3)“氧化”过程涉及到的离子方程式是_________ ,请设计一种检验所得溶液含I2的方法:___________ 。
(4)加入浓NaOH溶液充分振荡,发生的歧化反应中氧化剂和还原剂物质的量之比为________ ;向分离得到的含I-和 的水溶液中加入45%硫酸,发生归中反应的离子方程式为
的水溶液中加入45%硫酸,发生归中反应的离子方程式为________ 。
(5)图1是制取碘单质的原电池装置,图2是利用碘研制的新型的锌-碘溴液流电池(图中贮液器可储存电解质溶液,增加电池容量)。
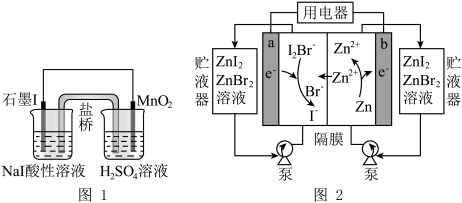
图1中,MnO2极发生的电极反应式为_______ ;图2中,放电时,a电极反应式为________ ,b电极质量减少6.5g时,a电极室增加________ mol离子(不考虑电极室与贮液器的溶液交换)。
I.海水提溴

(1)吹出塔中采用气-液逆流的方式(液体从塔顶喷淋,气体从塔底进入),其目的是
(2)请写出吸收塔中反应的离子方程式
II.海带提碘(海带中碘元素以I-形式存在)

(3)“氧化”过程涉及到的离子方程式是
(4)加入浓NaOH溶液充分振荡,发生的歧化反应中氧化剂和还原剂物质的量之比为
 的水溶液中加入45%硫酸,发生归中反应的离子方程式为
的水溶液中加入45%硫酸,发生归中反应的离子方程式为(5)图1是制取碘单质的原电池装置,图2是利用碘研制的新型的锌-碘溴液流电池(图中贮液器可储存电解质溶液,增加电池容量)。

图1中,MnO2极发生的电极反应式为
您最近一年使用:0次
7 . 根据流程回答问题
Ⅰ.从海带(含KI)中提取碘,某研究性学习小组设计了如图流程:
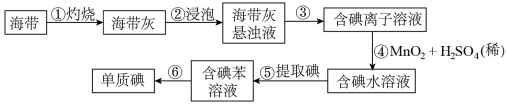
(1)步骤①中灼烧海带是在_______ (填仪器名称)中进行
(2)步骤③、⑤、⑥的实验操作分别为_______
(3)反应④的离子方程式为_______
(4)步骤⑤向碘水中加入苯,振荡静置后的现象为_______
Ⅱ.工业上用铝土矿(含有 杂质的
杂质的 ,
, 的含量a %)为原料冶炼铝的工艺流程如(所加试剂均过量):
的含量a %)为原料冶炼铝的工艺流程如(所加试剂均过量):
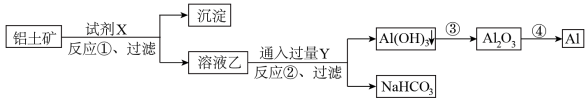
(5)试剂X是_______ (填化学式),上述反应过程中耗能最多的是_______ (填序号)
(6)反应②的离子方程式_______
(7)工业上生产1t Al,在生产过程中Al的损失率为b %,理论上需投入铝土矿_______ t(列出计算表达式即可)
Ⅰ.从海带(含KI)中提取碘,某研究性学习小组设计了如图流程:

(1)步骤①中灼烧海带是在
(2)步骤③、⑤、⑥的实验操作分别为
(3)反应④的离子方程式为
(4)步骤⑤向碘水中加入苯,振荡静置后的现象为
Ⅱ.工业上用铝土矿(含有
 杂质的
杂质的 ,
, 的含量a %)为原料冶炼铝的工艺流程如(所加试剂均过量):
的含量a %)为原料冶炼铝的工艺流程如(所加试剂均过量):
(5)试剂X是
(6)反应②的离子方程式
(7)工业上生产1t Al,在生产过程中Al的损失率为b %,理论上需投入铝土矿
您最近一年使用:0次
解题方法
8 . 海洋中蕴藏着巨大的化学资源,下列有关海水综合利用的说法正确的是
| A.海水提镁时,向海水中加入氢氧化钙,然后过滤得到氢氧化镁,再灼烧得MgO,电解熔融的MgO就可以得单质Mg |
| B.利用海水制盐,制得的NaCl溶于水,然后电解可以生产金属钠、氯气等化工产品 |
| C.海水提溴时,向海水中通入氯气,然后加入CCl4萃取、分液蒸馏就可以得到 |
| D.海带提碘时,需先将海带在坩埚中灼烧,然后用水溶解,过滤,然后再进行其它操作 |
您最近一年使用:0次
2022-07-13更新
|
250次组卷
|
3卷引用:四川省遂宁市2021-2022学年高一下学期期末考试化学试题
解题方法
9 . 碘是人体必需的微量元素,幼儿缺碘可导致发育迟缓、呆傻等多种疾病。海带中含有较多的碘元素,以下是从海带中提取碘并测定碘含量的实验方案。
提示:海带灰中碘元素以 形式存在。
形式存在。
实验一:海带中碘元素的检验
步骤Ⅰ:准确称取20.0g干海带,去除表面附着物、洗净、剪碎,用酒精浸润,灼烧完全至灰烬,停止加热、冷却。
步骤Ⅱ:将海带灰全部转移到小烧杯中,加入 蒸馏水搅拌,煮沸2~3分钟,过滤,洗涤,将滤液转移至
蒸馏水搅拌,煮沸2~3分钟,过滤,洗涤,将滤液转移至 容量瓶中定容。
容量瓶中定容。
步骤Ⅲ:取步骤IⅡ容量瓶中的溶液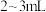 于试管中,加入几滴
于试管中,加入几滴
 溶液酸化,再加入
溶液酸化,再加入 3%的
3%的 溶液和几滴淀粉溶液,观察现象。
溶液和几滴淀粉溶液,观察现象。
实验二:海带中碘元素含量的测定
步骤Ⅳ:取步骤Ⅱ容量瓶中溶液 于锥形瓶中,逐滴加入饱和溴水到呈浅黄色,放置一段时间使其充分反应后加热煮沸至黄色褪去,冷却后加入
于锥形瓶中,逐滴加入饱和溴水到呈浅黄色,放置一段时间使其充分反应后加热煮沸至黄色褪去,冷却后加入 10%
10% 溶液,摇匀,立即用
溶液,摇匀,立即用 的
的 标准溶液滴定反应至浅黄色,加入几滴淀粉溶液作指示剂,继续滴定到溶液刚好褪色,达到反应终点。重复以上操作2~3次,测得平均消耗
标准溶液滴定反应至浅黄色,加入几滴淀粉溶液作指示剂,继续滴定到溶液刚好褪色,达到反应终点。重复以上操作2~3次,测得平均消耗 标准溶液
标准溶液 。
。
涉及的有关反应有:①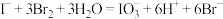
②
③
请按要求完成下列问题:
(1)步骤Ⅰ中用酒精浸润海带的作用是_______ ,灼烧海带的实验中需要的实验仪器有酒精灯、铁架台、泥三角、玻璃棒和_______ (填仪器名称)。
(2)说明海带中有碘元素的实验现象是_______ ,写出步骤中发生的离子反应方程式_______ 。
(3)根据以上数据计算每千克海带中含碘量约为_______  。
。
提示:海带灰中碘元素以
 形式存在。
形式存在。实验一:海带中碘元素的检验
步骤Ⅰ:准确称取20.0g干海带,去除表面附着物、洗净、剪碎,用酒精浸润,灼烧完全至灰烬,停止加热、冷却。
步骤Ⅱ:将海带灰全部转移到小烧杯中,加入
 蒸馏水搅拌,煮沸2~3分钟,过滤,洗涤,将滤液转移至
蒸馏水搅拌,煮沸2~3分钟,过滤,洗涤,将滤液转移至 容量瓶中定容。
容量瓶中定容。步骤Ⅲ:取步骤IⅡ容量瓶中的溶液
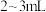 于试管中,加入几滴
于试管中,加入几滴
 溶液酸化,再加入
溶液酸化,再加入 3%的
3%的 溶液和几滴淀粉溶液,观察现象。
溶液和几滴淀粉溶液,观察现象。实验二:海带中碘元素含量的测定
步骤Ⅳ:取步骤Ⅱ容量瓶中溶液
 于锥形瓶中,逐滴加入饱和溴水到呈浅黄色,放置一段时间使其充分反应后加热煮沸至黄色褪去,冷却后加入
于锥形瓶中,逐滴加入饱和溴水到呈浅黄色,放置一段时间使其充分反应后加热煮沸至黄色褪去,冷却后加入 10%
10% 溶液,摇匀,立即用
溶液,摇匀,立即用 的
的 标准溶液滴定反应至浅黄色,加入几滴淀粉溶液作指示剂,继续滴定到溶液刚好褪色,达到反应终点。重复以上操作2~3次,测得平均消耗
标准溶液滴定反应至浅黄色,加入几滴淀粉溶液作指示剂,继续滴定到溶液刚好褪色,达到反应终点。重复以上操作2~3次,测得平均消耗 标准溶液
标准溶液 。
。涉及的有关反应有:①
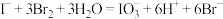
②

③

请按要求完成下列问题:
(1)步骤Ⅰ中用酒精浸润海带的作用是
(2)说明海带中有碘元素的实验现象是
(3)根据以上数据计算每千克海带中含碘量约为
 。
。
您最近一年使用:0次
10 . 紫菜和海带都是富含生物碘的海洋植物,以下为某兴趣小组模拟从紫菜提取碘单质的过程:
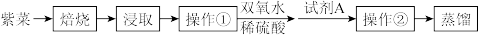
(1)为了充分浸取紫菜灰中的碘元素,可采用的方法是___________ 。(写两点)
(2)加入双氧水和稀硫酸后发生反应的离子方程式是___________ 。
(3)操作①的名称是___________ ,操作②应在___________ (填仪器名称)中振荡、静置;试剂A可选用下列物质中的___________ (填正确答案标号)。
A.乙醇 B. C.NaOH D.环己烯
C.NaOH D.环己烯
(4)该方案采用常压蒸馏并不合理,理由是___________ 。
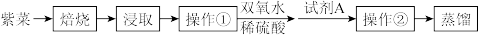
(1)为了充分浸取紫菜灰中的碘元素,可采用的方法是
(2)加入双氧水和稀硫酸后发生反应的离子方程式是
(3)操作①的名称是
A.乙醇 B.
 C.NaOH D.环己烯
C.NaOH D.环己烯(4)该方案采用常压蒸馏并不合理,理由是
您最近一年使用:0次



