1 . 海洋是巨大的资源宝库,从海洋中获取的部分资源如图所示:
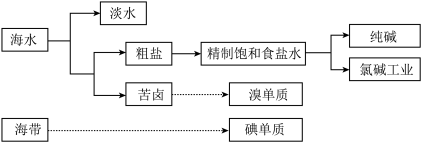
回答下列问题:
Ⅰ.微生物脱盐电池既可以实现海水的淡化,同时又能除去废水中的 和
和 ,原理如图所示,中阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过。
,原理如图所示,中阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过。
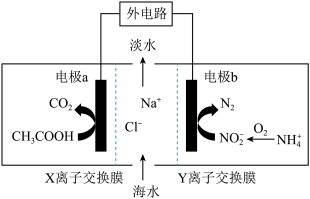
(1)电极b为电池的___________ 极(填正或负)。
(2)X离子交换膜为___________ 离子交换膜(填阴或阳)。
Ⅱ.溴被称为“海洋元素”,空气吹出法从海水中提取溴单质的流程如下图所示:
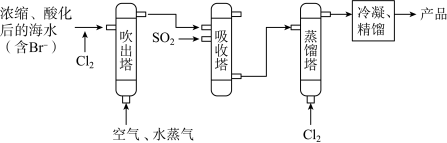
(3)吹出塔中采用气——液逆流的方式(液体从塔顶喷淋,气体从塔底进入),其目的是___________ 。
(4)写出蒸馏塔中反应的离子方程式___________ 。
Ⅲ.从海带中提取碘单质的流程如下:
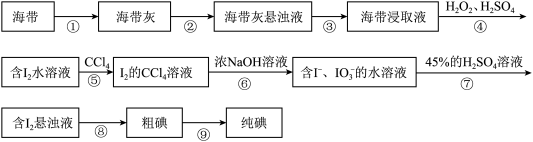
(5)上述流程中能循环使用的物质是___________ (填化学式)。
(6)步骤⑤的具体实验操作为:
A.将分液漏斗放在铁架台的铁圈中,静置、分层;
B.将含 水溶液和适量四氯化碳加入分液漏斗中,盖好玻璃塞;
水溶液和适量四氯化碳加入分液漏斗中,盖好玻璃塞;
C.检验分液漏斗活塞和上口玻璃塞是否漏液;
D.倒转分液漏斗振荡,并不时旋开活塞放气,最后关闭活塞;
E.从分液漏斗上口倒出上层液体;
F.将分液漏斗上口的玻璃塞打开或使塞上的凹槽对准分液漏斗口上的小孔;
G.旋开活塞,用烧杯接收下层液体;
上述实验操作的正确顺序为___________ (填序号),“操作A”静置、分层后的现象为___________ 。
(7)根据下表中有机物的性质分析,能代替步骤⑤中 的试剂是
的试剂是___________ (填试剂名称)。
(8)从海洋中获取资源涉及多种实验操作,为完成下列各组实验,所选仪器准确、完整的是___________ (填选项)。

回答下列问题:
Ⅰ.微生物脱盐电池既可以实现海水的淡化,同时又能除去废水中的
 和
和 ,原理如图所示,中阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过。
,原理如图所示,中阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过。
(1)电极b为电池的
(2)X离子交换膜为
Ⅱ.溴被称为“海洋元素”,空气吹出法从海水中提取溴单质的流程如下图所示:

(3)吹出塔中采用气——液逆流的方式(液体从塔顶喷淋,气体从塔底进入),其目的是
(4)写出蒸馏塔中反应的离子方程式
Ⅲ.从海带中提取碘单质的流程如下:

(5)上述流程中能循环使用的物质是
(6)步骤⑤的具体实验操作为:
A.将分液漏斗放在铁架台的铁圈中,静置、分层;
B.将含
 水溶液和适量四氯化碳加入分液漏斗中,盖好玻璃塞;
水溶液和适量四氯化碳加入分液漏斗中,盖好玻璃塞;C.检验分液漏斗活塞和上口玻璃塞是否漏液;
D.倒转分液漏斗振荡,并不时旋开活塞放气,最后关闭活塞;
E.从分液漏斗上口倒出上层液体;
F.将分液漏斗上口的玻璃塞打开或使塞上的凹槽对准分液漏斗口上的小孔;
G.旋开活塞,用烧杯接收下层液体;
上述实验操作的正确顺序为
(7)根据下表中有机物的性质分析,能代替步骤⑤中
 的试剂是
的试剂是| 试剂 | 性质 |
| 丙酮 | 无色液体,可以与水任意比例互溶, 易溶于丙酮 易溶于丙酮 |
| 氯仿 | 无色液体,不溶于水,密度比水大, 易溶于氯仿 易溶于氯仿 |
| 己烯 | 无色液体,不溶于水,密度比水小, 能与己烯发生化学反应 能与己烯发生化学反应 |
| 选项 | 实验 | 仪器 |
| A | 模拟海水晒盐制取粗盐 | 铁架台(带铁圈)、酒精灯、蒸发皿 |
| B | 将海带灼烧成海带灰 | 三脚架、酒精灯、坩埚、坩埚钳、玻璃棒 |
| C | 从含 的悬浊液中获取粗碘 的悬浊液中获取粗碘 | 铁架台(带铁圈)、普通漏斗、烧杯、玻璃棒 |
| D | 提纯粗碘制取纯碘 | 铁架台(带铁圈)、酒精灯、石棉网、烧杯、圆底烧瓶(盛有冷水) |
您最近一年使用:0次
2023-04-26更新
|
801次组卷
|
3卷引用:上海市宜川中学2023-2024学年高三上学期期末考试化学试题
名校
解题方法
2 . 我国拥有很长的海岸线,海洋资源的开发利用具有广阔前景。全球海水中溴的储藏量丰富,约占地球溴总储藏量的99%,故溴有“海洋元素”之称,海水中溴含量为65mg/L。空气吹出法工艺是目前“海水提溴”的最主要方法之一、其工艺流程如图:
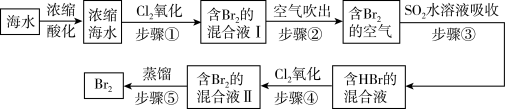
(1)步骤①中获得Br2的离子方程式为____ 。
(2)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是____ 。
(3)步骤③中若吸收剂为饱和Na2SO3溶液(足量),则完全吸收amolBr2共有___ 个电子转移(用a和NA的代数式表示)。
碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的流程图如图:

(4)设计“操作Ⅰ”的主要步骤:____ 、____ 。
(5)“试剂a”通常应具有一定的____ 性。
利用H2O2完成“溶液A”向“溶液B”的转变。配平该反应的化学方程式:____ 。
______KI+______H2O=______KOH+______I2
(6)由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是___ 。(选填编号)
(7)“操作II”宜选用的装置是____ 。(选填编号)
(8)在操作II后,检验提取碘后的水层是否仍含有碘单质的方法是:____ 。
(9)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,I2+2S2O =2I-+S4O
=2I-+S4O ,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
a.准确称取120g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液30.0mL,恰好反应完全。
则所测盐中碘的含量是____ mg•g-1(保留四位小数)。

(1)步骤①中获得Br2的离子方程式为
(2)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是
(3)步骤③中若吸收剂为饱和Na2SO3溶液(足量),则完全吸收amolBr2共有
碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的流程图如图:

(4)设计“操作Ⅰ”的主要步骤:
(5)“试剂a”通常应具有一定的
利用H2O2完成“溶液A”向“溶液B”的转变。配平该反应的化学方程式:
______KI+______H2O=______KOH+______I2
(6)由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是
| 试剂 | A.乙醇 | B.氯仿 | C.四氯化碳 | D.裂化汽油 |
| 相关性质 | 与水互溶不与反应 | 与水不互溶不与I2反应 | 与水不互溶不与I2反应 | 与水不互溶与I2反应 |
(7)“操作II”宜选用的装置是
A. | B.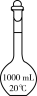 | C.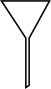 | D. |
(9)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,I2+2S2O
 =2I-+S4O
=2I-+S4O ,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:a.准确称取120g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液30.0mL,恰好反应完全。
则所测盐中碘的含量是
您最近一年使用:0次
3 . 为了从海带浸取液中提取碘,某同学设计了如图实验方案,解答下列问题:
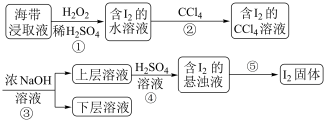
(1) 被称作绿色氧化剂的两个原因
被称作绿色氧化剂的两个原因_______ ;_______
(2)实验操作②的名称为_______ ,操作②需要的仪器除烧杯、玻璃棒外,尚缺少的玻璃仪器有_______ ,碘的 溶液位于
溶液位于_______ 层(填“上”或“下”),呈_______ 色。检验水层是否仍含碘单质的方法是_______ 。
(3)③是将富集在 中的碘单质利用化学转化重新富集在水中,称为反萃取,方程式为
中的碘单质利用化学转化重新富集在水中,称为反萃取,方程式为 ,接下来④发生的反应方程式为
,接下来④发生的反应方程式为_______ 。
(4)本实验中可以循环利用的物质是_______ 。

(1)
 被称作绿色氧化剂的两个原因
被称作绿色氧化剂的两个原因(2)实验操作②的名称为
 溶液位于
溶液位于(3)③是将富集在
 中的碘单质利用化学转化重新富集在水中,称为反萃取,方程式为
中的碘单质利用化学转化重新富集在水中,称为反萃取,方程式为 ,接下来④发生的反应方程式为
,接下来④发生的反应方程式为(4)本实验中可以循环利用的物质是
您最近一年使用:0次
4 . 溴元素和碘元素在工农业生产和日常生活中有着广泛应用。根据信息,完成下列填空。
Ⅰ.下图是从海水中提取粗溴的主要流程

(1)步骤①中,海水通过___________ (操作名称)、趁热过滤,得到苦卤;步骤②选用 作氧化剂,请写出发生反应的离子方程式
作氧化剂,请写出发生反应的离子方程式______ 。
(2)可用热空气吹出溴是因为溴的___________(选填编号)
(3)下列关于含溴化合物的用途说法错误的是___________(选填编号)
Ⅱ.实验小组从海带中提取碘
(4)将干海带经过浸泡、_____ (操作名称),得到滤液
(5)用如图所示的仪器提取碘水中的碘。该仪器名称为___________ ,该步操作的名称为___________ ;图示的提取剂可以是___________ (选填编号)。
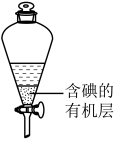
a.酒精b.苯c.四氯化碳d.醋酸
碘在该溶剂中显___________ 色
Ⅰ.下图是从海水中提取粗溴的主要流程

(1)步骤①中,海水通过
 作氧化剂,请写出发生反应的离子方程式
作氧化剂,请写出发生反应的离子方程式(2)可用热空气吹出溴是因为溴的___________(选填编号)
| A.熔点较低 | B.熔点较高 | C.沸点较低 | D.沸点较高 |
| A.食盐添加剂 | B.杀虫剂 | C.镇静剂 | D.感光材料 |
Ⅱ.实验小组从海带中提取碘
(4)将干海带经过浸泡、
(5)用如图所示的仪器提取碘水中的碘。该仪器名称为

a.酒精b.苯c.四氯化碳d.醋酸
碘在该溶剂中显
您最近一年使用:0次
2022-01-17更新
|
412次组卷
|
2卷引用:上海市金山区2021-2022学年高一上学期期末质量检测化学试题
5 . 关于化工生产,下列说法错误的是
| A.工业常用电解饱和食盐水的方法来制取氯气 |
| B.硫酸工业在常压下用SO2与O2反应制取SO3 |
| C.联合制碱法、氨碱法所需的CO2都来自石灰石的分解 |
| D.通常以海带、紫菜等为原料提取碘 |
您最近一年使用:0次
名校
解题方法
6 . I.某小组在实验室模拟工业提溴的流程(见下图),设计下图的装置进行实验。

回答下列问题:
(1)实验中先向A中通入Cl2,反应的离子方程式是_______ 。再向A中鼓入热空气,观察到的现象是_______ 。
(2)A中产生的气体被B中的 水溶液吸收,反应的化学方程式为
水溶液吸收,反应的化学方程式为_______ 。从氧化还原角度分析, 在该反应中体现了
在该反应中体现了_______ 性,下列试剂中能代替 水溶液的是
水溶液的是_______ (选填编号)。
a. 溶液 b. NaCl溶液 c.
溶液 b. NaCl溶液 c. 溶液
溶液
(3)为将B中的溴元素转化为液溴,向反应后B装置的溶液中通入氯气,充分反应,再加入苯,后续的实验操作步骤包含_______ (选填编号)。
a.过滤 b.萃取、分液 c.结晶 d. 蒸馏
(4)将1m3海水浓缩后最终得到21gBr2,若提取率为70%,则海水中溴元素的浓度为_______ g/L。
II.为了从海带中提取碘,该小组设计如下实验:
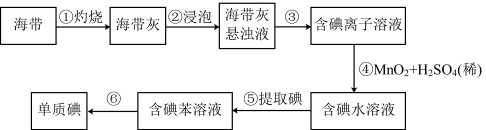
(5)步骤④的作用是_______ (选填编号)。
a. 浓缩 b. 氧化 c. 提取
(6)步骤⑤中选用苯提取碘的原因是_______ 。

回答下列问题:
(1)实验中先向A中通入Cl2,反应的离子方程式是
(2)A中产生的气体被B中的
 水溶液吸收,反应的化学方程式为
水溶液吸收,反应的化学方程式为 在该反应中体现了
在该反应中体现了 水溶液的是
水溶液的是a.
 溶液 b. NaCl溶液 c.
溶液 b. NaCl溶液 c. 溶液
溶液(3)为将B中的溴元素转化为液溴,向反应后B装置的溶液中通入氯气,充分反应,再加入苯,后续的实验操作步骤包含
a.过滤 b.萃取、分液 c.结晶 d. 蒸馏
(4)将1m3海水浓缩后最终得到21gBr2,若提取率为70%,则海水中溴元素的浓度为
II.为了从海带中提取碘,该小组设计如下实验:

(5)步骤④的作用是
a. 浓缩 b. 氧化 c. 提取
(6)步骤⑤中选用苯提取碘的原因是
您最近一年使用:0次
2023-01-13更新
|
332次组卷
|
2卷引用:上海市华东师范大学第三附属中学 2022-2023 学年高一上学期期末考试化学试题
名校
解题方法
7 . 海水的综合利用
海水的综合利用主要包括海水直接利用、海水淡化和海水中化学元素的利用三个方面。其中,海水中化学元素的利用是指从海水中提取钠、镁、氯、溴等元素,以及从海洋植物如海带中提取碘等。
(1)海水中含量最多的卤素是___________ 。
A.氟 B.氯 C.溴 D.碘
(2)海洋中蕴藏着巨大的化学资源。下列有关海水综合利用的说法正确的是___________ 。
A.蒸发海水可以得到单质碘
B.蒸馏海水可以得到淡水
C.利用活泼金属钾可置换海水中的镁
D.电解海水可以制得金属钠
(3)下列有关从海水中提取镁的说法错误的是___________ 。
A.贝壳在海水提取镁的生产流程中,主要经历了 的过程
的过程
B.工业生产中利用电解熔融 制备镁
制备镁
C.在从海水中提取镁的工业流程中, 可循环使用,用于制备盐酸,再溶解
可循环使用,用于制备盐酸,再溶解
D.利用 将海水中的
将海水中的 转化为
转化为 沉淀,然后电解
沉淀,然后电解 制备纯镁
制备纯镁
(4)下图是海水提溴的工艺流程,下列说法错误的是___________ 。
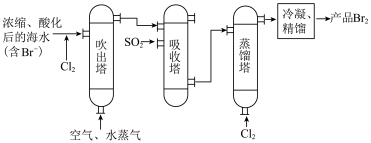
A.在海水中加“酸和氯气”,酸的作用是中和海水中的碱性物质
B .“吹出塔”中热空气的作用是将多余的氯气吹出
C.“吸收塔”中发生的反应为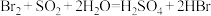
D.以上流程“吹出塔”和“吸收塔”内的反应是为了富集海水中的溴
(5)从海水中提取的粗盐精制后,通过电解饱和食盐水得到一系列化工产品。
①请写出电解饱和食盐水的化学方程式___________ 。
②检验阳极产物时可选用___________ ,向阴极附近溶液滴加紫色石蕊试液呈___________ 色。
③实验测得产生的 体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为
体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为___________  。
。
(6)实验室模拟工业从海藻中提碘的流程如图:
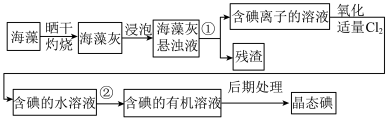
①选择合适实验操作名称填入流程图中:①___________ ,②___________ 。
A.溶解 B.过滤 C.萃取 D.分液
从“含碘的有机溶液”中回收溶剂,并得到碘单质,可选用如图装置完成。
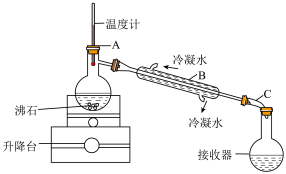
②装置中间部分是“冷凝管”,该装置中有一处明显的错误是___________ 。
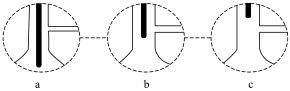
③装置A中,温度计所处的正确位置是___________ 。(选填编号)
海水的综合利用主要包括海水直接利用、海水淡化和海水中化学元素的利用三个方面。其中,海水中化学元素的利用是指从海水中提取钠、镁、氯、溴等元素,以及从海洋植物如海带中提取碘等。
(1)海水中含量最多的卤素是
A.氟 B.氯 C.溴 D.碘
(2)海洋中蕴藏着巨大的化学资源。下列有关海水综合利用的说法正确的是
A.蒸发海水可以得到单质碘
B.蒸馏海水可以得到淡水
C.利用活泼金属钾可置换海水中的镁
D.电解海水可以制得金属钠
(3)下列有关从海水中提取镁的说法错误的是
A.贝壳在海水提取镁的生产流程中,主要经历了
 的过程
的过程B.工业生产中利用电解熔融
 制备镁
制备镁C.在从海水中提取镁的工业流程中,
 可循环使用,用于制备盐酸,再溶解
可循环使用,用于制备盐酸,再溶解
D.利用
 将海水中的
将海水中的 转化为
转化为 沉淀,然后电解
沉淀,然后电解 制备纯镁
制备纯镁(4)下图是海水提溴的工艺流程,下列说法错误的是

A.在海水中加“酸和氯气”,酸的作用是中和海水中的碱性物质
B .“吹出塔”中热空气的作用是将多余的氯气吹出
C.“吸收塔”中发生的反应为
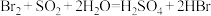
D.以上流程“吹出塔”和“吸收塔”内的反应是为了富集海水中的溴
(5)从海水中提取的粗盐精制后,通过电解饱和食盐水得到一系列化工产品。
①请写出电解饱和食盐水的化学方程式
②检验阳极产物时可选用
③实验测得产生的
 体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为
体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为 。
。(6)实验室模拟工业从海藻中提碘的流程如图:

①选择合适实验操作名称填入流程图中:①
A.溶解 B.过滤 C.萃取 D.分液
从“含碘的有机溶液”中回收溶剂,并得到碘单质,可选用如图装置完成。

②装置中间部分是“冷凝管”,该装置中有一处明显的错误是
③装置A中,温度计所处的正确位置是

您最近一年使用:0次
名校
解题方法
8 . 海水提溴与海带提碘,共同点是
| A.浓缩方法 | B.采用热空气吹出 |
| C.四氯化碳萃取 | D.氧化剂可选择氯水 |
您最近一年使用:0次
2023-04-14更新
|
274次组卷
|
2卷引用:上海市松江区2023届高三二模测试化学试题
名校
解题方法
9 . 海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
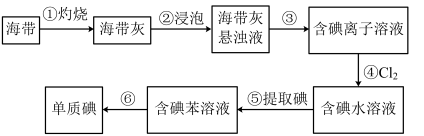
请填写下列空白:
(1)步骤③⑥的实验操作名称分别是_______ 和_______ 。步骤④反应的离子方程式是_______ 。除了氯水,从绿色化学角度考虑,最合适的试剂为_______ 。
A.浓硫酸 B.浓硝酸 C.KMnO4溶液 D.H2O2
(2)步骤⑤中,某学生选择用苯来提取碘的理由有:碘与苯不反应;苯与水不互溶:还有_______ 。从含碘水溶液中获得含碘苯溶液,该操作名称为_______ ,用到最主要仪器为_______ ,不能用酒精代替苯的理由是:_______
(3)向一容积为15 mL的试管中先加入3 mL碘水,再加入1 mL苯,充分振荡、静置后,下列图示现象正确的是_______

关于卤素氯、溴、碘的叙述,错误的是_______
a.单质易溶于有机溶剂中 b. X-的颜色逐渐加深
c.单质氧化性性逐渐减弱 d.X-的还原性逐渐增强

请填写下列空白:
(1)步骤③⑥的实验操作名称分别是
A.浓硫酸 B.浓硝酸 C.KMnO4溶液 D.H2O2
(2)步骤⑤中,某学生选择用苯来提取碘的理由有:碘与苯不反应;苯与水不互溶:还有
(3)向一容积为15 mL的试管中先加入3 mL碘水,再加入1 mL苯,充分振荡、静置后,下列图示现象正确的是

关于卤素氯、溴、碘的叙述,错误的是
a.单质易溶于有机溶剂中 b. X-的颜色逐渐加深
c.单质氧化性性逐渐减弱 d.X-的还原性逐渐增强
您最近一年使用:0次
名校
10 . 碘元素是我们人体不可或缺的微量元素,某化学兴趣小组在实验室模拟工业提碘,流程图如下,请回答下列问题:
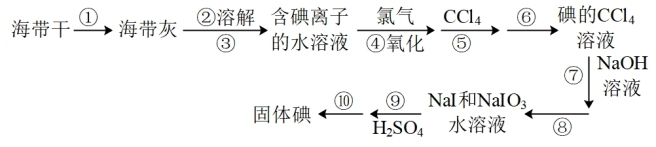
(1)请填写流程图中的操作步骤名称:③___________ ; ⑤___________ ;⑧___________ ;⑩___________ 。
(2)请填写该操作所需要的重要仪器名称:①___________ ;⑥___________ 。
(3)步骤①的目的是:___________ 。步骤④⑤⑥⑦⑧的目的是:___________ 。
(4)检验步骤③后的水溶液中是否含有碘离子的方法是___________ 。
(5)请写出步骤⑦发生的离子方程式:___________ 。
(6)为了获得更纯净的碘单质,针对固体碘可以进行的操作是___________。(填写编号)

(1)请填写流程图中的操作步骤名称:③
(2)请填写该操作所需要的重要仪器名称:①
(3)步骤①的目的是:
(4)检验步骤③后的水溶液中是否含有碘离子的方法是
(5)请写出步骤⑦发生的离子方程式:
(6)为了获得更纯净的碘单质,针对固体碘可以进行的操作是___________。(填写编号)
| A.加入干燥剂,加热升华 | B.蒸馏 |
| C.重结晶 | D.萃取、分液 |
您最近一年使用:0次



