真题
名校
1 . 通过下列实验可从I2,的CCl4溶液中回收I2。

下列说法正确的是


下列说法正确的是
A.NaOH溶液与I2反应的离子方程式:I2+2OH-=I-+IO +H2O +H2O |
| B.通过过滤可将水溶液与CCl4分离 |
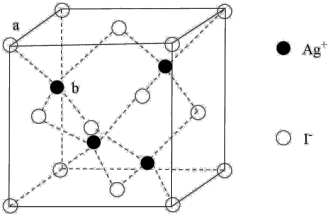
| C.向加酸后的上层清液中滴加AgNO3溶液生成AgI沉淀,1个AgI晶胞(如图)中含14个I- |
| D.回收的粗碘可通过升华进行纯化 |
您最近一年使用:0次
2022-01-04更新
|
5002次组卷
|
8卷引用:2021年新高考江苏化学高考真题
2021年新高考江苏化学高考真题(已下线)押江苏卷第9题 化学工艺流程选择题 -备战2022年高考化学临考题号押题(江苏卷)(已下线)易错点32 物质的分离、提纯与检验-备战2023年高考化学考试易错题广东省昌乐市第一中学2022-2023学年高三上学期期末质量检测化学试题吉林省长春市第五中学2022-2023学年高二下学期第一学程考试化学试题河北省衡水市武强中学2022-2023学年高二下学期期末考试化学试题辽宁省沈阳市第二中学2023-2024学年高三上学期期末模拟考试化学试题(已下线)热点06 物质的聚集状态与晶体的常识
2022·浙江金华·二模
名校
解题方法
2 . 下列方案设计、现象和结论有不正确 的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验海带中是否含有碘元素 | 将海带灰溶解过滤后,取适量滤液于试管中,酸化后加入少量新制氯水,充分反应后加入1~2滴淀粉溶液 | 溶液变蓝,则证明海带中含有碘元素 |
| B | 鉴定淀粉是否完全水解 | 取少量淀粉于锥形瓶中,以固液比1∶10加入稀硫酸,牛皮纸封口,在120℃下水解30min,取适量水解液于试管中,加入少量碘-碘化钾溶液 | 溶液未变蓝,则证明淀粉已完全水解 |
| C | 检验CO还原 的生成物中是否含有 的生成物中是否含有 | 将适量反应后的固体溶于稀盐酸中,取少量溶解液于试管中,滴加硫氰化钾溶液 | 溶液变血红色,则证明还原产物中含有 |
| D | 检验食盐中是否混有少量亚硝酸钠 | 取适量食盐样品于试管中,加水溶解后加入硝酸银溶液,过滤后取滤渣,滴加稀硝酸 | 若沉淀部分溶解,则证明食盐中混有亚硝酸钠 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-04-14更新
|
779次组卷
|
7卷引用:押江苏卷第11题 化学实验综合选择题 -备战2022年高考化学临考题号押题(江苏卷)
(已下线)押江苏卷第11题 化学实验综合选择题 -备战2022年高考化学临考题号押题(江苏卷)江苏省淮安市钦工中学2022-2023学年高三上学期第一次月考化学试题江苏省徐州市第七中学2022-2023学年高三上学期9月摸底学情调研化学试题浙江省金华十校2021-2022学年高三下学期4月模拟考试化学试题(已下线)2022年浙江省6月高考真题变式题21-25湖南省攸县第二中学2022-2023学年高三第六次月考化学试题湖南省攸县第一中学2022-2023学年高三第六次月考化学试题
3 . 围绕海水的综合利用,化学课外兴趣小组进行下列实验:
(1)模拟工业制备氯气
装置如图所示,接通电源,当观察到石墨电极与滤纸接触的区域有细小的气泡产生时,停止通电。将pH试纸分别放在a、b处滤纸上,观察颜色变化。
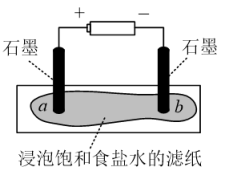
①在上述实验中观察a处pH试纸中心呈白色,边缘有一圈淡淡的红色,b处pH试纸呈___________ 色。
②实验结束后,将滤纸对折,使a、b处充分接触,可将a处残余的Cl2进一步处理。此时发生反应的化学反应方程式是___________ 。
(2)模拟反萃取法提取碘实验流程如下图:
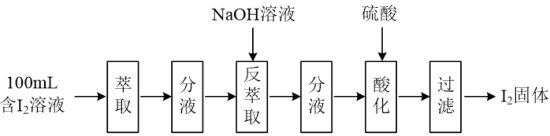
①“萃取”操作时须使用的玻璃仪器有烧杯、玻璃棒和___________ 。
②“反萃取”操作时溶液中有I-、IO 生成。“酸化”步骤发生反应的离子反应方程式为
生成。“酸化”步骤发生反应的离子反应方程式为___________ 。
(3)模拟浓海水提取镁实验流程如下图:
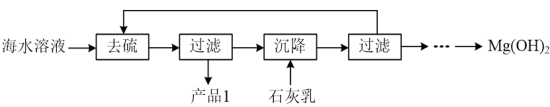
说明:模拟浓海水成分配制的“海水溶液”主要成分如下:
①产品1的化学式为___________ 。
②沉降阶段主要的化学反应方程式为___________ 。
(1)模拟工业制备氯气
装置如图所示,接通电源,当观察到石墨电极与滤纸接触的区域有细小的气泡产生时,停止通电。将pH试纸分别放在a、b处滤纸上,观察颜色变化。

①在上述实验中观察a处pH试纸中心呈白色,边缘有一圈淡淡的红色,b处pH试纸呈
②实验结束后,将滤纸对折,使a、b处充分接触,可将a处残余的Cl2进一步处理。此时发生反应的化学反应方程式是
(2)模拟反萃取法提取碘实验流程如下图:

①“萃取”操作时须使用的玻璃仪器有烧杯、玻璃棒和
②“反萃取”操作时溶液中有I-、IO
 生成。“酸化”步骤发生反应的离子反应方程式为
生成。“酸化”步骤发生反应的离子反应方程式为(3)模拟浓海水提取镁实验流程如下图:

说明:模拟浓海水成分配制的“海水溶液”主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO |
| 浓度/(g·L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
②沉降阶段主要的化学反应方程式为
您最近一年使用:0次
解题方法
4 . 实验室从海带浸取液中提取碘单质。
(1)碘的结构与性质
①碘原子核外有5个电子层,最外层有7个电子,碘元素在周期表中的位置是_______ 。
②质子数为53、中子数为78的碘核素表示为_______ 。
③设计简单的实验验证氯的非金属性比碘强:_____ 。(须用试剂:新制氯水、KI溶液,淀粉溶液)
(2)提取碘单质
I.萃取氧化法:向浸取液中加入 ,调节pH为3~4,加入
,调节pH为3~4,加入 ,再加入
,再加入 溶液,反应一段时间后得到
溶液,反应一段时间后得到 的
的 溶液。
溶液。
①调pH时不用盐酸来替代 的主要原因是
的主要原因是_______ 。(填序号)
a.盐酸易挥发使溶液pH变化快, 不易挥发溶液pH缓慢
不易挥发溶液pH缓慢
b. 为弱电解质,反应过程中电离出
为弱电解质,反应过程中电离出 维持溶液的pH
维持溶液的pH
②加入 的作用是
的作用是_______ ,得到 的
的 溶液。
溶液。
II.双氧化法:把浸取液分成A、B两份,在 催化下用
催化下用 把A溶液中的
把A溶液中的 氧化为
氧化为 ,然后与B溶液混合,经盐酸酸化得到碘单质。
,然后与B溶液混合,经盐酸酸化得到碘单质。
③ 氧化
氧化 的离子方程式为
的离子方程式为_______ 。
④A、B两份溶液的体积比为_______ 时,可使碘的提取率最高。
(3)废液的处理:提取碘后的酸性废液中含有少量的 、
、 ,向废液中加入适量
,向废液中加入适量 把
把 氧化成
氧化成 ,然后加入活性炭,过滤后排放。活性炭的作用是
,然后加入活性炭,过滤后排放。活性炭的作用是_______ 。
(1)碘的结构与性质
①碘原子核外有5个电子层,最外层有7个电子,碘元素在周期表中的位置是
②质子数为53、中子数为78的碘核素表示为
③设计简单的实验验证氯的非金属性比碘强:
(2)提取碘单质
I.萃取氧化法:向浸取液中加入
 ,调节pH为3~4,加入
,调节pH为3~4,加入 ,再加入
,再加入 溶液,反应一段时间后得到
溶液,反应一段时间后得到 的
的 溶液。
溶液。①调pH时不用盐酸来替代
 的主要原因是
的主要原因是a.盐酸易挥发使溶液pH变化快,
 不易挥发溶液pH缓慢
不易挥发溶液pH缓慢b.
 为弱电解质,反应过程中电离出
为弱电解质,反应过程中电离出 维持溶液的pH
维持溶液的pH②加入
 的作用是
的作用是 的
的 溶液。
溶液。II.双氧化法:把浸取液分成A、B两份,在
 催化下用
催化下用 把A溶液中的
把A溶液中的 氧化为
氧化为 ,然后与B溶液混合,经盐酸酸化得到碘单质。
,然后与B溶液混合,经盐酸酸化得到碘单质。③
 氧化
氧化 的离子方程式为
的离子方程式为④A、B两份溶液的体积比为
(3)废液的处理:提取碘后的酸性废液中含有少量的
 、
、 ,向废液中加入适量
,向废液中加入适量 把
把 氧化成
氧化成 ,然后加入活性炭,过滤后排放。活性炭的作用是
,然后加入活性炭,过滤后排放。活性炭的作用是
您最近一年使用:0次
解题方法
5 . 工业上一种从海水中制备碘的方法为:取净化除氯后的含碘海水,加入AgNO3溶液,富集得到AgI悬浊液,进而制得粗碘。从AgI悬浊液中回收I2的流程如图1所示。
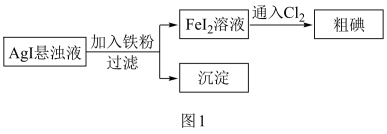
下列有关说法正确的是


下列有关说法正确的是
| A.Fe粉与AgI悬浊液反应的离子方程式为:Fe+2Ag+=Ag+Fe2+ |
| B.可在含碘海水中直接通入Cl2制备粗碘 |
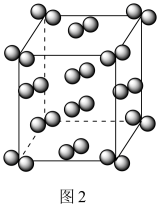
| C.如图2所示I2的晶胞中有14个I2分子 |
| D.流程中沉淀可进一步转化,实现AgNO3的循环使用 |
您最近一年使用:0次
2021-11-12更新
|
378次组卷
|
3卷引用:江苏省盐城市2021-2022学年高三上学期期中考试化学试题
江苏省盐城市2021-2022学年高三上学期期中考试化学试题(已下线)化学-2022年高考押题预测卷01(江苏卷)辽宁省大连市金普新区省示范性高中联合体2021-2022学年高三上学期第二阶段考试化学试题
名校
解题方法
6 . 碘( Godine)是人体必需的微量元素,是维持人体甲状腺正常功能所必需的元素, 人体缺碘时就会患甲状腺肿大,人们主要从饮水、粮食、蔬菜和周围环境中获取碘。多食海带,海鱼等含碘丰富的食品,对于防治甲状腺肿大很有效。某化学课外活动小组在实验室以海带为原料获得少量碘水,并以四氯化碳(沸点76.8℃)为溶剂将碘从碘水中提取出来,甲同学设计实验流程如图所示。请回答下列问题:
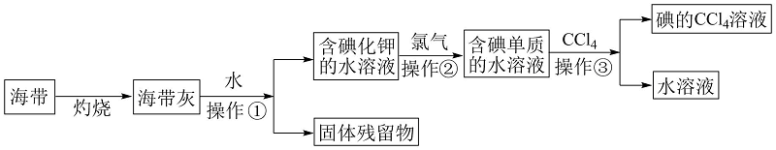
(1)上述流程中灼烧时必须用到最主要 的实验仪器有酒精灯、泥三角和___________ (填名称)。
(2)操作①的名称为___________ ;
(3)操作②中发生反应的离子方程式为______________________ ,乙同学对操作②进行了改进,用绿色氧化剂H2O2代替氯气并加适量稀盐酸,则所发生的离子反应方程式是____________________________________ 。
(4)操作③的实验名称为___________ ,最主要的 实验仪器的名称为___________ ;
(5)丙同学补充增加了一步操作:从碘的CCl4溶液中经过___________ 提取了碘单质并回收CCl4(填该操作名称)
(6)目前,我国推行全民食用的加碘盐是在食盐中加入___________ 这一物质(填写化学式)。

(1)上述流程中灼烧时
(2)操作①的名称为
(3)操作②中发生反应的离子方程式为
(4)操作③的实验名称为
(5)丙同学补充增加了一步操作:从碘的CCl4溶液中经过
(6)目前,我国推行全民食用的加碘盐是在食盐中加入
您最近一年使用:0次
解题方法
7 . 海带提碘是工业碘的主要来源之一,下列说法不正确 的是
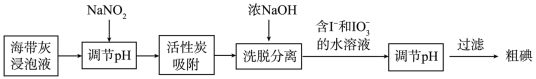

| A.活性炭可以循环使用 |
B.浓NaOH溶液与 反应的离子方程式: 反应的离子方程式: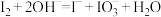 |
| C.两次“调节pH”均可以加稀硫酸调节溶液呈酸性 |
| D.回收的粗碘可通过升华进行提纯 |
您最近一年使用:0次
8 . 围绕海水的综合利用,化学课外兴趣小组进行下列研究。

(1)应用电渗析法制得 的同时可进行海水淡化,是解决淡水资源匮乏的有效途径之一,该方法是利用电解原理通过多组电渗析膜实现,工作原理如图所示,以NaCl溶液代替海水,其中p膜只允许阴离子透过,s膜只允许阳离子透过。直流电源a极为
的同时可进行海水淡化,是解决淡水资源匮乏的有效途径之一,该方法是利用电解原理通过多组电渗析膜实现,工作原理如图所示,以NaCl溶液代替海水,其中p膜只允许阴离子透过,s膜只允许阳离子透过。直流电源a极为___________ (选填“正极”或“负极”),接收淡水的出口是___________ (用字母A、B、C作答),电解总反应方程式为___________ 。
(2)模拟反萃取法提取碘实验流程如下图:
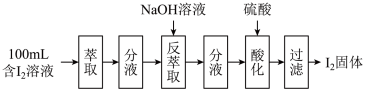
① NaOH的pH=
NaOH的pH=___________ ,由水电离产生的 浓度为
浓度为___________ 。
②“反萃取”操作时溶液中有 、
、 生成。“酸化”步骤发生反应生成碘单质,该反应离子方程式为
生成。“酸化”步骤发生反应生成碘单质,该反应离子方程式为___________ 。

(1)应用电渗析法制得
 的同时可进行海水淡化,是解决淡水资源匮乏的有效途径之一,该方法是利用电解原理通过多组电渗析膜实现,工作原理如图所示,以NaCl溶液代替海水,其中p膜只允许阴离子透过,s膜只允许阳离子透过。直流电源a极为
的同时可进行海水淡化,是解决淡水资源匮乏的有效途径之一,该方法是利用电解原理通过多组电渗析膜实现,工作原理如图所示,以NaCl溶液代替海水,其中p膜只允许阴离子透过,s膜只允许阳离子透过。直流电源a极为(2)模拟反萃取法提取碘实验流程如下图:

①
 NaOH的pH=
NaOH的pH= 浓度为
浓度为②“反萃取”操作时溶液中有
 、
、 生成。“酸化”步骤发生反应生成碘单质,该反应离子方程式为
生成。“酸化”步骤发生反应生成碘单质,该反应离子方程式为
您最近一年使用:0次
解题方法
9 . 海洋中蕴藏着各种油气及矿物资源,海洋的开发利用潜力巨大。下列关于实验室从海带中提取碘的过程说法正确的是
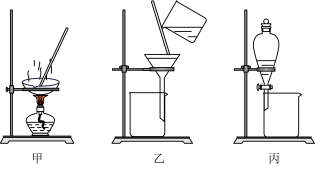

| A.用装置甲灼烧海带成海带灰 |
| B.用装置乙可以过滤海带灰悬浊液 |
| C.用装置甲直接加热含I2溶液可以得到I2 |
| D.装置丙使用时先放出下层液体,接着从下口放出上层液体 |
您最近一年使用:0次
10 . 海洋资源的综合利用是21世纪世界海洋开发利用的重点领域之一。
(1)模拟工业制备氯气
装置如图所示,接通电源,当观察到石墨电极与滤纸接触的区域有细小的气泡产生时,停止通电。将pH试纸分别放在a、b处滤纸上,观察颜色变化。
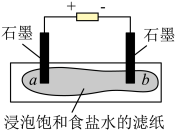
①写出“通电”时发生反应的离子方程式_______ 。
②在上述实验中观察a处pH试纸中心呈白色,边缘有一圈淡淡的红色,b处pH试纸呈_______ 色。
(2)模拟从海水提取食盐后的母液中提取溴的流程如下图:
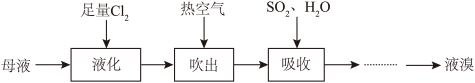
①“吸收”步骤中发生的离子反应方程式为_______ 。
②设计简单的实验验证溴的非金属性比碘强_______ 。(可供选择的试剂:溴水、碘水、NaBr溶液、KI溶液、淀粉溶液)
(3)模拟反萃取法提取碘的实验流程如下图:
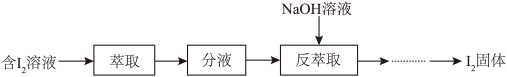
①“萃取”操作中可使用 作为
作为 的萃取剂,其原因除
的萃取剂,其原因除 不与
不与 反应外,还有
反应外,还有_______ 。
②“反萃取”操作时溶液中有 、
、 生成。该步骤发生反应的离子反应方程式:
生成。该步骤发生反应的离子反应方程式:_______ 。
(1)模拟工业制备氯气
装置如图所示,接通电源,当观察到石墨电极与滤纸接触的区域有细小的气泡产生时,停止通电。将pH试纸分别放在a、b处滤纸上,观察颜色变化。

①写出“通电”时发生反应的离子方程式
②在上述实验中观察a处pH试纸中心呈白色,边缘有一圈淡淡的红色,b处pH试纸呈
(2)模拟从海水提取食盐后的母液中提取溴的流程如下图:

①“吸收”步骤中发生的离子反应方程式为
②设计简单的实验验证溴的非金属性比碘强
(3)模拟反萃取法提取碘的实验流程如下图:

①“萃取”操作中可使用
 作为
作为 的萃取剂,其原因除
的萃取剂,其原因除 不与
不与 反应外,还有
反应外,还有②“反萃取”操作时溶液中有
 、
、 生成。该步骤发生反应的离子反应方程式:
生成。该步骤发生反应的离子反应方程式:
您最近一年使用:0次



