解题方法
1 . 请分析海水提镁、海带提碘的主要过程,按要求回答下列问题。
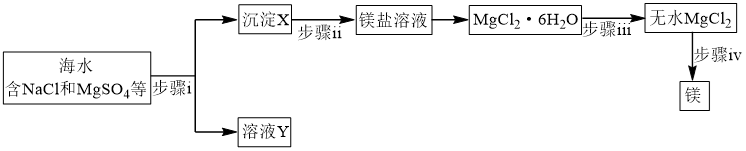
(1)海水提镁
① 在周期表中位于
在周期表中位于_______ 区。
②步骤ⅰ所需试剂属于(填“强酸”、“强碱”或“可溶盐”)_______ 溶液。
③步骤ⅱ反应的离子方程式为_______ 。
④步骤ⅲ系列操作中需在 氛围中进行原因为
氛围中进行原因为_______ 。
⑤步骤ⅳ惰性电极电解熔融 时,在
时,在_______ 极每产生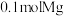 时,电路中转移电子数目为
时,电路中转移电子数目为_______ 。
(2)海带提碘(碘元素在海带中碘化物形式存在,碘为微溶于水的紫黑色固体)
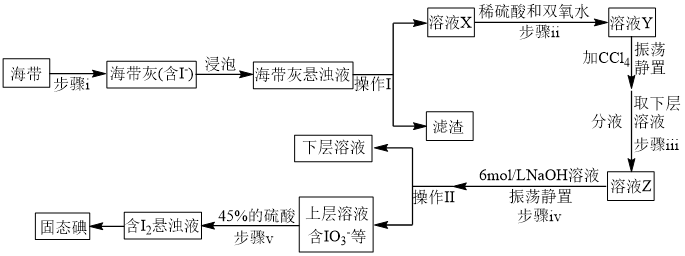
①步骤ⅰ不会用到下列仪器中的_______ (填字母)
a.酒精灯 b.漏斗 c.坩埚 d.泥三角
②操作Ⅰ、Ⅱ的名称依次为_______ 、_______ 。
③步骤ⅱ反应的离子方程式为_______ 。
④步骤ⅲ到步骤Ⅴ的目的是_______ 。
⑤步骤Ⅴ中 参与反应的离子方程式为
参与反应的离子方程式为_______ 。
(1)海水提镁

①
 在周期表中位于
在周期表中位于②步骤ⅰ所需试剂属于(填“强酸”、“强碱”或“可溶盐”)
③步骤ⅱ反应的离子方程式为
④步骤ⅲ系列操作中需在
 氛围中进行原因为
氛围中进行原因为⑤步骤ⅳ惰性电极电解熔融
 时,在
时,在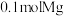 时,电路中转移电子数目为
时,电路中转移电子数目为(2)海带提碘(碘元素在海带中碘化物形式存在,碘为微溶于水的紫黑色固体)

①步骤ⅰ不会用到下列仪器中的
a.酒精灯 b.漏斗 c.坩埚 d.泥三角
②操作Ⅰ、Ⅱ的名称依次为
③步骤ⅱ反应的离子方程式为
④步骤ⅲ到步骤Ⅴ的目的是
⑤步骤Ⅴ中
 参与反应的离子方程式为
参与反应的离子方程式为
您最近一年使用:0次
解题方法
2 . 实验室从海带浸取液中提取碘单质。
(1)碘的结构与性质
①碘原子核外有5个电子层,最外层有7个电子,碘元素在周期表中的位置是_______ 。
②质子数为53、中子数为78的碘核素表示为_______ 。
③设计简单的实验验证氯的非金属性比碘强:_____ 。(须用试剂:新制氯水、KI溶液,淀粉溶液)
(2)提取碘单质
I.萃取氧化法:向浸取液中加入 ,调节pH为3~4,加入
,调节pH为3~4,加入 ,再加入
,再加入 溶液,反应一段时间后得到
溶液,反应一段时间后得到 的
的 溶液。
溶液。
①调pH时不用盐酸来替代 的主要原因是
的主要原因是_______ 。(填序号)
a.盐酸易挥发使溶液pH变化快, 不易挥发溶液pH缓慢
不易挥发溶液pH缓慢
b. 为弱电解质,反应过程中电离出
为弱电解质,反应过程中电离出 维持溶液的pH
维持溶液的pH
②加入 的作用是
的作用是_______ ,得到 的
的 溶液。
溶液。
II.双氧化法:把浸取液分成A、B两份,在 催化下用
催化下用 把A溶液中的
把A溶液中的 氧化为
氧化为 ,然后与B溶液混合,经盐酸酸化得到碘单质。
,然后与B溶液混合,经盐酸酸化得到碘单质。
③ 氧化
氧化 的离子方程式为
的离子方程式为_______ 。
④A、B两份溶液的体积比为_______ 时,可使碘的提取率最高。
(3)废液的处理:提取碘后的酸性废液中含有少量的 、
、 ,向废液中加入适量
,向废液中加入适量 把
把 氧化成
氧化成 ,然后加入活性炭,过滤后排放。活性炭的作用是
,然后加入活性炭,过滤后排放。活性炭的作用是_______ 。
(1)碘的结构与性质
①碘原子核外有5个电子层,最外层有7个电子,碘元素在周期表中的位置是
②质子数为53、中子数为78的碘核素表示为
③设计简单的实验验证氯的非金属性比碘强:
(2)提取碘单质
I.萃取氧化法:向浸取液中加入
 ,调节pH为3~4,加入
,调节pH为3~4,加入 ,再加入
,再加入 溶液,反应一段时间后得到
溶液,反应一段时间后得到 的
的 溶液。
溶液。①调pH时不用盐酸来替代
 的主要原因是
的主要原因是a.盐酸易挥发使溶液pH变化快,
 不易挥发溶液pH缓慢
不易挥发溶液pH缓慢b.
 为弱电解质,反应过程中电离出
为弱电解质,反应过程中电离出 维持溶液的pH
维持溶液的pH②加入
 的作用是
的作用是 的
的 溶液。
溶液。II.双氧化法:把浸取液分成A、B两份,在
 催化下用
催化下用 把A溶液中的
把A溶液中的 氧化为
氧化为 ,然后与B溶液混合,经盐酸酸化得到碘单质。
,然后与B溶液混合,经盐酸酸化得到碘单质。③
 氧化
氧化 的离子方程式为
的离子方程式为④A、B两份溶液的体积比为
(3)废液的处理:提取碘后的酸性废液中含有少量的
 、
、 ,向废液中加入适量
,向废液中加入适量 把
把 氧化成
氧化成 ,然后加入活性炭,过滤后排放。活性炭的作用是
,然后加入活性炭,过滤后排放。活性炭的作用是
您最近一年使用:0次
名校
解题方法
3 . 海洋是一座巨大的化学资源宝库,如图是从海水中或海产品中提取若干种化学物质的流程图。
I.试剂级NaCl可用海盐(含泥沙、海藻、Ca2+、Mg2+、Fe3+、SO 等杂质)为原料制备。
等杂质)为原料制备。

(1)焙炒海盐的目的是______ 。
(2)根据除杂原理,填写合适的试剂③,并选择每步 预期沉淀的离子。
离子:a.Ca2+ b.Mg2+ c.Fe3+ d.SO
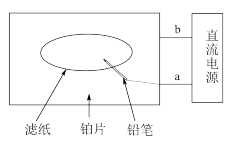
(3)以氯化钠为原料设计了“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。下列叙述正确的是______ 。
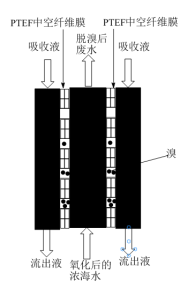
II.国家海洋局科研学者考察了从浓海水中提溴的一种新型方法:聚四氟乙烯(PTFE)气态膜法提溴。本方法关键是采用了PTFE中空纤维膜,在该膜中,水不可以通过,而溴分子可以自主进入和脱离。
将氧化后的浓海水加入气态膜设备预处理,用NaOH溶液作为吸收液配合处理。处理过程的俯视截面示意图如图所示。经流出液氧化后的流出液检验,流出液中含BrO 离子。
离子。
(4)浓海水中溴元素的存在形式是______ ,氧化浓海水时可选用的氧化剂是______ 。
(5)流出液中另外一种含溴物质是______ 。
(6)说明聚四氟乙烯(PTFE)气态膜是如何在上述过程中起到富集作用______ 。
III.小淳同学按如图实验过程,证明海带中存在碘元素。
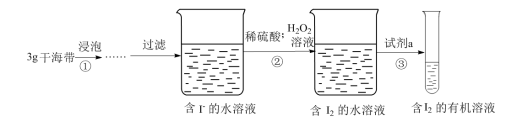
(7)H2O2的作用是______ 。
(8)试剂a不能选择的是(填序号)______ 。
(9)操作③的名称是______ 。
(10)操作③中需要振荡排放气体,放气时分液漏斗的状态是______ 。
小桢同学欲探究I-的性质,进行如图实验:
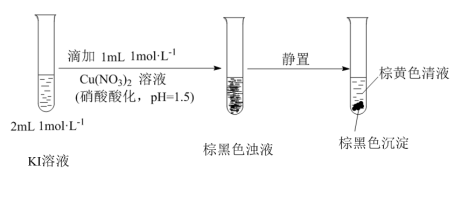
(11)该小组同学推测反应生成了I2。设计实施了如下方案,证实了推测。请将方案补充完整:取棕色清液,______ 。
进一步探究发现:棕黑色沉淀中含有CuI。
(12)由此推知:Cu(NO3)2与KI反应过程中,一定发生的反应的离子方程式为______ 。
I.试剂级NaCl可用海盐(含泥沙、海藻、Ca2+、Mg2+、Fe3+、SO
 等杂质)为原料制备。
等杂质)为原料制备。
(1)焙炒海盐的目的是
(2)根据除杂原理,填写合适的试剂③,并
离子:a.Ca2+ b.Mg2+ c.Fe3+ d.SO

| 实验步骤 | 试剂 | 预期沉淀的离子 |
| 步骤1 | 适量NaOH溶液 | ① |
| 步骤2 | 适量BaCl2溶液 | ② |
| 步骤3 | 适量③ | ④ |
(3)以氯化钠为原料设计了“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。下列叙述正确的是

| A.b极发生还原反应 | B.铂片端作阴极 |
| C.铅笔端有少量的氯气产生 | D.a处是负极 |
II.国家海洋局科研学者考察了从浓海水中提溴的一种新型方法:聚四氟乙烯(PTFE)气态膜法提溴。本方法关键是采用了PTFE中空纤维膜,在该膜中,水不可以通过,而溴分子可以自主进入和脱离。
将氧化后的浓海水加入气态膜设备预处理,用NaOH溶液作为吸收液配合处理。处理过程的俯视截面示意图如图所示。经流出液氧化后的流出液检验,流出液中含BrO
 离子。
离子。
(4)浓海水中溴元素的存在形式是
(5)流出液中另外一种含溴物质是
(6)说明聚四氟乙烯(PTFE)气态膜是如何在上述过程中起到富集作用
III.小淳同学按如图实验过程,证明海带中存在碘元素。

(7)H2O2的作用是
(8)试剂a不能选择的是(填序号)
| A.CCl4 | B.苯 | C.酒精 | D.直馏汽油 |
(9)操作③的名称是
(10)操作③中需要振荡排放气体,放气时分液漏斗的状态是
A.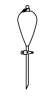 | B.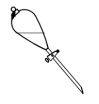 | C.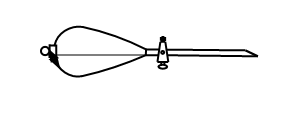 | D. |
小桢同学欲探究I-的性质,进行如图实验:

(11)该小组同学推测反应生成了I2。设计实施了如下方案,证实了推测。请将方案补充完整:取棕色清液,
进一步探究发现:棕黑色沉淀中含有CuI。
(12)由此推知:Cu(NO3)2与KI反应过程中,一定发生的反应的离子方程式为
您最近一年使用:0次
名校
解题方法
4 . 海带提碘过程为海带灼烧为海带灰、用水浸取、过滤,所得浸取液中加氧化剂氧化、萃取分液、加NaOH浓溶液反萃取、酸化后过滤得碘单质。上述过程中,用到的玻璃仪器有
①酒精灯、②烧杯、、③坩埚、④分液漏斗、⑤250mL容量瓶、⑥玻璃棒、⑦漏斗、⑧蒸发皿
①酒精灯、②烧杯、、③坩埚、④分液漏斗、⑤250mL容量瓶、⑥玻璃棒、⑦漏斗、⑧蒸发皿
| A.②③④⑦ | B.①②④⑥⑦ | C.②④⑥⑦ | D.①②③④⑥⑦ |
您最近一年使用:0次
2023-09-23更新
|
220次组卷
|
6卷引用:河北省部分学校2023-2024学年高三一轮复习联考(一)化学试题
5 . 碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。工业上从含碘海水中制备 的一种方法如图所示。已知氧化性
的一种方法如图所示。已知氧化性 ,还原性
,还原性 。回答下列问题:
。回答下列问题:
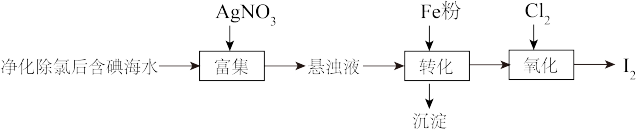
(1)海带中含有丰富的碘元素,处理时应将海带放入_______ (填仪器名称)中进行灼烧得含 的灰烬。
的灰烬。
(2)转化过程加入的Fe粉是过量的,发生的反应为: 。若往转化所得的沉淀中加入稀硫酸,反应的离子方程式为
。若往转化所得的沉淀中加入稀硫酸,反应的离子方程式为_______ ;若要检验转化过程所加Fe粉是否过量,可取适量转化所得的溶液于试管中,加入_______ 溶液,观察现象。
(3)氧化过程可以用适量的酸化的 代替
代替 ,则该反应的离子方程式为
,则该反应的离子方程式为_______ 。用 做氧化剂时也需控制
做氧化剂时也需控制 的用量,若反应物
的用量,若反应物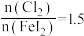 时,氧化产物为
时,氧化产物为 和
和_______ ,当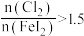 ,
, 会被过量的
会被过量的 进一步氧化从而导致单质碘的收率会降低。
进一步氧化从而导致单质碘的收率会降低。
(4)实验室从含碘废液(除 外,还含有
外,还含有 、
、 、
、 等)中回收碘,其实验过程如图所示:
等)中回收碘,其实验过程如图所示:
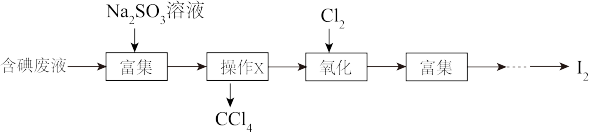
①操作X的名称为_______ 。
②向含碘废液中加入稍过量的 溶液,将废液中的
溶液,将废液中的 还原为
还原为 ,该操作的目的是
,该操作的目的是_______ 。
③氧化时,在三颈烧瓶中将含 的水溶液用盐酸调至pH约为2,缓慢通入
的水溶液用盐酸调至pH约为2,缓慢通入 ,在40℃左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因可能是
,在40℃左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因可能是_______ 。(选填字母编号)
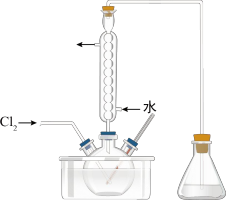
A.增大 的溶解度 B.防止
的溶解度 B.防止 的升华 C.防止水发生分解
的升华 C.防止水发生分解
 的一种方法如图所示。已知氧化性
的一种方法如图所示。已知氧化性 ,还原性
,还原性 。回答下列问题:
。回答下列问题:
(1)海带中含有丰富的碘元素,处理时应将海带放入
 的灰烬。
的灰烬。(2)转化过程加入的Fe粉是过量的,发生的反应为:
 。若往转化所得的沉淀中加入稀硫酸,反应的离子方程式为
。若往转化所得的沉淀中加入稀硫酸,反应的离子方程式为(3)氧化过程可以用适量的酸化的
 代替
代替 ,则该反应的离子方程式为
,则该反应的离子方程式为 做氧化剂时也需控制
做氧化剂时也需控制 的用量,若反应物
的用量,若反应物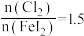 时,氧化产物为
时,氧化产物为 和
和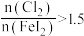 ,
, 会被过量的
会被过量的 进一步氧化从而导致单质碘的收率会降低。
进一步氧化从而导致单质碘的收率会降低。(4)实验室从含碘废液(除
 外,还含有
外,还含有 、
、 、
、 等)中回收碘,其实验过程如图所示:
等)中回收碘,其实验过程如图所示:
①操作X的名称为
②向含碘废液中加入稍过量的
 溶液,将废液中的
溶液,将废液中的 还原为
还原为 ,该操作的目的是
,该操作的目的是③氧化时,在三颈烧瓶中将含
 的水溶液用盐酸调至pH约为2,缓慢通入
的水溶液用盐酸调至pH约为2,缓慢通入 ,在40℃左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因可能是
,在40℃左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因可能是
A.增大
 的溶解度 B.防止
的溶解度 B.防止 的升华 C.防止水发生分解
的升华 C.防止水发生分解
您最近一年使用:0次
名校
6 . 下列叙述不正确的是
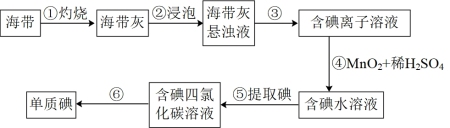

| A.步骤③的分离操作为过滤 |
| B.步骤④中理论上每产生1molI2,需要1molMnO2被氧化 |
| C.步骤⑥操作可以为先加入浓碱过滤,向水层再加入45%硫酸溶液分液,将碘提取出来 |
| D.步骤⑤中加入萃取剂后现象是溶液分层,下层为四氯化碳层呈紫色 |
您最近一年使用:0次
2022-05-15更新
|
199次组卷
|
3卷引用:北京市昌平区第一中学2021-2022学年高一下学期线上期中学情调研化学试题
北京市昌平区第一中学2021-2022学年高一下学期线上期中学情调研化学试题(已下线)第13练 自然资源的开发利用-2022年【暑假分层作业】高一化学(人教版2019必修第二册)北京市昌平区第一中学2022-2023学年高一上学期期中考试化学试题
7 . 我国拥有很长的海岸线,具有丰富的海洋资源。
Ⅰ.盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如图甲所示)。
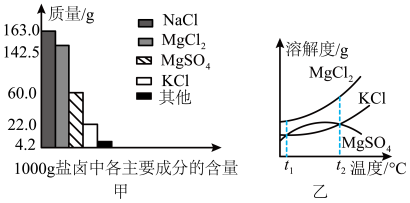
(1)根据图甲所示,写出盐卤中含量最多的盐为__________ 。(填化学式)
(2)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到 以上,根据溶解度曲线,首先析出的晶体应是
以上,根据溶解度曲线,首先析出的晶体应是__________ 。(填化学式)
(3)如图是常用于混合物的分离和提纯的装置:
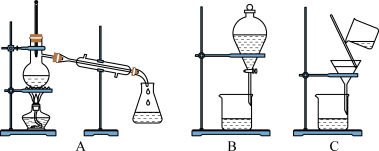
粗盐的提纯应选择图__________ (填字母,下同)装置,若实验中为了除去粗盐中的 、
、 、
、 等杂质离子加入试剂的顺序可以是
等杂质离子加入试剂的顺序可以是__________ 。
A.NaOH、 、
、 、HCl B.NaOH、
、HCl B.NaOH、 、
、 、HCl
、HCl
C. 、
、 、NaOH、HCl D.
、NaOH、HCl D. 、NaOH、
、NaOH、 、HCl
、HCl
Ⅱ.海带是一种含碘量很高的海藻,从中提取的碘广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图。

(4)实验步骤①会用到下列仪器中的__________ (填字母)
a.酒精灯 b.蒸发皿 c.坩埚 d.泥三角
(5)设计实验证明第③步操作后滤液中 的存在,
的存在,______________________________ 。
(6)“提取碘”存在以下两种方案。
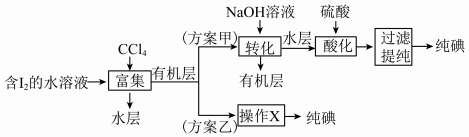
①方案乙中“操作X”的名称是__________ 。
②该流程可循环利用的物质是__________ 。
③采用方案乙得到纯碘的产率较低,原因是______________________________ 。
Ⅰ.盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如图甲所示)。

(1)根据图甲所示,写出盐卤中含量最多的盐为
(2)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到
 以上,根据溶解度曲线,首先析出的晶体应是
以上,根据溶解度曲线,首先析出的晶体应是(3)如图是常用于混合物的分离和提纯的装置:

粗盐的提纯应选择图
 、
、 、
、 等杂质离子加入试剂的顺序可以是
等杂质离子加入试剂的顺序可以是A.NaOH、
 、
、 、HCl B.NaOH、
、HCl B.NaOH、 、
、 、HCl
、HClC.
 、
、 、NaOH、HCl D.
、NaOH、HCl D. 、NaOH、
、NaOH、 、HCl
、HClⅡ.海带是一种含碘量很高的海藻,从中提取的碘广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图。

(4)实验步骤①会用到下列仪器中的
a.酒精灯 b.蒸发皿 c.坩埚 d.泥三角
(5)设计实验证明第③步操作后滤液中
 的存在,
的存在,(6)“提取碘”存在以下两种方案。

①方案乙中“操作X”的名称是
②该流程可循环利用的物质是
③采用方案乙得到纯碘的产率较低,原因是
您最近一年使用:0次
2023-12-27更新
|
190次组卷
|
2卷引用:河北省保定市1+3联考2023-2024学年高一上学期12月月考化学试题
名校
8 . 碘在科研与生活中有重要作用。
Ⅰ.实验室按如下实验流程提取海带中的碘。___________ (从下列图中选择,写出名称)。___________ 。
(3)海带灰中含有的其他可溶性无机盐,是在___________ (从以上流程中选填实验操作名称)中实现与碘分离。
Ⅱ.测定反应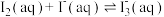 的平衡常数K
的平衡常数K
常温下,取2个碘量瓶分别加入下表中的药品,振荡半小时,均有少量固体不溶。取一定体积的上层清液,加入淀粉作指示剂,用c1 mol L-1 Na2S2O3溶液进行滴定(发生反应
L-1 Na2S2O3溶液进行滴定(发生反应 ),测定
),测定 和
和 的总浓度,进而可以测得K。
的总浓度,进而可以测得K。
(注:在本实验中,认为碘在水中和KI溶液中达到饱和时,它们的碘分子浓度c(I2)相等)
(4)Na2S2O3溶液也可以滴定 的原因是
的原因是___________ (用平衡移动原理回答);滴定终点的实验现象为___________ 。
(5)实验I中,c( )=
)=___________ mol/L(用含c1、c2、c3或c4的式子表示,下同),反应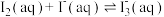 的平衡常数K=
的平衡常数K=___________ 。
(6)若所加的碘偏少,导致实验I中碘量瓶振荡半小时后无固体剩余(不饱和),而实验Ⅱ的碘量瓶中仍有固体不溶,则测得的K将___________ (填“偏大”、“偏小”或“无影响”)。
Ⅰ.实验室按如下实验流程提取海带中的碘。


(3)海带灰中含有的其他可溶性无机盐,是在
Ⅱ.测定反应
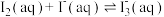 的平衡常数K
的平衡常数K常温下,取2个碘量瓶分别加入下表中的药品,振荡半小时,均有少量固体不溶。取一定体积的上层清液,加入淀粉作指示剂,用c1 mol
 L-1 Na2S2O3溶液进行滴定(发生反应
L-1 Na2S2O3溶液进行滴定(发生反应 ),测定
),测定 和
和 的总浓度,进而可以测得K。
的总浓度,进而可以测得K。(注:在本实验中,认为碘在水中和KI溶液中达到饱和时,它们的碘分子浓度c(I2)相等)
| 碘量瓶 (实验Ⅰ) | 碘量瓶 (实验Ⅱ) | |
| 药品 | 0.5 g研细的碘,100 mL c2 mol L-1 KI L-1 KI | 0.5 g研细的碘,100 mL H2O |
| I2和I3-的总浓度 | c3 mol L-1 L-1 | c4 mol L-1 L-1 |
 的原因是
的原因是(5)实验I中,c(
 )=
)=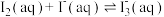 的平衡常数K=
的平衡常数K=(6)若所加的碘偏少,导致实验I中碘量瓶振荡半小时后无固体剩余(不饱和),而实验Ⅱ的碘量瓶中仍有固体不溶,则测得的K将
您最近一年使用:0次
2024-04-24更新
|
177次组卷
|
2卷引用:广东省广州市五校(省实、广雅、执信、二中、六中)2023-2024学年高二上学期期末联考化学试题
名校
解题方法
9 . 从海带中提取碘的主要流程如下,下列说法中错误的是


| A.海带具有富集碘的能力 |
| B.过滤时用到的玻璃仪器有漏斗、烧杯、玻璃棒 |
| C.用苯萃取碘时,上层呈红棕色,下层几乎无色 |
D.可以用淀粉检验含碘水溶液中的 |
您最近一年使用:0次
名校
10 . 某学习小组拟在实验室从海带中提取碘单质,设计流程如图所示。下列说法正确的是
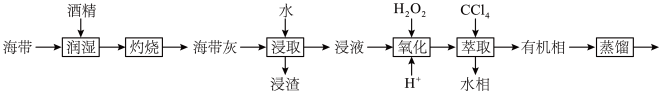

| A.“灼烧”海带应在蒸发皿中进行,并且用玻璃棒搅拌 |
B.海带灰中除了含有较多的 外,还有其他无机质 外,还有其他无机质 |
C.“氧化”时用足量 代替 代替 ,可获得较多的 ,可获得较多的 |
| D.蒸馏和萃取均需用到的玻璃仪器是分液漏斗 |
您最近一年使用:0次
2022-11-28更新
|
300次组卷
|
5卷引用:安徽省铜陵市等5地2022届高三下学期二模统考化学试题



