名校
1 . 海洋植物如海带,海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下:(已知: )。
)。
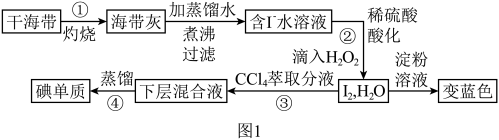
(1)以上步骤不需要用到的仪器是_______。
(2)选用试剂 的理由是_______。
的理由是_______。
(3)写出步骤②中反应的离子方程式_______ 。
(4)工业制备过程中,步骤④很难达到目的,常对图1步骤④进行如下改进:
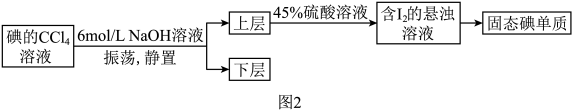
写出上述流程中加入45%硫酸溶液一步反应的离子方程式_______ 。
(5)向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
①已知碘元素最终变为无色HIO3。上述整个过程中的还原剂有_______ 。
②若把KI成KBr,则CCl4层变为_______ 色,继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是_______ 。
 )。
)。
(1)以上步骤不需要用到的仪器是_______。
A. | B. | C. | D. |
 的理由是_______。
的理由是_______。A. 不溶于水 不溶于水 | B. 的密度比水大 的密度比水大 |
C.碘在 中比在水中溶解度更大 中比在水中溶解度更大 | D. 与碘水不反应 与碘水不反应 |
(4)工业制备过程中,步骤④很难达到目的,常对图1步骤④进行如下改进:

写出上述流程中加入45%硫酸溶液一步反应的离子方程式
(5)向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
①已知碘元素最终变为无色HIO3。上述整个过程中的还原剂有
②若把KI成KBr,则CCl4层变为
您最近一年使用:0次
解题方法
2 .  常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备
常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备 的一种流程如下:
的一种流程如下:
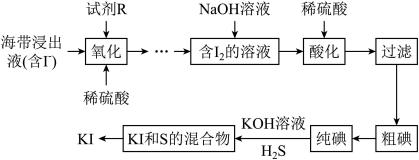
回答下列问题:
(1)“酸化”时稀硫酸的作用是___________ 。
(2)分离 和S的混合物得到
和S的混合物得到 溶液的试剂和方法如下,正确的是
溶液的试剂和方法如下,正确的是___________ (填标号)。
(3)利用下图装置完成 与
与 反应制备
反应制备 。
。

① 溶液的作用是
溶液的作用是___________ (用离子方程式表示)。
②三颈烧瓶中产生 的正确操作顺序为
的正确操作顺序为___________ (填标号)。
a.旋开活塞K,通入 b.加入稀硫酸 c.加入
b.加入稀硫酸 c.加入 溶液
溶液
(4)产品纯度测定。
准确称取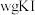 样品溶于水配成
样品溶于水配成 溶液,量取
溶液,量取 溶液于锥形瓶中,加入足量用稀硫酸酸化的
溶液于锥形瓶中,加入足量用稀硫酸酸化的 溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用
溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用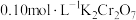 标准溶液反应至完全(还原产物只有
标准溶液反应至完全(还原产物只有 ),消耗标准溶液
),消耗标准溶液 。该
。该 产品的纯度为
产品的纯度为___________ (用含w,V的式子表示)。
 常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备
常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备 的一种流程如下:
的一种流程如下:
回答下列问题:
(1)“酸化”时稀硫酸的作用是
(2)分离
 和S的混合物得到
和S的混合物得到 溶液的试剂和方法如下,正确的是
溶液的试剂和方法如下,正确的是| 选项 | 试剂 | 方法 |
| a | 二硫化碳 | 分液 |
| b | 酒精 | 分液 |
| c |  溶液 溶液 | 过滤 |
(3)利用下图装置完成
 与
与 反应制备
反应制备 。
。
①
 溶液的作用是
溶液的作用是②三颈烧瓶中产生
 的正确操作顺序为
的正确操作顺序为a.旋开活塞K,通入
 b.加入稀硫酸 c.加入
b.加入稀硫酸 c.加入 溶液
溶液(4)产品纯度测定。
准确称取
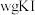 样品溶于水配成
样品溶于水配成 溶液,量取
溶液,量取 溶液于锥形瓶中,加入足量用稀硫酸酸化的
溶液于锥形瓶中,加入足量用稀硫酸酸化的 溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用
溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用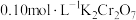 标准溶液反应至完全(还原产物只有
标准溶液反应至完全(还原产物只有 ),消耗标准溶液
),消耗标准溶液 。该
。该 产品的纯度为
产品的纯度为
您最近一年使用:0次
名校
解题方法
3 . 海带中含有丰富的碘元素,从海带中提取碘,可经过以下实验步骤完成。
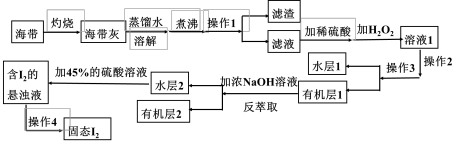
回答下列问题:
(1)灼烧的目的是___________ 。
(2)操作2和操作3用到的玻璃仪器有___________ 。
(3)若有机层1在下层,则有机层2主要成分可能为___________ 。
(4)加入H2O2,发生反应的离子方程式为___________ 。
(5)用铂丝蘸取少量水层2中溶液在酒精灯上灼烧,可观察到___________ 色。
(6)反萃取过程发生反应的离子方程式为___________ 。

回答下列问题:
(1)灼烧的目的是
(2)操作2和操作3用到的玻璃仪器有
(3)若有机层1在下层,则有机层2主要成分可能为
(4)加入H2O2,发生反应的离子方程式为
(5)用铂丝蘸取少量水层2中溶液在酒精灯上灼烧,可观察到
(6)反萃取过程发生反应的离子方程式为
您最近一年使用:0次
解题方法
4 . 已知 悬浊液,加入Fe粉
悬浊液,加入Fe粉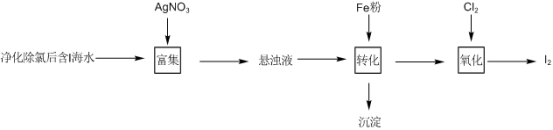 进行转化反应的离子方程式为
进行转化反应的离子方程式为_______ ,生成的沉淀与硝酸反应,生成_______ 后可循环使用。
 悬浊液,加入Fe粉
悬浊液,加入Fe粉 进行转化反应的离子方程式为
进行转化反应的离子方程式为
您最近一年使用:0次
解题方法
5 . 利用下列玻璃仪器(导管及非玻璃仪器任选)能完成的实验是


| A.实验室制乙烯 | B.配制 硫酸 硫酸 |
| C.从海带灰中提取碘单质 | D.实验室制乙酸乙酯 |
您最近一年使用:0次
6 . 海洋资源的综合利用是21世纪世界海洋开发利用的重点领域之一。
(1)模拟工业制备氯气
装置如图所示,接通电源,当观察到石墨电极与滤纸接触的区域有细小的气泡产生时,停止通电。将pH试纸分别放在a、b处滤纸上,观察颜色变化。
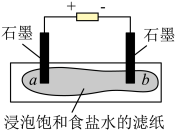
①写出“通电”时发生反应的离子方程式_______ 。
②在上述实验中观察a处pH试纸中心呈白色,边缘有一圈淡淡的红色,b处pH试纸呈_______ 色。
(2)模拟从海水提取食盐后的母液中提取溴的流程如下图:
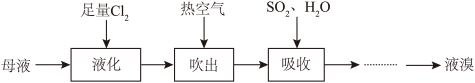
①“吸收”步骤中发生的离子反应方程式为_______ 。
②设计简单的实验验证溴的非金属性比碘强_______ 。(可供选择的试剂:溴水、碘水、NaBr溶液、KI溶液、淀粉溶液)
(3)模拟反萃取法提取碘的实验流程如下图:
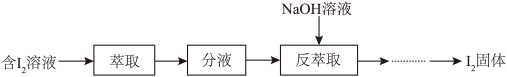
①“萃取”操作中可使用 作为
作为 的萃取剂,其原因除
的萃取剂,其原因除 不与
不与 反应外,还有
反应外,还有_______ 。
②“反萃取”操作时溶液中有 、
、 生成。该步骤发生反应的离子反应方程式:
生成。该步骤发生反应的离子反应方程式:_______ 。
(1)模拟工业制备氯气
装置如图所示,接通电源,当观察到石墨电极与滤纸接触的区域有细小的气泡产生时,停止通电。将pH试纸分别放在a、b处滤纸上,观察颜色变化。

①写出“通电”时发生反应的离子方程式
②在上述实验中观察a处pH试纸中心呈白色,边缘有一圈淡淡的红色,b处pH试纸呈
(2)模拟从海水提取食盐后的母液中提取溴的流程如下图:

①“吸收”步骤中发生的离子反应方程式为
②设计简单的实验验证溴的非金属性比碘强
(3)模拟反萃取法提取碘的实验流程如下图:

①“萃取”操作中可使用
 作为
作为 的萃取剂,其原因除
的萃取剂,其原因除 不与
不与 反应外,还有
反应外,还有②“反萃取”操作时溶液中有
 、
、 生成。该步骤发生反应的离子反应方程式:
生成。该步骤发生反应的离子反应方程式:
您最近一年使用:0次
解题方法
7 . 开发和利用海洋资源是当前科学研究的一项重要任务,如图是某化工厂对海洋资源综合利用的流程图:
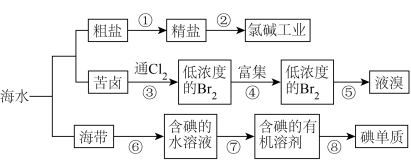
请回答下列问题:
(1)粗盐中含有泥沙、 、
、 、
、 等杂质,精制时一般步骤如下:
等杂质,精制时一般步骤如下:
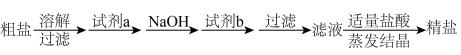
加入的试剂a、b分别是___________ 、___________ 。
(2)③中发生反应的离子方程式为___________ ,可推断氧化性:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(3)⑥通常分三个步骤:
第1步:灼烧,将足量海带灼烧成灰烬;
第2步: 溶液的获取;
溶液的获取;
第3步:氧化。
下列仪器在第1步中不会用到的有___________ 。
A.试管B.瓷坩埚C.坩埚钳D.铁三脚架E.泥三角F.酒精灯G.烧杯H.量筒
第3步中最好选用的氧化剂是___________ 。
A.浓硫酸B.新制氯水C.酸性高锰酸钾D.
(4)⑦中所用的操作方法有___________ 、___________ 。

请回答下列问题:
(1)粗盐中含有泥沙、
 、
、 、
、 等杂质,精制时一般步骤如下:
等杂质,精制时一般步骤如下:
加入的试剂a、b分别是
(2)③中发生反应的离子方程式为

 (填“>”或“<”)。
(填“>”或“<”)。(3)⑥通常分三个步骤:
第1步:灼烧,将足量海带灼烧成灰烬;
第2步:
 溶液的获取;
溶液的获取;第3步:氧化。
下列仪器在第1步中不会用到的有
A.试管B.瓷坩埚C.坩埚钳D.铁三脚架E.泥三角F.酒精灯G.烧杯H.量筒
第3步中最好选用的氧化剂是
A.浓硫酸B.新制氯水C.酸性高锰酸钾D.

(4)⑦中所用的操作方法有
您最近一年使用:0次
8 . 海带中含有丰富的碘,某中学实验小组为了提取和检验海带灰中的碘,设计了以下实验流程。(已知:海带灰中的碘元素主要以 形式存在)
形式存在)
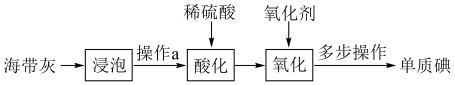
(1)“浸泡”时需充分搅拌,并将悬浊液煮沸2~3分钟,主要的目的是___________ (写一条即可)。
(2)操作a需要用到的玻璃仪器,除烧杯外,还需要___________ 。
(3)“酸化”时需要稀硫酸,回答下列有关问题:
①配制 稀硫酸,需要质量分数为98%的浓硫酸(密度:
稀硫酸,需要质量分数为98%的浓硫酸(密度: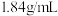 )的体积约为
)的体积约为___________  。(已知:用量筒取用浓硫酸)
。(已知:用量筒取用浓硫酸)
②配制过程的部分操作如下图,则操作步骤的正确顺序为___________ 。(用字母序号表示)
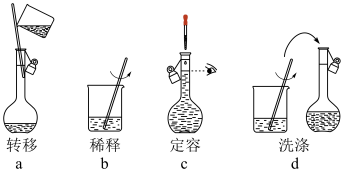
③下列有关配制上述稀硫酸的描述正确的是___________
A.稀释时将蒸馏水缓缓注入盛有浓硫酸的烧杯中
B.溶液未冷却至室温,立即转移、定容
C.定容时俯视容量瓶的刻度线,导致所配溶液的浓度偏大
D.将所配的稀硫酸分装于带橡胶塞的广口瓶中
(4)“氧化”时氧化剂的选择将影响实验结果。
①若选用 ,“氧化”时发生反应的离子方程式为
,“氧化”时发生反应的离子方程式为___________ 。
②若选用 ,过量的
,过量的 可将碘单质氧化成
可将碘单质氧化成 ,其反应的化学方程式为
,其反应的化学方程式为___________ 。
(5)检验“氧化”后的水溶液中是否含有单质碘的实验操作方法___________ 。
 形式存在)
形式存在)
(1)“浸泡”时需充分搅拌,并将悬浊液煮沸2~3分钟,主要的目的是
(2)操作a需要用到的玻璃仪器,除烧杯外,还需要
(3)“酸化”时需要稀硫酸,回答下列有关问题:
①配制
 稀硫酸,需要质量分数为98%的浓硫酸(密度:
稀硫酸,需要质量分数为98%的浓硫酸(密度: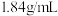 )的体积约为
)的体积约为 。(已知:用量筒取用浓硫酸)
。(已知:用量筒取用浓硫酸)②配制过程的部分操作如下图,则操作步骤的正确顺序为

③下列有关配制上述稀硫酸的描述正确的是
A.稀释时将蒸馏水缓缓注入盛有浓硫酸的烧杯中
B.溶液未冷却至室温,立即转移、定容
C.定容时俯视容量瓶的刻度线,导致所配溶液的浓度偏大
D.将所配的稀硫酸分装于带橡胶塞的广口瓶中
(4)“氧化”时氧化剂的选择将影响实验结果。
①若选用
 ,“氧化”时发生反应的离子方程式为
,“氧化”时发生反应的离子方程式为②若选用
 ,过量的
,过量的 可将碘单质氧化成
可将碘单质氧化成 ,其反应的化学方程式为
,其反应的化学方程式为(5)检验“氧化”后的水溶液中是否含有单质碘的实验操作方法
您最近一年使用:0次
名校
解题方法
9 . 氢气在工业上可用于海水提溴、海带提碘。
Ⅰ.海水提溴工业流程如下图。
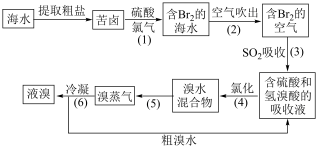
(1)骤(1)中,加硫酸的目的是___________ ;步骤(2)利用了溴的什么物理性质?___________ 。该空气的温度一般控制在80~90℃,温度过高有何不妥?___________ 。
(2)步骤(3)反应中,氧化产物是___________ 。该反应的离子方程式为___________ 。
(3)步骤(2)(3)(4)的目的是___________ 。
(4)步骤(5)、(6)的操作名称依次为___________ 、___________ 。
Ⅱ.海藻中含有丰富的碘元素。实验室中提取碘的流程如下:

(5)步骤①的目的是___________ 。欲确认步骤③中的反应已发生,可取样,加___________ (试剂名称)。
(6)在实验室中进行步骤④操作需要的仪器是___________ 。步骤⑤的名称为___________ 。
(7)关于海水提溴、海藻提碘,下列说法正确的是___________;
Ⅰ.海水提溴工业流程如下图。

(1)骤(1)中,加硫酸的目的是
(2)步骤(3)反应中,氧化产物是
(3)步骤(2)(3)(4)的目的是
(4)步骤(5)、(6)的操作名称依次为
Ⅱ.海藻中含有丰富的碘元素。实验室中提取碘的流程如下:

(5)步骤①的目的是
(6)在实验室中进行步骤④操作需要的仪器是
(7)关于海水提溴、海藻提碘,下列说法正确的是___________;
| A.都需经过浓缩、氧化、提取 |
B.海水提溴的浓缩原理是蒸发,提高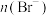 |
C.都可通氯气将 、 、 分别还原为 分别还原为 、 、 |
D.海藻提碘可采用 萃取 萃取 ,海水提溴没有萃取操作 ,海水提溴没有萃取操作 |
您最近一年使用:0次
名校
10 . 碘在科研与生活中有重要作用。
Ⅰ.实验室按如下实验流程提取海带中的碘。___________ (从下列图中选择,写出名称)。___________ 。
(3)海带灰中含有的其他可溶性无机盐,是在___________ (从以上流程中选填实验操作名称)中实现与碘分离。
Ⅱ.测定反应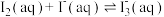 的平衡常数K
的平衡常数K
常温下,取2个碘量瓶分别加入下表中的药品,振荡半小时,均有少量固体不溶。取一定体积的上层清液,加入淀粉作指示剂,用c1 mol L-1 Na2S2O3溶液进行滴定(发生反应
L-1 Na2S2O3溶液进行滴定(发生反应 ),测定
),测定 和
和 的总浓度,进而可以测得K。
的总浓度,进而可以测得K。
(注:在本实验中,认为碘在水中和KI溶液中达到饱和时,它们的碘分子浓度c(I2)相等)
(4)Na2S2O3溶液也可以滴定 的原因是
的原因是___________ (用平衡移动原理回答);滴定终点的实验现象为___________ 。
(5)实验I中,c( )=
)=___________ mol/L(用含c1、c2、c3或c4的式子表示,下同),反应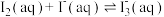 的平衡常数K=
的平衡常数K=___________ 。
(6)若所加的碘偏少,导致实验I中碘量瓶振荡半小时后无固体剩余(不饱和),而实验Ⅱ的碘量瓶中仍有固体不溶,则测得的K将___________ (填“偏大”、“偏小”或“无影响”)。
Ⅰ.实验室按如下实验流程提取海带中的碘。


(3)海带灰中含有的其他可溶性无机盐,是在
Ⅱ.测定反应
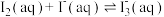 的平衡常数K
的平衡常数K常温下,取2个碘量瓶分别加入下表中的药品,振荡半小时,均有少量固体不溶。取一定体积的上层清液,加入淀粉作指示剂,用c1 mol
 L-1 Na2S2O3溶液进行滴定(发生反应
L-1 Na2S2O3溶液进行滴定(发生反应 ),测定
),测定 和
和 的总浓度,进而可以测得K。
的总浓度,进而可以测得K。(注:在本实验中,认为碘在水中和KI溶液中达到饱和时,它们的碘分子浓度c(I2)相等)
| 碘量瓶 (实验Ⅰ) | 碘量瓶 (实验Ⅱ) | |
| 药品 | 0.5 g研细的碘,100 mL c2 mol L-1 KI L-1 KI | 0.5 g研细的碘,100 mL H2O |
| I2和I3-的总浓度 | c3 mol L-1 L-1 | c4 mol L-1 L-1 |
 的原因是
的原因是(5)实验I中,c(
 )=
)=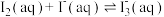 的平衡常数K=
的平衡常数K=(6)若所加的碘偏少,导致实验I中碘量瓶振荡半小时后无固体剩余(不饱和),而实验Ⅱ的碘量瓶中仍有固体不溶,则测得的K将
您最近一年使用:0次



