解题方法
1 . 卤族元素包含F(氟)、Cl(氯)、Br(溴)和I(碘)等元素,卤族元素的单质及其化合物在生产生活中有着重要的应用,人们从自然界中获得卤族单质及基化合物的过程,体现了化学科学在利用自然资源创造新物质中的独特作用,根据所学知识及所给信息,回答下列问题:
(1)写出 的离子结构示意图
的离子结构示意图_______ 。
(2)氯元素存在 、
、 两种核素,由这两种
两种核素,由这两种 、
、 核素构成的氯气单质有
核素构成的氯气单质有_______ 种。
(3)将氯气通入紫色石蕊溶液中,实验的现象是_______ ,结合离子方程式加上必要的文字解释原因_______ 。
(4)从海带中提取碘单质的工艺流程如下,其中海带灰溶于水后碘的存在形成是 。干海带
。干海带 海带灰
海带灰 悬浊液
悬浊液 滤液
滤液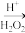 碘水。工艺流程中不会用到的实验仪器有
碘水。工艺流程中不会用到的实验仪器有_______ 。
①酒精灯 ②三脚架 ③泥三角 ④分液漏斗 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒 ⑧量筒 ⑨漏斗
向“滤液”中加入 和
和 发生的离子方程式为
发生的离子方程式为_______ ;检验提取的碘水中含有 的试剂是
的试剂是_______ 。
(5)从海水晒盐后的盐卤(主要含 、
、 、
、 、
、 等)中模拟工业生产来提取镁,主要流程如图:
等)中模拟工业生产来提取镁,主要流程如图:

从流程提取镁的反应①~⑥中,没有涉及到的四种基本反应类型的是_______ 反应。工业上从盐卤中获取 用石灰乳而不用NaOH溶液的原因是
用石灰乳而不用NaOH溶液的原因是_______ 。写出 与盐酸反应的离子方程式
与盐酸反应的离子方程式_______ 。
(1)写出
 的离子结构示意图
的离子结构示意图(2)氯元素存在
 、
、 两种核素,由这两种
两种核素,由这两种 、
、 核素构成的氯气单质有
核素构成的氯气单质有(3)将氯气通入紫色石蕊溶液中,实验的现象是
(4)从海带中提取碘单质的工艺流程如下,其中海带灰溶于水后碘的存在形成是
 。干海带
。干海带 海带灰
海带灰 悬浊液
悬浊液 滤液
滤液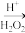 碘水。工艺流程中不会用到的实验仪器有
碘水。工艺流程中不会用到的实验仪器有①酒精灯 ②三脚架 ③泥三角 ④分液漏斗 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒 ⑧量筒 ⑨漏斗
向“滤液”中加入
 和
和 发生的离子方程式为
发生的离子方程式为 的试剂是
的试剂是(5)从海水晒盐后的盐卤(主要含
 、
、 、
、 、
、 等)中模拟工业生产来提取镁,主要流程如图:
等)中模拟工业生产来提取镁,主要流程如图:
从流程提取镁的反应①~⑥中,没有涉及到的四种基本反应类型的是
 用石灰乳而不用NaOH溶液的原因是
用石灰乳而不用NaOH溶液的原因是 与盐酸反应的离子方程式
与盐酸反应的离子方程式
您最近一年使用:0次
2 . 围绕海水的综合利用,化学课外兴趣小组进行下列研究。

(1)应用电渗析法制得 的同时可进行海水淡化,是解决淡水资源匮乏的有效途径之一,该方法是利用电解原理通过多组电渗析膜实现,工作原理如图所示,以NaCl溶液代替海水,其中p膜只允许阴离子透过,s膜只允许阳离子透过。直流电源a极为
的同时可进行海水淡化,是解决淡水资源匮乏的有效途径之一,该方法是利用电解原理通过多组电渗析膜实现,工作原理如图所示,以NaCl溶液代替海水,其中p膜只允许阴离子透过,s膜只允许阳离子透过。直流电源a极为___________ (选填“正极”或“负极”),接收淡水的出口是___________ (用字母A、B、C作答),电解总反应方程式为___________ 。
(2)模拟反萃取法提取碘实验流程如下图:
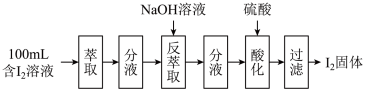
① NaOH的pH=
NaOH的pH=___________ ,由水电离产生的 浓度为
浓度为___________ 。
②“反萃取”操作时溶液中有 、
、 生成。“酸化”步骤发生反应生成碘单质,该反应离子方程式为
生成。“酸化”步骤发生反应生成碘单质,该反应离子方程式为___________ 。

(1)应用电渗析法制得
 的同时可进行海水淡化,是解决淡水资源匮乏的有效途径之一,该方法是利用电解原理通过多组电渗析膜实现,工作原理如图所示,以NaCl溶液代替海水,其中p膜只允许阴离子透过,s膜只允许阳离子透过。直流电源a极为
的同时可进行海水淡化,是解决淡水资源匮乏的有效途径之一,该方法是利用电解原理通过多组电渗析膜实现,工作原理如图所示,以NaCl溶液代替海水,其中p膜只允许阴离子透过,s膜只允许阳离子透过。直流电源a极为(2)模拟反萃取法提取碘实验流程如下图:

①
 NaOH的pH=
NaOH的pH= 浓度为
浓度为②“反萃取”操作时溶液中有
 、
、 生成。“酸化”步骤发生反应生成碘单质,该反应离子方程式为
生成。“酸化”步骤发生反应生成碘单质,该反应离子方程式为
您最近一年使用:0次
名校
3 . 碘是人体必须的微量元素之一,海洋植物如海带、海藻中含有丰富的碘元素。在实验室中,从海藻里提取碘的流程如下:
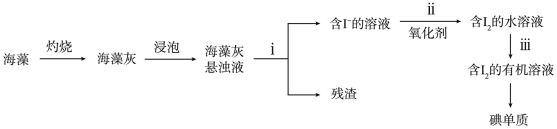
(1)指出上述过程中有关实验操作的名称,步骤i:___________ ,步骤iii:___________ 。
(2)步骤ii中可使用 ,从原子结构角度说明理由:
,从原子结构角度说明理由:___________ 。 过量时,可能无法获得
过量时,可能无法获得 ,原因是
,原因是 会被继续氧化为
会被继续氧化为 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(3)当使用 做氧化剂时,
做氧化剂时, 的转化率受外界因素的影响如下图所示。
的转化率受外界因素的影响如下图所示。
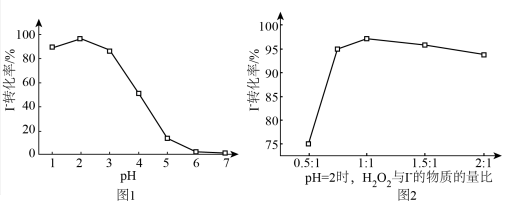
①图1中, 时
时 转化率几乎为0,结合离子方程式解释原因:
转化率几乎为0,结合离子方程式解释原因:___________ 。
②图2中, 与
与 物质的量之比从0.5﹕1提高至1﹕1时,
物质的量之比从0.5﹕1提高至1﹕1时, 的转化率明显增大,可能的原因是
的转化率明显增大,可能的原因是___________ (写出2条)。

(1)指出上述过程中有关实验操作的名称,步骤i:
(2)步骤ii中可使用
 ,从原子结构角度说明理由:
,从原子结构角度说明理由: 过量时,可能无法获得
过量时,可能无法获得 ,原因是
,原因是 会被继续氧化为
会被继续氧化为 ,该反应的离子方程式为
,该反应的离子方程式为(3)当使用
 做氧化剂时,
做氧化剂时, 的转化率受外界因素的影响如下图所示。
的转化率受外界因素的影响如下图所示。
①图1中,
 时
时 转化率几乎为0,结合离子方程式解释原因:
转化率几乎为0,结合离子方程式解释原因:②图2中,
 与
与 物质的量之比从0.5﹕1提高至1﹕1时,
物质的量之比从0.5﹕1提高至1﹕1时, 的转化率明显增大,可能的原因是
的转化率明显增大,可能的原因是
您最近一年使用:0次
2021-11-04更新
|
202次组卷
|
4卷引用:北京市第一六一中学2023-2024学年高三上学期10月月考化学试题
名校
解题方法
4 . 某学习小组按如下实验流程探究海带中碘含量的测定和碘的提取。
Ⅰ.碘含量的测定

(1)灼烧海带实验用到的主要的含硅酸盐的仪器有酒精灯、玻璃棒、___________ 、___________ 等。
(2)仪器A的名称为:___________ 。
(3)碘浓度还可用色度计测定吸光度,吸光度越大碘浓度越大。用色度计测得某碘溶液的吸光度后,利用以溶液吸光度为纵坐标、碘浓度(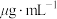 )为横坐标的标准曲线图,可以得出被测溶液碘浓度。为了绘制标准曲线图,取0.10g碘单质,用100mL容量瓶配成碘的
)为横坐标的标准曲线图,可以得出被测溶液碘浓度。为了绘制标准曲线图,取0.10g碘单质,用100mL容量瓶配成碘的 溶液,再从中取出0.10mL加入
溶液,再从中取出0.10mL加入 中配得第一份4.00mL碘的
中配得第一份4.00mL碘的 标准溶液。用色度计测其吸光度,得到标准曲线的第一个坐标点,该坐标点的横坐标是
标准溶液。用色度计测其吸光度,得到标准曲线的第一个坐标点,该坐标点的横坐标是___________ 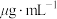 。(注:
。(注: )
)
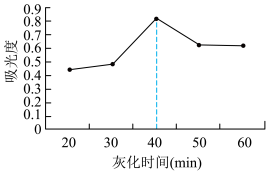
(4)课题组在其他实验条件相同情况下,研究了不同灰化时间(干海带灼烧成灰的时间)对碘提取效果的影响。其结果如图所示。灰化时间超过40min,测得碘的含量逐渐降低,原因是___________ 。
Ⅱ.碘的提取
某同学另取海带原液设计如下实验方案提取碘:
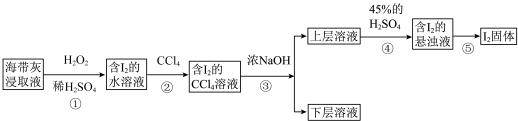
步骤③的离子反应方程式为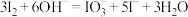
(5)步骤①中发生反应的离子方程式为___________ 。
(6)向含有 的水溶液中加入
的水溶液中加入 振荡静置后的实验现象为
振荡静置后的实验现象为___________ 。
(7)步骤④发生反应的离子方程式为___________ 。
Ⅰ.碘含量的测定

(1)灼烧海带实验用到的主要的含硅酸盐的仪器有酒精灯、玻璃棒、
(2)仪器A的名称为:
(3)碘浓度还可用色度计测定吸光度,吸光度越大碘浓度越大。用色度计测得某碘溶液的吸光度后,利用以溶液吸光度为纵坐标、碘浓度(
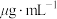 )为横坐标的标准曲线图,可以得出被测溶液碘浓度。为了绘制标准曲线图,取0.10g碘单质,用100mL容量瓶配成碘的
)为横坐标的标准曲线图,可以得出被测溶液碘浓度。为了绘制标准曲线图,取0.10g碘单质,用100mL容量瓶配成碘的 溶液,再从中取出0.10mL加入
溶液,再从中取出0.10mL加入 中配得第一份4.00mL碘的
中配得第一份4.00mL碘的 标准溶液。用色度计测其吸光度,得到标准曲线的第一个坐标点,该坐标点的横坐标是
标准溶液。用色度计测其吸光度,得到标准曲线的第一个坐标点,该坐标点的横坐标是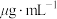 。(注:
。(注: )
)(4)课题组在其他实验条件相同情况下,研究了不同灰化时间(干海带灼烧成灰的时间)对碘提取效果的影响。其结果如图所示。灰化时间超过40min,测得碘的含量逐渐降低,原因是

Ⅱ.碘的提取
某同学另取海带原液设计如下实验方案提取碘:

步骤③的离子反应方程式为
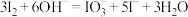
(5)步骤①中发生反应的离子方程式为
(6)向含有
 的水溶液中加入
的水溶液中加入 振荡静置后的实验现象为
振荡静置后的实验现象为(7)步骤④发生反应的离子方程式为
您最近一年使用:0次
名校
解题方法
5 . 海水是一个巨大的化学资源宝库。请回答下列问题:
Ⅰ.从海带中提取碘单质
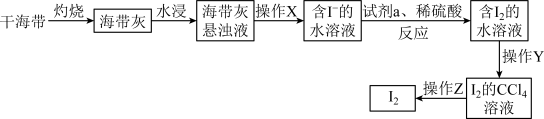
(1)“灼烧”过程需要用到的仪器为酒精灯、三脚架、泥三角、_____ ,“操作X”的名称为_____ 。
(2)若试剂 选择
选择 ,试剂
,试剂 参与反应的离子方程式为
参与反应的离子方程式为_____ ,氧化性:
_____ (填“>”或“<”) 。
。
(3)“操作Y”为萃取分液,萃取后分液时,转移 的
的 溶液至烧杯中的操作是
溶液至烧杯中的操作是_____ 。
Ⅱ.海水提溴:海水→海水淡化→ 氧化→空气吹出→吸收→……→液溴
氧化→空气吹出→吸收→……→液溴
(4)“空气吹出”体现了溴的_____ 性,该步骤的目的是_____ 。
(5)若“吸收”步骤使用浓的 溶液,则反应后产物有
溶液,则反应后产物有 、
、 ,该过程发生反应的离子方程式为
,该过程发生反应的离子方程式为_____ 。若反应后得到 、
、 、
、 的混合溶液,经测定,
的混合溶液,经测定,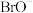 与
与 的物质的量之比为
的物质的量之比为 ,则
,则 与
与 反应时,被还原的溴元素和被氧化的溴元素的物质的量之比
反应时,被还原的溴元素和被氧化的溴元素的物质的量之比_____ 。
Ⅰ.从海带中提取碘单质

(1)“灼烧”过程需要用到的仪器为酒精灯、三脚架、泥三角、
(2)若试剂
 选择
选择 ,试剂
,试剂 参与反应的离子方程式为
参与反应的离子方程式为
 。
。(3)“操作Y”为萃取分液,萃取后分液时,转移
 的
的 溶液至烧杯中的操作是
溶液至烧杯中的操作是Ⅱ.海水提溴:海水→海水淡化→
 氧化→空气吹出→吸收→……→液溴
氧化→空气吹出→吸收→……→液溴(4)“空气吹出”体现了溴的
(5)若“吸收”步骤使用浓的
 溶液,则反应后产物有
溶液,则反应后产物有 、
、 ,该过程发生反应的离子方程式为
,该过程发生反应的离子方程式为 、
、 、
、 的混合溶液,经测定,
的混合溶液,经测定,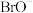 与
与 的物质的量之比为
的物质的量之比为 ,则
,则 与
与 反应时,被还原的溴元素和被氧化的溴元素的物质的量之比
反应时,被还原的溴元素和被氧化的溴元素的物质的量之比
您最近一年使用:0次
名校
6 . I.海洋是生命的摇篮,浩瀚的海洋中蕴藏着丰富的资源。人们可以从海水中提取淡水和制得镁、溴等重要的化工产品。
(1)从海水中获得淡水的主要方法有蒸馏法、离子交换法和___________ 。离子交换法净化水的过程如图所示。下列说法正确的是___________ (填序号)。
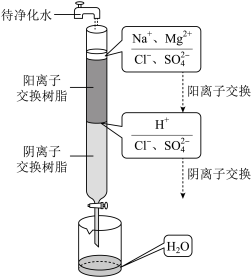
A.经过阳离子交换树脂后,水中阳离子总数
B.通过阴离子交换树脂后,水中只有 被除去
被除去
C.通过净化处理后的水,导电性增强
D.阴离子交换树脂填充段存在反应:
(2)工业上通过 制备Mg,常用的冶炼方法是
制备Mg,常用的冶炼方法是___________ 。制备溴时通入热空气可以吹出溴,是利用了溴的___________ 。
Ⅱ.海带中含有碘元素。从海带中提取碘的实验过程如下图所示:
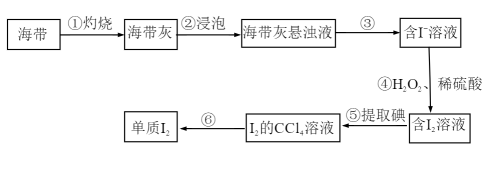
(3)实验步骤①不会用到下列仪器中的___________ (填字母)
a.泥三角 b.250ml容量瓶 c.坩埚 d.漏斗 e.酒精灯
(4)步骤③的操作名称是___________
(5)步骤④中反应的离子方程式为___________
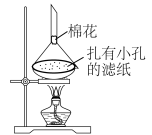
(6)利用如图装置,可以从氯化钠固体中分离出碘单质。简述原理________ ;棉花的作用是________ 。
(1)从海水中获得淡水的主要方法有蒸馏法、离子交换法和

A.经过阳离子交换树脂后,水中阳离子总数
B.通过阴离子交换树脂后,水中只有
 被除去
被除去C.通过净化处理后的水,导电性增强
D.阴离子交换树脂填充段存在反应:

(2)工业上通过
 制备Mg,常用的冶炼方法是
制备Mg,常用的冶炼方法是Ⅱ.海带中含有碘元素。从海带中提取碘的实验过程如下图所示:

(3)实验步骤①不会用到下列仪器中的
a.泥三角 b.250ml容量瓶 c.坩埚 d.漏斗 e.酒精灯
(4)步骤③的操作名称是
(5)步骤④中反应的离子方程式为
(6)利用如图装置,可以从氯化钠固体中分离出碘单质。简述原理

您最近一年使用:0次
7 . 海水是资源的宝库,是目前溴和碘的主要来源,请根据海水提溴和海带提碘的流程,回答下列问题:
(一)海水提溴
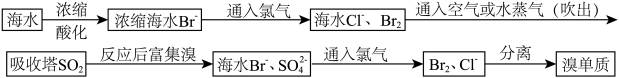
(1)热空气或者水蒸气吹出海水中的溴,说明溴具有___________ 性;
(2) 在流程中的作用说明氯的非金属性比溴
在流程中的作用说明氯的非金属性比溴___________ ,请列举另一种能说明氯和溴的非金属性强弱的性质___________ :
(3) 水溶液吸收溴的反应方程式为
水溶液吸收溴的反应方程式为___________ ;
(二)海带提碘
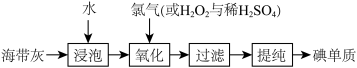
(4)将海带灼烧成灰的目的是___________ (至少答一点):
(5)请从环保的角度,说明用 代替氯气的优点
代替氯气的优点___________ :
(6)某电视台曾播出用土豆片检验食盐中的碘的节目,后被证实为伪科学,请结合所学知识简要说明土豆片不能检验出食盐中含碘的原因___________ 。
(一)海水提溴

(1)热空气或者水蒸气吹出海水中的溴,说明溴具有
(2)
 在流程中的作用说明氯的非金属性比溴
在流程中的作用说明氯的非金属性比溴(3)
 水溶液吸收溴的反应方程式为
水溶液吸收溴的反应方程式为(二)海带提碘

(4)将海带灼烧成灰的目的是
(5)请从环保的角度,说明用
 代替氯气的优点
代替氯气的优点(6)某电视台曾播出用土豆片检验食盐中的碘的节目,后被证实为伪科学,请结合所学知识简要说明土豆片不能检验出食盐中含碘的原因
您最近一年使用:0次
解题方法
8 . 食品添加剂的常见类别有:着色剂、增味剂、膨松剂、凝固剂、防腐剂、营养强化剂等。
(1)碘酸钾为___________ (填食品添加剂的类别)。
(2)从海带中提取碘的主要实验过程如下图所示:

①干海带的“灼烧”需在___________ (填仪器名称)中进行。
②操作1为___________ (填操作名称)。
③在“氧化”步骤中,最符合绿色化学思想的氧化剂是下列物质中的___________ (填选项字母),酸性条件下该反应的离子方程式为___________ 。
A. 溶液 B.浓硝酸 C.
溶液 B.浓硝酸 C.
④检验操作2后水层中是否含有碘单质的方法为___________ 。
(3)在加热条件下,将 通入到
通入到 和
和 的混合溶液中制备
的混合溶液中制备 ,该反应的化学方程式为
,该反应的化学方程式为___________ ;若要制备500g的加碘食盐(碘含量为2.54%),至少需要
___________ g。
(1)碘酸钾为
(2)从海带中提取碘的主要实验过程如下图所示:

①干海带的“灼烧”需在
②操作1为
③在“氧化”步骤中,最符合绿色化学思想的氧化剂是下列物质中的
A.
 溶液 B.浓硝酸 C.
溶液 B.浓硝酸 C.
④检验操作2后水层中是否含有碘单质的方法为
(3)在加热条件下,将
 通入到
通入到 和
和 的混合溶液中制备
的混合溶液中制备 ,该反应的化学方程式为
,该反应的化学方程式为
您最近一年使用:0次
解题方法
9 . 碘和碘的化合物在有机化学中十分重要,另外在医药和照相方面的用途也很广泛。海带提碘的相关流程如下所示,已知 ,请回答下列问题:
,请回答下列问题:
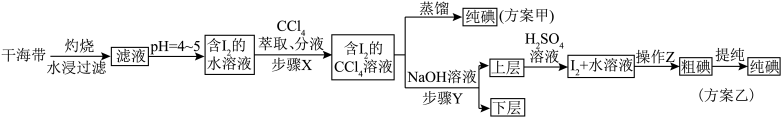
(1)海带灼烧的目的是_______ ;实验室进行此操作用到的主要仪器名称为_______ 。
(2)滤液得到含 的水溶液,除了调节
的水溶液,除了调节 ,还需要加入臭氧或过氧化氢,所加试剂在反应中作
,还需要加入臭氧或过氧化氢,所加试剂在反应中作_______ 剂(填“氧化”或“还原”),写出加入过氧化氢时发生反应的离子方程式:_______ 。
(3)步骤 是否可以用酒精代替
是否可以用酒精代替 ,并说明理由
,并说明理由_______ 。
(4)步骤 的操作为
的操作为_______ 。
(5)上层液体加入 溶液后发生反应的离子方程式为
溶液后发生反应的离子方程式为_______ 。
(6)以上流程中可以循环使用的试剂是_______ 。
(7)加碘食盐中的碘以碘酸钾 形式存在,根据以上信息,可用试纸和一些常见试剂进行检验,证明食盐中存在
形式存在,根据以上信息,可用试纸和一些常见试剂进行检验,证明食盐中存在 。可供选用的物质有:①
。可供选用的物质有:① 试纸、②蓝色石蕊试纸、③碘化钾淀粉试纸、④蒸馏水、⑤食醋、⑥醇,进行上述实验时必须使用的物质是
试纸、②蓝色石蕊试纸、③碘化钾淀粉试纸、④蒸馏水、⑤食醋、⑥醇,进行上述实验时必须使用的物质是_______ (填序号)。
 ,请回答下列问题:
,请回答下列问题:
(1)海带灼烧的目的是
(2)滤液得到含
 的水溶液,除了调节
的水溶液,除了调节 ,还需要加入臭氧或过氧化氢,所加试剂在反应中作
,还需要加入臭氧或过氧化氢,所加试剂在反应中作(3)步骤
 是否可以用酒精代替
是否可以用酒精代替 ,并说明理由
,并说明理由(4)步骤
 的操作为
的操作为(5)上层液体加入
 溶液后发生反应的离子方程式为
溶液后发生反应的离子方程式为(6)以上流程中可以循环使用的试剂是
(7)加碘食盐中的碘以碘酸钾
 形式存在,根据以上信息,可用试纸和一些常见试剂进行检验,证明食盐中存在
形式存在,根据以上信息,可用试纸和一些常见试剂进行检验,证明食盐中存在 。可供选用的物质有:①
。可供选用的物质有:① 试纸、②蓝色石蕊试纸、③碘化钾淀粉试纸、④蒸馏水、⑤食醋、⑥醇,进行上述实验时必须使用的物质是
试纸、②蓝色石蕊试纸、③碘化钾淀粉试纸、④蒸馏水、⑤食醋、⑥醇,进行上述实验时必须使用的物质是
您最近一年使用:0次
名校
解题方法
10 . 海洋资源的利用具有非常广阔的前景,从海水中可提取多种化工原料。
Ⅰ.如图是从海水中提取镁的简单流程,回答下列问题:

(1)工业上常用于沉淀 的试剂A是
的试剂A是___________ ,操作A的名称是___________ 。
(2)由无水 制取Mg的化学方程式是
制取Mg的化学方程式是___________ 。
Ⅱ.海水中Br含量为 ,工业上常用“吹出法”从海水中提溴,工艺流程示意图如图,回答下列问题:
,工业上常用“吹出法”从海水中提溴,工艺流程示意图如图,回答下列问题:
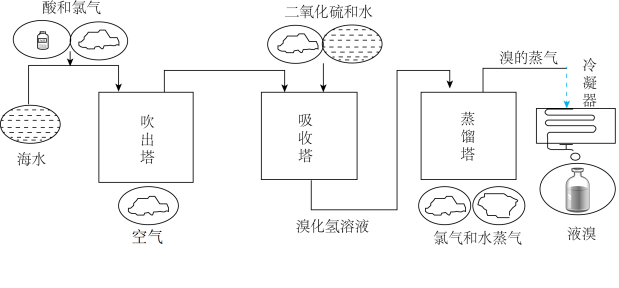
(3)鼓入热空气将生成的溴吹出,利用了 的
的___________ 性。
(4)吸收塔中 的吸收率可达95%,吸收塔中主要反应的方程式是
的吸收率可达95%,吸收塔中主要反应的方程式是 。也有工艺是在吹出
。也有工艺是在吹出 后用碳酸钠溶液吸收,生成溴化钠和溴酸钠,该反应的离子方程式是
后用碳酸钠溶液吸收,生成溴化钠和溴酸钠,该反应的离子方程式是___________ 。
Ⅲ.海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计如下实验:

(5)步骤①中灼烧海带时,应将海带放入___________ (填仪器名称)中灼烧。
(6)步骤④发生的离子反应方程式为___________ 。
(7)实验室常用碘量法测定溶液中 的含量。取200mL样品,加入
的含量。取200mL样品,加入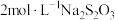 溶液,发生反应
溶液,发生反应 ,充分反应后,消耗
,充分反应后,消耗 溶液100mL。则该样品中
溶液100mL。则该样品中 的含量是
的含量是___________  。
。
Ⅰ.如图是从海水中提取镁的简单流程,回答下列问题:

(1)工业上常用于沉淀
 的试剂A是
的试剂A是(2)由无水
 制取Mg的化学方程式是
制取Mg的化学方程式是Ⅱ.海水中Br含量为
 ,工业上常用“吹出法”从海水中提溴,工艺流程示意图如图,回答下列问题:
,工业上常用“吹出法”从海水中提溴,工艺流程示意图如图,回答下列问题:
(3)鼓入热空气将生成的溴吹出,利用了
 的
的(4)吸收塔中
 的吸收率可达95%,吸收塔中主要反应的方程式是
的吸收率可达95%,吸收塔中主要反应的方程式是 。也有工艺是在吹出
。也有工艺是在吹出 后用碳酸钠溶液吸收,生成溴化钠和溴酸钠,该反应的离子方程式是
后用碳酸钠溶液吸收,生成溴化钠和溴酸钠,该反应的离子方程式是Ⅲ.海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计如下实验:

(5)步骤①中灼烧海带时,应将海带放入
(6)步骤④发生的离子反应方程式为
(7)实验室常用碘量法测定溶液中
 的含量。取200mL样品,加入
的含量。取200mL样品,加入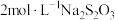 溶液,发生反应
溶液,发生反应 ,充分反应后,消耗
,充分反应后,消耗 溶液100mL。则该样品中
溶液100mL。则该样品中 的含量是
的含量是 。
。
您最近一年使用:0次



