名校
1 . 海带中含有较多的碘元素,某化学兴趣小组通过以下步骤提取海带中的碘:
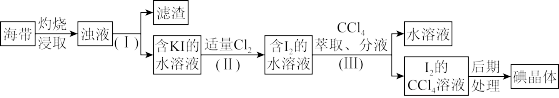
(1)步骤(Ⅰ)中分离操作的名称是_______ ,该操作中用到的玻璃仪器有漏斗、烧杯和_______ 。
(2)写出步骤(Ⅱ)中KI和Cl2反应的离子方程式_______ ,取少量反应后的溶液滴入淀粉试液,溶液呈_______ 色;
(3)步骤(Ⅲ)中萃取后分层, 的
的 溶液在
溶液在_______ (填“上层”或“下层”)。
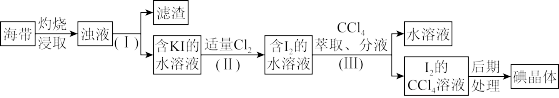
(1)步骤(Ⅰ)中分离操作的名称是
(2)写出步骤(Ⅱ)中KI和Cl2反应的离子方程式
(3)步骤(Ⅲ)中萃取后分层,
 的
的 溶液在
溶液在
您最近一年使用:0次
2022-04-20更新
|
117次组卷
|
2卷引用:福建省莆田第二十五中学2022-2023学年高一下学期期中考试化学试题
2 . 溴、碘主要存在于海水中,有“海洋元素”的美称。从海带中提取碘单质,工艺流程如下图。
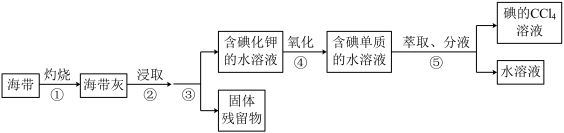
下列操作错误的是

下列操作错误的是
| A | B | C | D |
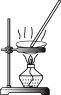 | 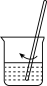 | 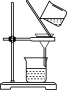 | 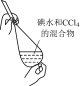 |
| 步骤①操作 | 步骤②操作 | 步骤③操作 | 步骤⑤中振荡萃取操作 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . Ⅰ.将海水淡化与浓海水资源化结合起来是综合利用海水的重要途径之一,一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺流程提取其他产品。回答下问题:
(1)请列举一种海水淡化的方法:_______ 。
(2)海水提溴中将Br2从苦卤中吹出,利用了Br2的_______ 性。
Ⅱ.通过传统的海带提碘工艺提取单质碘后,其所得废水中尚残留部分的I2,可用活性炭吸附法加以回收利用。具体流程如图:
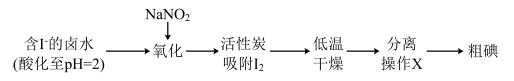
已知:i.pH=2时,NaNO2溶液只能将I-氧化为I2,同时生成NO
ii.将湿润的淀粉-KI试纸伸入盛满氯气的集气瓶中,试纸先变蓝,后褪色
(3)写出氧化含I-的卤水中发生的离子方程式:________ 。
(4)在分离操作X的装置如图所示,电加热器的作用是________ ,得到I2的位置位于该装置中________ 处(填图中选项)。

(5)已知Cl2的氧化性强于NaNO2,但该方法中却选择了价格较高的NaNO2,原因是_______ 。
(6)某工厂排出的废水,经测定含0.012mol/L的游离I2和8×10-4mol/L的H+,若改用加Na2SO3的方法除去I2,发生的化学反应为:Na2SO3+I2+H2O=Na2SO4+2HI,该反应中氧化产物与还原产物的物质的量之比为_______ ,现需处理5L该废水,则需加入0.05mol/L的Na2SO3溶液_______ L才能把I2除尽。
(1)请列举一种海水淡化的方法:
(2)海水提溴中将Br2从苦卤中吹出,利用了Br2的
Ⅱ.通过传统的海带提碘工艺提取单质碘后,其所得废水中尚残留部分的I2,可用活性炭吸附法加以回收利用。具体流程如图:

已知:i.pH=2时,NaNO2溶液只能将I-氧化为I2,同时生成NO
ii.将湿润的淀粉-KI试纸伸入盛满氯气的集气瓶中,试纸先变蓝,后褪色
(3)写出氧化含I-的卤水中发生的离子方程式:
(4)在分离操作X的装置如图所示,电加热器的作用是

(5)已知Cl2的氧化性强于NaNO2,但该方法中却选择了价格较高的NaNO2,原因是
(6)某工厂排出的废水,经测定含0.012mol/L的游离I2和8×10-4mol/L的H+,若改用加Na2SO3的方法除去I2,发生的化学反应为:Na2SO3+I2+H2O=Na2SO4+2HI,该反应中氧化产物与还原产物的物质的量之比为
您最近一年使用:0次
解题方法
4 . 某校研究性学习小组在实验室模拟从海带中提取碘的实验,实验流程如图所示。
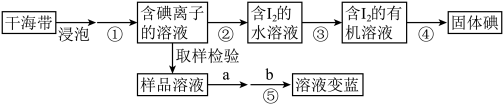
(1)请分别为步骤①和步骤③选择合适的实验操作:①___________ ,③___________ (填字母)
a.溶解 b.过滤 c.萃取 d.分液 e.蒸馏
(2)工业上步骤②多在酸性条件下用NaNO2进行氧化,反应中生成一种无色气体,遇空气立即变为红棕色,请写出该步骤中发生反应的离子方程式是___________ 。
(3)已知步骤③可以用有机物“石油醚”达到目的,根据流程可推测石油醚具有以下哪些性质___________ (填字母)。
a.不溶于水 b.不与水反应
c.石油醚的密度小于水 d.I2在石油醚中的溶解度大于水
(4)步骤④中,为了将I2从有机溶剂中提取出来,某小组成员向含I2的有机溶液中加入浓NaOH溶液,振荡、静置、分液,取水层用45%的硫酸酸化,得到含I2的悬浊液,再过滤获得固体碘(已知:3I2+6NaOH=5NaI+NaIO3+3H2O)。其中分液操作中需要用到的玻璃仪器有___________ (填仪器名称),加入45%的硫酸溶液发生反应的离子方程式为:___________ 。
(5)步骤⑤取样检验样品中的碘离子时,可用适量氯水检验,则应选用___________ (填物质名称)作指示剂。

(1)请分别为步骤①和步骤③选择合适的实验操作:①
a.溶解 b.过滤 c.萃取 d.分液 e.蒸馏
(2)工业上步骤②多在酸性条件下用NaNO2进行氧化,反应中生成一种无色气体,遇空气立即变为红棕色,请写出该步骤中发生反应的离子方程式是
(3)已知步骤③可以用有机物“石油醚”达到目的,根据流程可推测石油醚具有以下哪些性质
a.不溶于水 b.不与水反应
c.石油醚的密度小于水 d.I2在石油醚中的溶解度大于水
(4)步骤④中,为了将I2从有机溶剂中提取出来,某小组成员向含I2的有机溶液中加入浓NaOH溶液,振荡、静置、分液,取水层用45%的硫酸酸化,得到含I2的悬浊液,再过滤获得固体碘(已知:3I2+6NaOH=5NaI+NaIO3+3H2O)。其中分液操作中需要用到的玻璃仪器有
(5)步骤⑤取样检验样品中的碘离子时,可用适量氯水检验,则应选用
您最近一年使用:0次
名校
解题方法
5 . 以海带为原料提取碘单质的流程如下:
(1)为提高“水浸”速率,宜采取的措施有:_____________ (任写两种);“氧化1”中 ,不宜过量的原因是
,不宜过量的原因是_____ 。
(2)“过滤”操作需要的玻璃仪器有______ (填仪器名称)。
(3)“吸附”的目的是______ 。
(4)“解吸”中氧化剂、还原剂的物质的量之比为______ 。
(5)“氧化2”中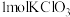 完全反应转移
完全反应转移 电子。与出该反应的离子方程式:
电子。与出该反应的离子方程式:______ 。
(6)利用如图装置提纯碘。
提纯 的原理是
的原理是______ ,棉花防止碘扩散到空气中造成污染。
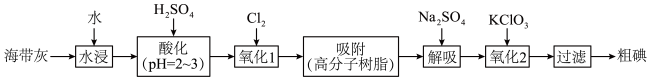
(1)为提高“水浸”速率,宜采取的措施有:
 ,不宜过量的原因是
,不宜过量的原因是(2)“过滤”操作需要的玻璃仪器有
(3)“吸附”的目的是
(4)“解吸”中氧化剂、还原剂的物质的量之比为
(5)“氧化2”中
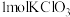 完全反应转移
完全反应转移 电子。与出该反应的离子方程式:
电子。与出该反应的离子方程式:(6)利用如图装置提纯碘。
提纯
 的原理是
的原理是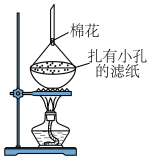
您最近一年使用:0次
2024-01-24更新
|
85次组卷
|
3卷引用:云南省楚雄东兴中学2023-2024学年高三上学期12月月考理综试题
解题方法
6 . 球上99%的溴存在于海水中,故溴也被称为海洋元素,溴主要用于制造汽油抗爆剂、药品、试剂和农药等。以海水提盐后得到的苦卤为原料,提取溴的流程如图所示。
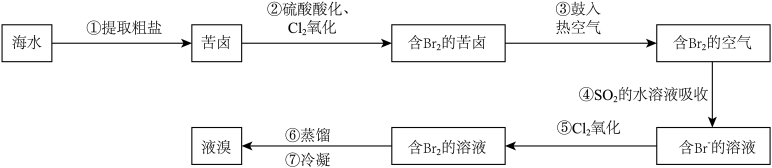
已知:Br2+SO2+2H2O= H2SO4+2HBr。
(1)苦卤可用作提取溴的原料的原因是:_______ 。
(2)写出步骤②中通入Cl2反应的离子方程式:_______ 。
(3)步骤③用热空气将溴吹出制成粗溴,是因为_______(填编号)。
(4)步骤④将Br2转化为Br-,是利用了SO2的_______ 性。
(5)设计一个简单实验,说明溴的活动性大于碘单质:_______ 。

已知:Br2+SO2+2H2O= H2SO4+2HBr。
(1)苦卤可用作提取溴的原料的原因是:
(2)写出步骤②中通入Cl2反应的离子方程式:
(3)步骤③用热空气将溴吹出制成粗溴,是因为_______(填编号)。
| A.Br2的化学性质稳定 | B.Br2沸点低,易挥发 |
| C.Br2易升华 | D.Br2不溶于水 |
(5)设计一个简单实验,说明溴的活动性大于碘单质:
您最近一年使用:0次
7 . 海洋中蕴含丰富的资源。
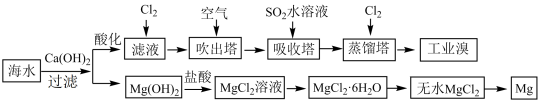
I.利用海水提取淡水、溴、镁和碘的部分过程如图所示:
(1)海水中部分离子的含量如下:
其中,Mg2+的物质的量浓度是_______ mol/L。海水淡化的方法有_______ 、离子交换法和电渗析法等。
(2)滤液中通入Cl2后发生反应的离子方程式为_______
(3)提取溴元素时,热空气吹出并用SO2水溶液吸收的目的是_______ ,然后再通入Cl2。
(4)若要提取1mol溴,理论上至少需要标准状况下Cl2的体积为_______ L(忽略Cl2的溶解)。
(5)由无水MgCl2制取Mg的化学方程式为_______ 。
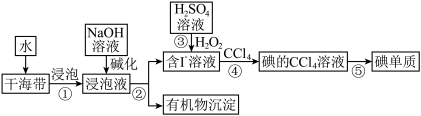
II.海带中含有丰富的碘元素。从海带中提取碘单质的工业生产流程如图所示:
(6)步骤②的操作是_______
(7)步骤③反应的离子方程式有H++OH-=H2O和_______ 。
(8)步骤④还可以选用的试剂是_______ (填字母序号)。
A.苯 B.乙醇 C.己烷 D.乙酸
I.利用海水提取淡水、溴、镁和碘的部分过程如图所示:

(1)海水中部分离子的含量如下:
| 成分 | 含量(mg/L) | 成分 | 含量(mg/L) |
| Na+ | 10560 | Cl- | 18980 |
| Mg2+ | 1272 | Br- | 64 |
| Ca2+ | 400 |  | 2560 |
(2)滤液中通入Cl2后发生反应的离子方程式为
(3)提取溴元素时,热空气吹出并用SO2水溶液吸收的目的是
(4)若要提取1mol溴,理论上至少需要标准状况下Cl2的体积为
(5)由无水MgCl2制取Mg的化学方程式为
II.海带中含有丰富的碘元素。从海带中提取碘单质的工业生产流程如图所示:

(6)步骤②的操作是
(7)步骤③反应的离子方程式有H++OH-=H2O和
(8)步骤④还可以选用的试剂是
A.苯 B.乙醇 C.己烷 D.乙酸
您最近一年使用:0次
名校
解题方法
8 . 从海带中提取碘的实验过程主要包括:灼烧、浸取、过滤、氧化、萃取、蒸馏等步骤。下列说法错误的是
| A.“灼烧”时,可用酒精灯直接加热坩埚 |
| B.“过滤”时,为加快过滤速率,要用玻璃棒不断搅动漏斗中的液体 |
| C.“氧化”时,可选用H2O2作氧化剂 |
| D.“萃取”时,若用CCl4作萃取剂,则有机层从分液漏斗下方流出 |
您最近一年使用:0次
2023-11-03更新
|
81次组卷
|
2卷引用:河南省普高联考2023-2024学年高三上学期测评(三)化学试题
名校
9 . 碘元素是人体中重要的微量元素之一,被称为“智力元素”。实验室从海带中提取碘单质的操作流程如图所示。下列说法正确的是


| A.步骤①的操作名称是研磨 |
| B.步骤③中玻璃棒的作用是搅拌 |
C.步骤④中理论上每生成 ,需消耗 ,需消耗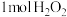 |
D.步骤⑤可以选用 或乙醇 或乙醇 |
您最近一年使用:0次
2023-07-09更新
|
207次组卷
|
2卷引用:广东省肇庆市2022-2023学年高一下学期期末教学质量检测化学试题
10 . 海带中含有碘元素,从海带中提取碘的实验过程如下所示。
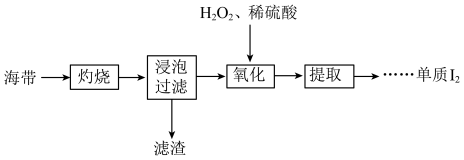
(1)“灼烧”时用到下列仪器中的___________。
(2)“浸泡过滤”后滤液中含有I-,“氧化”的离子方程式为___________ 。
(3)检验“氧化”产生I2的操作:取“氧化”后的少量溶液于试管中,___________ (实验操作及现象)。
(4)“提取”存在以下两种方案。
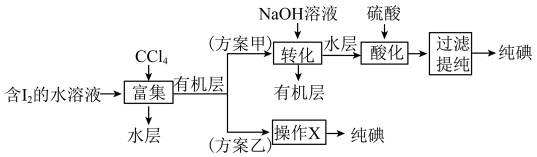
已知: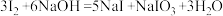 ;酸性条件下,I2在水溶液中的溶解度很小。
;酸性条件下,I2在水溶液中的溶解度很小。
①方案乙中“操作X”的名称是___________ 。
②方案甲中,“酸化”步骤氧化剂与还原剂物质的量之比为___________ 。
③该流程可循环利用的物质是___________ 。
④采用方案乙得到纯碘的产率较低,原因是___________ 。

(1)“灼烧”时用到下列仪器中的___________。
| A.酒精灯 | B.漏斗 | C.蒸发皿 | D.坩埚 |
(3)检验“氧化”产生I2的操作:取“氧化”后的少量溶液于试管中,
(4)“提取”存在以下两种方案。

已知:
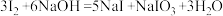 ;酸性条件下,I2在水溶液中的溶解度很小。
;酸性条件下,I2在水溶液中的溶解度很小。①方案乙中“操作X”的名称是
②方案甲中,“酸化”步骤氧化剂与还原剂物质的量之比为
③该流程可循环利用的物质是
④采用方案乙得到纯碘的产率较低,原因是
您最近一年使用:0次



