陕西省西安市蓝田县2019届高三上学期第一次模拟考试理科综合化学试题
陕西
高三
一模
2019-03-02
581次
整体难度:
适中
考查范围:
认识化学科学、有机化学基础、化学与STSE、常见无机物及其应用、物质结构与性质、化学实验基础、化学反应原理
陕西省西安市蓝田县2019届高三上学期第一次模拟考试理科综合化学试题
陕西
高三
一模
2019-03-02
581次
整体难度:
适中
考查范围:
认识化学科学、有机化学基础、化学与STSE、常见无机物及其应用、物质结构与性质、化学实验基础、化学反应原理
一、单选题 添加题型下试题
单选题
|
适中(0.65)
解题方法
1. 化学与生活息息相关,下列有关说法不正确的是
| A.我国发射“嫦娥三号”卫星所使用的碳纤维是一种非金属材料 |
| B.食用油的主要成分是油脂,其成分与汽油、煤油不相同 |
| C.《本草拾遗》记载“醋……消食,杀恶毒……,其中醋的有效成分是乙酸 |
| D.PM2.5是指大气中直径接近2.5×10-6m的颗粒物,颗粒物分散在空气中形成胶体 |
您最近一年使用:0次
单选题
|
适中(0.65)
2. 环之间共用一个碳原子的化合物称为螺环化合物,螺[2,2]戊烷( )是最简单的一种。下列关于该化合物的说法正确的是
)是最简单的一种。下列关于该化合物的说法正确的是
 )是最简单的一种。下列关于该化合物的说法正确的是
)是最简单的一种。下列关于该化合物的说法正确的是| A.与环戊烯不是同分异构体 | B.二氯代物超过两种 |
| C.生成1molC5H12,至少需要3molH2 | D.与丙炔互为同系物 |
【知识点】 同系物的判断解读 同分异构现象 同分异构体的数目的确定解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
3. 设NA为阿伏伽德罗常数的值,下列说法中正确的是
| A.0.2mol FeI2与足量氯气反应时转移电子数为0.4NA |
| B.常温常压下,46g NO2和N2O4混合气体含有的原子数为3NA |
| C.标准状况下,2.24LCCl4含有的共价键数为0.4NA |
| D.常温下,56g铁片投入足量浓H2SO4中生成NA个SO2分子 |
您最近一年使用:0次
2019-02-26更新
|
907次组卷
|
4卷引用:陕西省西安市蓝田县2019届高三上学期第一次模拟考试理科综合化学试题
单选题
|
适中(0.65)
名校
4. X、Y、Z、W、M五种元素的原子序数依次增大。已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子;Y 原子的最外层电子数是内层电子数的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M是地壳中含量最高的金属元素。下列说法正确的是
| A.X、Z、W三元素所形成的化合物一定为共价化合 物 |
| B.原子半径:r(M)>r(Y) >r(Z) >r(W) >r(X) |
| C.W和M形成的化合物不能与强碱反应 |
| D.Y、Z的最高价含氧酸的酸性:Y>Z |
您最近一年使用:0次
2019-05-28更新
|
236次组卷
|
6卷引用:陕西省西安市蓝田县2019届高三上学期第一次模拟考试理科综合化学试题
单选题
|
适中(0.65)
5. 根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向FeCl3饱和溶液中滴入足量浓氨水,并加热至沸 | 生成红褐色透明液体 | 得到Fe(OH)3胶体 |
| B | 向KI溶液中加入淀粉,然后加入稀硫酸搅拌 | 开始无明显现象,片刻溶液变蓝 | 氧化性H2SO4 >I2 |
| C | 将浸透石蜡油的石棉网放置在硬质试管底部,加入少量碎瓷片并加热,将生成的气体通入酸性高锰酸钾溶液中。 | 高锰酸钾溶液褪色 | 石蜡油分解产物中生成不饱和烃 |
| D | 向待测液中加入适量的稀NaOH溶液,将湿润的蓝色石蕊试纸放在试管口 | 湿润的蓝色石蕊试纸未变红 | 待测液中不含有NH4+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
6. 某新型水系钠离子电池工作原理如图所示。TiO2光电极能使电池在太阳光照下充电,充电时Na2S4还原为Na2S,下列说法不正确的是


| A.充电时,太阳能转化为电能,电能又转化为化学能 |
| B.放电时,a极为负极 |
| C.充电时,阳极的电极反应式为3I――2e-=13- |
| D.M是阴离子交换膜 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
7. 常温下,向10.0mL0.10mol·L-1某二元酸H2R溶液中滴入同物质的量浓度的NaOH溶液,测得溶液的pH随NaOH溶液体积的变化如图所示。下列说法中正确的是


| A.HR-的电离能力大于水解能力 |
| B.曲线上m点时溶液中c(Na+)>c(HR-)>c(R2-)>c(H+) |
| C.无法判断H2R是强酸还是弱酸 |
| D.溶液中c(Na+)+c(H+)=c(HR-)+c(R2-)+c(OH-) |
您最近一年使用:0次
2019-02-26更新
|
305次组卷
|
6卷引用:【全国百强校】甘肃省西北师范大学附属中学2018届高三冲刺诊断考试理综化学试题
二、解答题 添加题型下试题
解答题-工业流程题
|
适中(0.65)
名校
解题方法
8. 铍铜是力学、化学综合性能良好的合金,广泛应用于制造高级弹性元件。以下是从某废旧铍铜元件(含BeO 、CuS、少量FeS 和SiO2)中回收铍和铜两种金属的流程。

已知:Ⅰ.铍、铝元素处于周期表中的对角线位置,化学性质相似
Ⅱ.常温下: Ksp[Cu(OH)2]、=2.2×10-20、Ksp[Fe(OH)3]=4.0×10-38、Ksp[Mn(OH)2]=2.l×10-13
(1)写出铍铜元件中SiO2与NaOH溶液反应的离子方程式______________________ 。
(2)滤渣B的主要成分为___________________ ( 填化学式)。写出反应Ⅰ中含铍化合物与过量盐酸反应的化学方程式___________________________________________ 。
(3)①溶液C中含NaCl、BeCl2和少量HCl,为提纯BeCl2,选择合理步骤并排序________ 。
a.加入过量的NaOH b.过滤 c.加入适量的HCl
d.加入过量的氨水 e.通入过量的CO2 f.洗涤
②从BeCl2溶液中得到BeCl2 固体的操作是___________________________________ 。
(4)MnO2 能将金属硫化物中的硫元素氧化为单质硫,写出反应Ⅱ中CuS 发生反应的离子方程式________________________________ 。
(5)溶液D 中含c(Cu2+)=2.2 mol·L-1、c( Fe3+)=0.008 mol·L-1、c( Mn2+)=0.01mol·L-1,逐滴加入稀氨水调节pH 可依次分离,首先沉淀的是___________ (填离子符号)。

已知:Ⅰ.铍、铝元素处于周期表中的对角线位置,化学性质相似
Ⅱ.常温下: Ksp[Cu(OH)2]、=2.2×10-20、Ksp[Fe(OH)3]=4.0×10-38、Ksp[Mn(OH)2]=2.l×10-13
(1)写出铍铜元件中SiO2与NaOH溶液反应的离子方程式
(2)滤渣B的主要成分为
(3)①溶液C中含NaCl、BeCl2和少量HCl,为提纯BeCl2,选择合理步骤并排序
a.加入过量的NaOH b.过滤 c.加入适量的HCl
d.加入过量的氨水 e.通入过量的CO2 f.洗涤
②从BeCl2溶液中得到BeCl2 固体的操作是
(4)MnO2 能将金属硫化物中的硫元素氧化为单质硫,写出反应Ⅱ中CuS 发生反应的离子方程式
(5)溶液D 中含c(Cu2+)=2.2 mol·L-1、c( Fe3+)=0.008 mol·L-1、c( Mn2+)=0.01mol·L-1,逐滴加入稀氨水调节pH 可依次分离,首先沉淀的是
您最近一年使用:0次
2018-12-29更新
|
643次组卷
|
4卷引用:【全国百强校】山东省师范大学附属中学2019届高三上学期第四次模拟理科综合化学试题
三、填空题 添加题型下试题
填空题
|
适中(0.65)
9. 工业上可通过煤的液化合成甲醇,主反应为:
CO(g)+2H2(g) CH3OH(1)△H=xkJ/mol
CH3OH(1)△H=xkJ/mol
(1)已知常温下CH3OH(1)、H2和CO的燃烧热分别为726.5kJ/mol、285.5kJ/mol、283.0kJ/mol,则x=___________ ;为提高合成甲醇反应的选择性,关键因素是___________ 。
(2)TK下,在容积为1.00L的某密闭容器中进行反应CO(g)+2H2(g) CH3OH(g)△H<0,相关数据如图。
CH3OH(g)△H<0,相关数据如图。
①该反应0~10min的平均速率υ(H2)___________ mol/(L·min);M和N点的逆反应速率较大的是___________ (填“υ逆(M)”、“υ逆(N)”或“不能确定”)。
②10min时容器内CO的体积分数为___________ 。
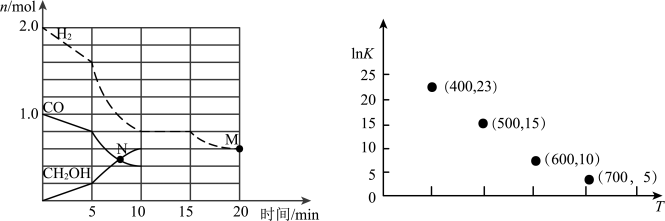
③对于气相反应,常用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)表示平衡常数(以Kp表示),其中PB=P总×B的体积分数。若在TK下平衡气体总压强为xMPa,则该反应的平衡常数Kp=___________ (写出表达式,不必化简)。实验测得不同温度下的lnKp(化学平衡常数Kp的自然对数)如图,请分析lnKp随T呈现上述变化趋势的原因______________________ 。
CO(g)+2H2(g)
 CH3OH(1)△H=xkJ/mol
CH3OH(1)△H=xkJ/mol(1)已知常温下CH3OH(1)、H2和CO的燃烧热分别为726.5kJ/mol、285.5kJ/mol、283.0kJ/mol,则x=
(2)TK下,在容积为1.00L的某密闭容器中进行反应CO(g)+2H2(g)
 CH3OH(g)△H<0,相关数据如图。
CH3OH(g)△H<0,相关数据如图。①该反应0~10min的平均速率υ(H2)
②10min时容器内CO的体积分数为

③对于气相反应,常用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)表示平衡常数(以Kp表示),其中PB=P总×B的体积分数。若在TK下平衡气体总压强为xMPa,则该反应的平衡常数Kp=
您最近一年使用:0次
四、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
10. 无水四氯化锡常用作媒染剂和有机合成中的氯化催化剂。实验室可用熔融的锡(熔点 与
与 反应制备
反应制备 ,装置如图。
,装置如图。
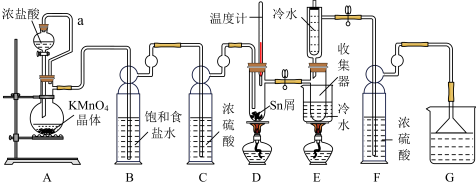
已知: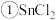 、
、 有关物理性质:
有关物理性质:
 极易水解生成
极易水解生成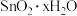 。回答下列问题:
。回答下列问题:
(1)导管a的作用是____________ ,装置A中发生反应的离子方程式为____________________ 。
(2)当观察到装置F液面上方___________ 时才开始点燃D处的酒精灯,待锡熔化后适当增大氯气流量,继续加热。此时继续加热的目的是
________ ;
______
(3)若上述装置中缺少装置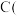 其它均相同),则D处具支试管中发生的主要副反应化学方程式为
其它均相同),则D处具支试管中发生的主要副反应化学方程式为_________________________________ 。
(4) 和锡的反应产物有
和锡的反应产物有 和
和 ,为防止产品中带入过多的
,为防止产品中带入过多的 ,可采取的措施是
,可采取的措施是____________________________________________ 。
(5)滴定分析产品中2价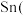 Ⅱ
Ⅱ 的含量:用分析天平称取
的含量:用分析天平称取 产品于锥形瓶中,用蒸馏水溶解,加入淀粉溶液,用
产品于锥形瓶中,用蒸馏水溶解,加入淀粉溶液,用 的碘标准溶液滴定至终点时消耗
的碘标准溶液滴定至终点时消耗 ,则产品中
,则产品中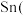 Ⅱ
Ⅱ 的质量分数为
的质量分数为___________ 。 小数点后保留2位,已知
小数点后保留2位,已知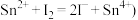
 与
与 反应制备
反应制备 ,装置如图。
,装置如图。 
已知:
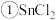 、
、 有关物理性质:
有关物理性质: | 物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
| SnCl2 | 无色晶体 | 246 | 652 |
| SnCl4 | 无色液体 | -33 | 114 |
 极易水解生成
极易水解生成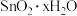 。回答下列问题:
。回答下列问题: (1)导管a的作用是
(2)当观察到装置F液面上方


(3)若上述装置中缺少装置
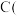 其它均相同),则D处具支试管中发生的主要副反应化学方程式为
其它均相同),则D处具支试管中发生的主要副反应化学方程式为(4)
 和锡的反应产物有
和锡的反应产物有 和
和 ,为防止产品中带入过多的
,为防止产品中带入过多的 ,可采取的措施是
,可采取的措施是(5)滴定分析产品中2价
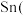 Ⅱ
Ⅱ 的含量:用分析天平称取
的含量:用分析天平称取 产品于锥形瓶中,用蒸馏水溶解,加入淀粉溶液,用
产品于锥形瓶中,用蒸馏水溶解,加入淀粉溶液,用 的碘标准溶液滴定至终点时消耗
的碘标准溶液滴定至终点时消耗 ,则产品中
,则产品中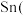 Ⅱ
Ⅱ 的质量分数为
的质量分数为 小数点后保留2位,已知
小数点后保留2位,已知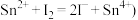
您最近一年使用:0次
2020-01-23更新
|
205次组卷
|
6卷引用:辽宁省沈阳市东北育才学校2019届高三上学期第三次模拟化学试题
解答题-结构与性质
|
适中(0.65)
解题方法
11. Cu3N具有良好的电学和光学性能,在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工程等领域中,发挥着广泛的、不可替代的巨大作用。
(1)C、N、O三种元素的第一电离能由大到小的顺序为___________ 。
(2)与N3-含有相同电子数的三原子分子的空间构型是___________ 。
(3)Cu+的核外电子排布式为___________ ,其在酸性溶液中不稳定,可发生歧化反应生成Cu2+和Cu。但CuO在高温下会分解成Cu2O,试从结构角度解释高温下CuO为何会生成Cu2O__________________ 。
(4)在Cu的催化作用下,乙醇可被空气氧化为乙醛,乙醛分子中碳原子的杂化方式是___________ ,乙醇的沸点明显高于乙醛,其主要原因为___________ 。
(5)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被Cl-取代有两种不同的结构,试画出[Cu(H2O)2(Cl)2]具有极性的分子的结构式___________ 。
(6)Cu3N的晶胞结构如图所示,N3-的配位数为___________ ,Cu+的半径为apm,N3-的半径为bpm,Cu3N的密度为___________ g·cm-3(阿伏伽德罗常数用NA表示)。

(1)C、N、O三种元素的第一电离能由大到小的顺序为
(2)与N3-含有相同电子数的三原子分子的空间构型是
(3)Cu+的核外电子排布式为
(4)在Cu的催化作用下,乙醇可被空气氧化为乙醛,乙醛分子中碳原子的杂化方式是
(5)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被Cl-取代有两种不同的结构,试画出[Cu(H2O)2(Cl)2]具有极性的分子的结构式
(6)Cu3N的晶胞结构如图所示,N3-的配位数为

您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
12. 化合物M是二苯乙炔类液晶材料的一种,最简单的二苯乙炔类化合物是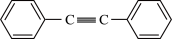 。以互为同系物的单取代芳烃A、G为原料合成M的一种路线如下:(部分反应条件略去)
。以互为同系物的单取代芳烃A、G为原料合成M的一种路线如下:(部分反应条件略去)
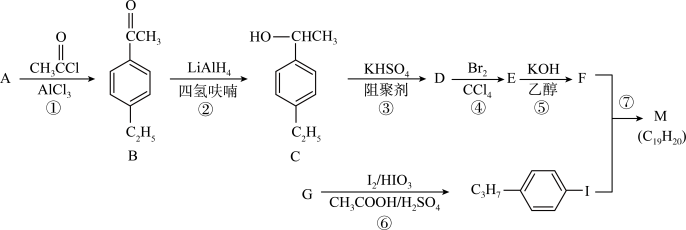
回答下列问题:
(1)A的名称为___________ ,G的分子式为___________ 。M中含有的官能团名称是___________ 。
(2)D分子中最多有___________ 个碳原子共平面。
(3)①的反应类型是___________ ,④的反应类型是___________ 。
(4)⑤的化学方程式为_________________________________ 。
(5)B的同分异构体中能同时满足如下条件:①苯环上有两个取代基,②能发生银镜反应,共有___________ 种(不考虑立体异构),其中核磁共振氢谱为5组峰,且峰面积比为6︰2︰2︰1︰1的结构简式是______________________ 。
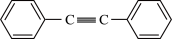 。以互为同系物的单取代芳烃A、G为原料合成M的一种路线如下:(部分反应条件略去)
。以互为同系物的单取代芳烃A、G为原料合成M的一种路线如下:(部分反应条件略去)
回答下列问题:
(1)A的名称为
(2)D分子中最多有
(3)①的反应类型是
(4)⑤的化学方程式为
(5)B的同分异构体中能同时满足如下条件:①苯环上有两个取代基,②能发生银镜反应,共有
【知识点】 根据要求书写同分异构体解读 有机物的推断
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:认识化学科学、有机化学基础、化学与STSE、常见无机物及其应用、物质结构与性质、化学实验基础、化学反应原理
试卷题型(共 12题)
题型
数量
单选题
7
解答题
4
填空题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 胶体的定义及分类 乙酸 几种“油”的辨析 无机非金属材料 | |
| 2 | 0.65 | 同系物的判断 同分异构现象 同分异构体的数目的确定 | |
| 3 | 0.65 | 阿伏加德罗常数的求算 22.4L/mol适用条件 结合物质结构基础知识与NA相关推算 浓硫酸的强氧化性 | |
| 4 | 0.65 | 元素周期律、元素周期表的推断 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 “位构性”关系理解及应用 | |
| 5 | 0.65 | 胶体的制备 铵根离子的检验 石蜡油分解实验 化学实验方案的设计与评价 | |
| 6 | 0.65 | 二次电池 其他二次电池 | |
| 7 | 0.65 | 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 二、解答题 | |||
| 8 | 0.65 | 离子方程式的书写 溶度积常数相关计算 物质分离、提纯综合应用 物质制备的探究 | 工业流程题 |
| 10 | 0.65 | 物质含量的测定 物质制备的探究 综合实验设计与评价 | 实验探究题 |
| 11 | 0.65 | 电离能变化规律 利用杂化轨道理论判断分子的空间构型 利用杂化轨道理论判断化学键杂化类型 晶胞的有关计算 | 结构与性质 |
| 12 | 0.65 | 根据要求书写同分异构体 有机物的推断 | 有机推断题 |
| 三、填空题 | |||
| 9 | 0.65 | 盖斯定律及其有关计算 化学平衡的移动及其影响因素 化学平衡题中基于图表数据的相关计算 | |



