10. 许多含氮物质是农作物生长的营养物质。
(1)肼(N
2H
4)、N
2O
4常用于航天火箭的发射。已知下列反应:
①N
2(g)+O
2(g) =2NO(g) ΔH=+180kJ·mol
-1②2NO(g)+O
2(g)

2NO
2(g) ΔH=-112kJ·mol
-1③2NO
2(g)⇌N
2O
4(g) ΔH=-57kJ·mol
-1④2N
2H
4(g)+N
2O
4(g) =3N
2(g)+4H
2O(g) ΔH=-1136kJ·mol
-1则N
2H
4与O
2反应生成氮气与水蒸气的热化学方程式为
_________________。
(2)一定温度下,向某密闭容器中充入1 mol NO
2,发生反应:2NO
2(g)⇌N
2O
4(g),测得反应体系中气体体积分数与压强之间的关系如图所示:

①a、b、c三点逆反应速率由大到小的顺序为
_______。平衡时若保持压强、温度不变,再向体系中加入一定量的Ne,则平衡
_______移动(填“正向”“逆向”或“不”)。
②a点时NO
2的转化率为
___________,用平衡分压代替平衡浓度也可求出平衡常数K
p,则该温度下K
p=
________Pa
-1。
(3)已知在一定温度下的可逆反应N
2O
4(g)⇌2NO
2(g)中,v
正=k
正c(N
2O
4),v
逆=k
逆c
2(NO
2)(k
正、k
逆只是温度的函数)。若该温度下的平衡常数K=10,则k
正=
______k
逆。升高温度,k
正增大的倍数
_______(填“大于”“小于”或“等于”)k
逆增大的倍数。
(4)氨气是合成众多含氮物质的原料,利用H
2-N
2—生物燃料电池,科学家以固氮酶为正极催化剂、氢化酶为负极催化剂,X交换膜为隔膜,在室温条件下即实现了合成NH
3的同时还获得电能。其工作原理图如下:
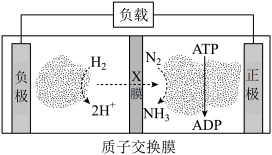
则X膜为
___________交换膜,正极上的电极反应式为
______________________。