26. (1)元素周期表体现了元素周期律,元素周期律的本质是原子核外电子排布的周期性变化。
①下表中的实线是元素周期表的部分边界。请在表中用实线补全周期表的边界
_____________。

②元素甲是第三周期第VIA族元素,请在右边方框中按上图中氢元素的样式写出元素甲的原子序数、元素符号、元素名称和相对原子质量(取整数)
________________。
③元素乙的M层电子数比K层电子数多1,则乙原子半径与甲原子半径比较:
_______>
________(用元素符号表示)。甲、乙的最高价氧化物对应的水化物的酸性强弱为
_______>
________(用化学式表示)。
④请写出55号元素在元素周期表中的位置:
_______________________________(2)工业合成氨的反应N
2(g)+ 3H
2(g)

2NH
3(g)是一个可逆反应、反应条件是高温、高压,并且需要合适的催化剂。已知形成1mol H一H键、1mol N一H键、Imol
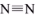
键放出的能量分别为436kJ、391kJ、946kJ。
①若1mol N
2完全反应生成NH
3可
____________(填“吸收”或“放出”)热量
_________kJ。
②如果将1mol N
2和3mol H
2混合,在一定条件下使其充分反应,测得的热量数值总小于上述数值,
其原因是
_______________________________________________________________③实验室模拟工业合成氨时,在容积为2L的密闭容器中进行,反应经过10min后,生成10molNH
3则用N
2表示的化学反应速率是
_______________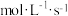
。