10. 我国承诺二氧化碳排放力争2030年前达到峰值,努力争取2060年前实现碳中和。“碳达峰、碳中和”目标下,必须加强对二氧化碳资源开发利用的研究。
(1)2021年9月,中科院天津工业生物技术研究所成果“无细胞化学酶系统催化CO
2合成淀粉”在国际学术期刊《Science》上发表。其中核心反应里有一步是在催化剂作用下CO
2加氢制得甲醇,该反应历程如图所示(吸附在催化剂表面的物质用*标注,如*CO
2表示CO
2吸附在催化剂表面,图中*H已省略)。
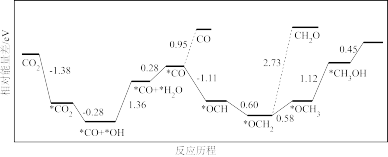
上述过程中得到相对较多的副产物为
___________,合成甲醇过程的决速步化学反应方程式为
___________。
(2)采用CO
2作为碳源,通过催化加氢的方式,不仅可以减少温室气体,还可以转化为高附加值的产品,具有重要的战略意义。CO
2催化加氢可制得多种烯烃,例如乙烯2CO
2(g)+6H
2(g)

C
2H
4(g)+4H
2O(g) ΔH=- 128.0 kJ·mol
-1,下列有利于提高体系CO
2平衡转化率的措施有
___________(填标号)。
A.减小n(CO
2):n(H
2)投料比B.减小体系压强
C.使用高效催化剂D.及时分离H
2O(g)
CO
2催化加氢制乙烯的副反应比较多,主要的副产物为烷烃和CO。若n(CO
2):n(H
2)投料比为1:3,体系压力为1MPa时,无烷烃产物的平衡体系中CO
2转化率和产物选择性随反应温度变化曲线如图。有利于短链烯烃(n≤4)生成的温度范围为
___________(填标号)。
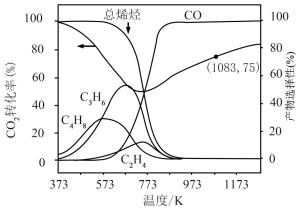
A.373~ 573K B.573~773K
C.773~973K D.973~1173K
(3)为了进一步响应节能减排,实现“双碳”,某企业科研机构利用CO
2和CH
4催化重整,制得合成气(主要成分为CO、H
2),已知部分反应的热化学方程式为:
反应i CH
4(g)=C(s)+2H
2(g) ΔH=+75 kJ·mol
-1反应ii C(s)+O
2(g)=CO
2(g) ΔH= - 394 kJ·mol
-1反应iii C(s)+1/2O
2(g)=CO(g) ΔH=- 111 kJ·mol
-1①由CO
2和CH
4反应生成合成气的热化学方程式为
___________。
②在密闭容器中通入物质的量均为0.1mol的CH
4和CO
2,在一定条件下使CO
2(g)和CH
4(g)发生反应,CH
4的平衡转化率与温度及压强(单位Pa)的关系如图所示。

i:结合如图,在1100°C下y点时v
正___________v
逆(填“大于”、“小于”或“等于”)。
ii:在1100°C下x点已达到平衡状态1,用平衡分压代替平衡浓度可以得到平衡常数K
p,则x点对应温度下反应的平衡常数K
p=
___________。(已知气体分压p
分=气体总压p
总×气体的物质的量分数)。
iii:若起始时在上述密闭容器中加入物质的量均为0.2mol的H
2和CO,在1100°C和p
2条件下达到平衡状态2,与平衡状态1相比,该状态下的c(CO
2)
___________(填“变大”、“变小”或“不变”)。