江苏省连云港市2023-2024学年高二上学期普通高中学业水平合格性考试模拟化学试题
江苏
高二
学业考试
2024-01-14
248次
整体难度:
容易
考查范围:
有机化学基础、化学实验基础、化学与STSE、认识化学科学、物质结构与性质、常见无机物及其应用、化学反应原理
一、单选题 添加题型下试题
| A.酸 | B.碱 | C.氧化物 | D.有机物 |
【知识点】 有机物的分类-根据官能团分类解读
A.  | B. 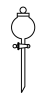 | C.  | D. 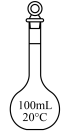 |
【知识点】 配制一定物质的量浓度的溶液实验的仪器解读
| A.Cl- | B.MnO | C.Hg2+ | D.Pb2+ |
【知识点】 水污染
| A.氯化钠溶液 | B.硫酸钾 |
| C.金属铝 | D.二氧化硫 |
| A.BaCl2 | B.KOH | C.CaO | D.Na2S |
【知识点】 化学键与物质类别关系的判断解读
 、
、 、Cl-,该溶液中还可能大量存在的离子是
、Cl-,该溶液中还可能大量存在的离子是| A.OH- | B.Ba2+ | C.Na+ | D.Ag+ |
【知识点】 限定条件下的离子共存解读
| A.乙酸乙酯 | B.聚乙烯 | C.十六烷 | D.甘油 |
【知识点】 聚乙烯结构及应用解读 高分子化合物的分类和表示方法解读
| A.核电荷数 | B.电子数 |
| C.最外层电子数 | D.电子层数 |
【知识点】 原子的基本构成解读 原子中相关数值及其之间的相互关系解读
| A.N2的结构式:N—N |
B.中子数为8的氮原子: |
C.NH3的电子式: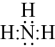 |
D.NH4Cl的电离方程式:NH4Cl⇌ +Cl- +Cl- |
| A.Cl2是氧化剂 | B.N元素化合价降低 |
| C.该反应中N元素全部被氧化 | D.Cl2在反应过程中失去电子 |
| A.浓硫酸具有脱水性,可用来干燥Cl2 |
| B.FeCl3溶液显酸性,可用于印刷电路板 |
| C.Na2O2呈淡黄色,可用作呼吸面具中的供氧剂 |
| D.活性铁粉具有还原性,可用作食品抗氧化剂 |
| A.用过滤法除去NaCl溶液中的泥沙 |
| B.用蒸馏法分离乙酸(沸点118℃)与乙醚(沸点34℃) |
| C.用石灰水鉴别NaHCO3与Na2CO3 |
| D.用盐酸酸化的BaCl2溶液检验Na2SO3是否变质 |
| A.原子半径:r(Al)>r(Mg) | B.金属性:Mg>Na |
| C.熔点:Na2O>Al2O3 | D.碱性:NaOH>Mg(OH)2 |
【知识点】 同周期元素性质递变规律 微粒半径大小的比较方法解读
| A.钠与水的反应:2Na+2H2O=2Na++2OH-+H2↑ |
B.用小苏打治疗胃酸过多:CO +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
C.氧化铝溶于氢氧化钠溶液:Al2O3+2OH-=2AlO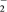 +H2O +H2O |
D.电解饱和食盐水:2Cl-+2H2O 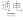 2OH-+H2↑+Cl2↑ 2OH-+H2↑+Cl2↑ |
22. 乙酸(CH3COOH)是生活中常见的一种有机物,下列有关乙酸的说法正确的是
| A.无色无味难溶于水 |
| B.可以使紫色石蕊试液变蓝 |
| C.能与金属钠反应生成氢气 |
| D.能与甲醇发生酯化反应生成甲酸乙酯 |
| A.CH2=CH2+HBr→CH3CH2Br |
B.2CH3CH2OH+O2  2CH3CHO+2H2O 2CH3CHO+2H2O |
C.CH3COOH+CH3CH2OH 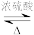 CH3COOCH2CH3 CH3COOCH2CH3 |
D. 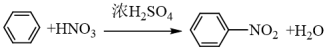 |
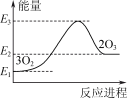
| A.2O3(g)=3O2(g)为吸热反应 |
| B.氧气比臭氧稳定 |
| C.反应物的总能量高于生成物的总能量 |
| D.O2(g)中化学键的断裂需要放出能量 |
|
|
|
|
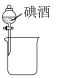
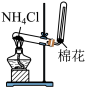
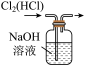
| A.分离碘和酒精 | B.实验室制氨气 | C.除去Cl2中的HCl | D.排水法收集NO |
| A.A | B.B | C.C | D.D |
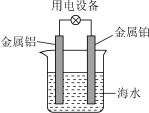
| A.铝片作正极 |
| B.该装置可将电能转化为化学能 |
| C.电池工作时铝电极逐渐被消耗 |
| D.电子从铂电极经导线流向铝电极 |
| A.升高温度会加快反应速率 |
| B.增大Fe3+和I-的浓度能加快反应速率 |
| C.当上述可逆反应达到平衡时,溶液中c(Fe3+)与c(Fe2+)相等 |
| D.向反应后的溶液中加入CCl4,充分振荡后静置,取上层溶液滴加KSCN溶液,溶液变成血红色 |
【知识点】 Fe3+的检验解读 影响化学反应速率的因素

| A.装置a中每生成1 mol CuCl,理论上至少需要通入标准状况下22.4 L SO2 |
| B.装置b的作用是安全瓶,防止倒吸 |
| C.装置c中的液体可以是NaOH浓溶液,吸收尾气 |
| D.当n(NaCl)/n(CuSO4)大于1.6时,CuCl产率减小的原因是部分CuCl转化为[CuCl2]- |
二、填空题 添加题型下试题
CO2
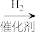 CH3OH
CH3OH HCHO
HCHO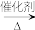 …→(C6H10O5)n
…→(C6H10O5)n(1)CH3OH分子中与氧原子形成共价键的原子为
(2)CH3CHO与HCHO互为同系物,具有相同的官能团是
(3)CO2催化加H2制CH3OH,该反应一般由以下两步反应实现:
Ⅰ. CO2+H2⇌CO+H2O Ⅱ. ……
写出一定条件下反应Ⅱ的化学方程式:
【知识点】 物质的转化 常见官能团名称、组成及结构解读 醇的组成、结构解读
三、解答题 添加题型下试题
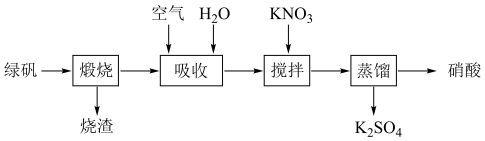
(2)“吸收”过程通入足量空气的目的是
(3)“蒸馏”获得的硝酸液体显黄色是因为溶有
(4)通过下列实验测定硫酸亚铁晶体样品的纯度。准确称取1.2000 g样品置于锥形瓶中,用50 mL蒸馏水完全溶解,加一定量硫酸和磷酸溶液;用0.02000 mol·L-1 KMnO4标准溶液滴定至终点,消耗KMnO4标准溶液41.00 mL。
已知:8H++MnO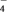 +5Fe2+=Mn2++5Fe3++4H2O。计算硫酸亚铁晶体样品中FeSO4·7H2O的质量分数(写出计算过程)。
+5Fe2+=Mn2++5Fe3++4H2O。计算硫酸亚铁晶体样品中FeSO4·7H2O的质量分数(写出计算过程)。
【知识点】 常见无机物的制备解读 探究物质组成或测量物质的含量解读
试卷分析
试卷题型(共 30题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 有机物的分类-根据官能团分类 | |
| 2 | 0.85 | 淀粉和纤维素 淀粉、纤维素的水解 | |
| 3 | 0.85 | 配制一定物质的量浓度的溶液实验的仪器 | |
| 4 | 0.65 | 水污染 | |
| 5 | 0.65 | 胶体的性质和应用 | |
| 6 | 0.85 | 酸、碱、盐、氧化物 电解质与非电解质 非电解质、电解质物质类别判断 | |
| 7 | 0.65 | 同分异构现象、同分异构体的概念 元素、核素、同位素 几组常见同素异形体 | |
| 8 | 0.65 | 化学键与物质类别关系的判断 | |
| 9 | 0.65 | 限定条件下的离子共存 | |
| 10 | 0.65 | 氯水 氨水 碳酸钠 | |
| 11 | 0.85 | 聚乙烯结构及应用 高分子化合物的分类和表示方法 | |
| 12 | 0.65 | 原子的基本构成 原子中相关数值及其之间的相互关系 | |
| 13 | 0.65 | 氯气 氯水 | |
| 14 | 0.65 | 化学用语综合判断 原子结构示意图、离子结构示意图 共价化合物的结构及形成过程 | |
| 15 | 0.85 | 氧化还原反应的几组概念 氧化还原反应定义、本质及特征 氧化还原反应的规律 | |
| 16 | 0.65 | 氨的还原性 | |
| 17 | 0.65 | 浓硫酸的吸水性 过氧化钠的物理性质、组成、结构及用途 铁 铁盐 | |
| 18 | 0.65 | 碳酸钠与碳酸氢钠鉴别的实验 蒸馏与分馏 过滤 亚硫酸及其盐 | |
| 19 | 0.65 | 四种基本反应类型 | |
| 20 | 0.65 | 同周期元素性质递变规律 微粒半径大小的比较方法 | |
| 21 | 0.85 | 离子方程式的正误判断 钠与水反应原理 碳酸氢钠的俗称、物理性质及用途 氧化铝与碱溶液反应 | |
| 22 | 0.85 | 乙酸具有酸的通性 乙酸的酯化反应 | |
| 23 | 0.65 | 有机反应类型 取代反应 苯的取代反应 | |
| 24 | 0.65 | 吸热反应和放热反应 根据△H=生成物的总能量之和-反应物的总能量之和进行计算 | |
| 25 | 0.85 | 氯气的实验室制法 氨气的实验室制法 常见气体的制备与收集 | |
| 26 | 0.85 | 原电池原理理解 原电池电子流向判断及应用 原电池正负极判断 | |
| 27 | 0.65 | Fe3+的检验 影响化学反应速率的因素 | |
| 28 | 0.65 | 二氧化硫的化学性质 物质制备的探究 | |
| 二、填空题 | |||
| 29 | 0.65 | 物质的转化 常见官能团名称、组成及结构 醇的组成、结构 | |
| 三、解答题 | |||
| 30 | 0.65 | 常见无机物的制备 探究物质组成或测量物质的含量 | 工业流程题 |

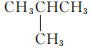 和CH3CH2CH2CH3
和CH3CH2CH2CH3