23. 某兴趣小组用硫酸铜制备硫酸四氨合铜([Cu(NH
3)
4]SO
4·H
2O,M=246g/mol),并对产品的纯度进行了测定。
实验一:硫酸四氨合铜的制备
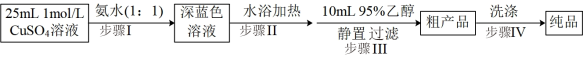
实验二:硫酸四氨合铜纯度测定
步骤①:准确称取mg固体于烧杯中,加稀硫酸溶解,再定容至250mL
步骤②:量取上述试液25.00mL于锥形瓶中,加入100mL水和KI固体(稍过量)
步骤③:用Na
2S
2O
3标准溶液(0.1mol/L)滴定至溶液呈淡黄色,加入淀粉溶液2mL,溶液变为蓝黑色,再加入10%KSCN溶液10mL,继续用Na
2S
2O
3标准溶液滴定至蓝色刚好消失,重复操作3次,平均用量为VmL。
已知:①[Cu(NH
3)
4]SO
4·H
2O溶于水。
②[Cu(NH
3)
4]
2+
Cu
2++4NH
3,2Cu
2++4I
-=2CuI↓+I
2,CuI沉淀表面易吸附I
2。③CuSCN比CuI更难溶。
④I
2+2

=

+2I
-。
请回答:
(1)硫酸四氨合铜的制备过程中,步骤I的反应中先生成沉淀再溶解,该步骤中的离子方程式为
___________。步骤Ⅲ中加入95%乙醇能降低溶质溶解度的原因
___________。
(2)下列说法正确的是
___________。
A.配制250mL溶液的实验中用到的玻璃仪器只包括烧杯、玻璃棒、250mL容量瓶
B.滴定时,加入KSCN的目的是把CuI吸附的I
2释放出来
C.上述测定过程提及的仪器中容量瓶、锥形瓶,在使用前一定不能润洗
D.将标准溶液装入滴定管时,应借助烧杯或漏斗等玻璃仪器转移
E.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
(3)硫酸四氨合铜纯度测定过程中:
①Cu
2+与I
-反应时,pH不能过高,给出两点理由:
___________。
②滴定前。有关滴定管的正确操作为 (选出正确操作并按序排列):
___________。
检漏→蒸馏水洗涤→___________→___________→___________→___________→开始滴定。
A.烘干
B.装入滴定液至零刻度以上
C.调整滴定液液面至零刻度或零刻度以下
D.用洗耳球吹出润洗液
E记录起始读数
F.用滴定液润洗2至3次
G.排除气泡
③在横线上补全滴定管润洗的操作:从滴定管上口加3~5mL所要盛装的酸或碱,
___________。然后,一手控制活塞(轻轻转动酸式滴定管的活塞:或者轻轻挤压碱式滴定管中的玻璃球),将液体从滴定管下部放入预置的烧杯中。重复2~3次。
④硫酸四氨合铜纯度是
___________(用m、V表示)。