18-19高一·浙江·周测
名校
1 . 现有下列几个离子反应:
①Cr2O +14H++6Cl-=2Cr3++3Cl2↑+7H2O
+14H++6Cl-=2Cr3++3Cl2↑+7H2O
②2Fe2++Br2=2Fe3++2Br-
③2Fe3++SO2+2H2O=2Fe2++SO +4H+
+4H+
④2Br-+Cl2=Br2+2Cl-
下列有关性质的比较中正确的是
①Cr2O
 +14H++6Cl-=2Cr3++3Cl2↑+7H2O
+14H++6Cl-=2Cr3++3Cl2↑+7H2O②2Fe2++Br2=2Fe3++2Br-
③2Fe3++SO2+2H2O=2Fe2++SO
 +4H+
+4H+④2Br-+Cl2=Br2+2Cl-
下列有关性质的比较中正确的是
A.氧化性:Cr2O >Cl2>Fe3+ >Cl2>Fe3+ | B.氧化性:Cl2>Br2>Cr2O |
| C.还原性:SO2<Fe2+<Br- | D.还原性:Cl->Cr3+>Fe2+ |
您最近一年使用:0次
2020-03-13更新
|
573次组卷
|
13卷引用:新疆维吾尔自治区乌鲁木齐市第四中学2020-2021学年高一上学期期末考试化学试题
新疆维吾尔自治区乌鲁木齐市第四中学2020-2021学年高一上学期期末考试化学试题(已下线)【新东方】高中化学5037广西武宣县第二中学2019-2020学年高一上学期期末考试化学试题(已下线)专题四 氧化还原反应(提分特训)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训(已下线)1.3.2 氧化剂还原剂(精练)——2020-2021学年上学期高一化学同步精品课堂(人教版必修第一册)浙江省平湖市当湖高级中学2021-2022学年高一上学期第一次月考化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)甘肃省永昌县第一高级中学2021-2022学年高一上学期期末补考化学试题 (已下线)衔接点12 氧化剂和还原剂-2022年初升高化学无忧衔接?云南省玉溪市民族中学2021-2022学年高一上学期期末考试化学试题第2课时 氧化剂和还原剂河北省石家庄市第二中学西校区2023-2024学年高一上学期期中模拟考试化学试题
11-12高一上·山西忻州·期中
2 . 在溶液中可以发生反应:X+2Y3+=2Y2++X2+,则下列叙述①X被氧化;②X是氧化剂;③X具有还原性;④Y2+是氧化产物;⑤Y2+具有还原性;⑥Y3+的氧化性比X2+的氧化性强。以下叙述中正确的是( )
| A.②④⑥ | B.①③④ | C.①③⑤⑥ | D.②⑤ |
您最近一年使用:0次
2020-03-06更新
|
324次组卷
|
28卷引用:新疆乌鲁木齐市第二十中学2020-2021学年高一上学期段考(期中)化学试题
新疆乌鲁木齐市第二十中学2020-2021学年高一上学期段考(期中)化学试题新疆哈密市第八中学2021-2022学年高一上学期期中考试化学试题(已下线)2011-2012学年山西省忻州一中高一上学期期中考试化学试卷(已下线)2011-2012学年山西省临汾一中高一上学期期中考试化学试卷(已下线)2011-2012学年云南省玉溪一中高一下学期期中考试化学试卷(已下线)2013届山西省太原五中高三10月月考理科化学试卷(已下线)2014-2015学年山东省德州市普高高二上学期期中理科化学试卷2016届福建省福州四中高三上学期10月第一次月考化学试卷2015-2016学年山西省大同一中高一上期末考试化学试卷湖南省衡阳县第一中学2018届高三上学期第二次月考化学试题吉林省长春市九台区师范高级中学2018-2019学年高一上学期期中考试化学试题陕西省城固县第一中学2018-2019学年高一上学期期末考试化学试题山西省灵丘县一中2017-2018学年高一上学期期中考试化学试卷北京市昌平区新学道临川学校2019-2020学年高一上学期期中考试化学试题江西省南昌市进贤一中2019-2020学年高一上学期期中考试化学试题步步为赢 高一化学寒假作业:作业七 阶段检测(二)黑龙江省大庆市第十中学2019-2020学年高一上学期10月月考化学试题2019年广东省汕尾市高三第一次模拟考试化学试题四川省南充市阆中中学2020届高三化学选择题专项训练(13)(已下线)【南昌新东方】2019 进贤一中 高一上 期中(已下线)小题必刷08 氧化还原反应的规律及应用——2021年高考化学一轮复习小题必刷(通用版)山东省滨州市博兴县第三中学2020-2021学年高一上学期10月月考化学试题江西省宜春市第九中学2020-2021学年高一上学期第二次月考化学试题湖南省临澧县第一中学2020-2021学年高一上学期阶段性考试(二)化学试题安徽省滁州市定远县炉桥中学2020-2021学年高一上学期第一次质量检测化学试题宁夏固原市第一中学2023届高三上学期第一次月考化学试题山东省利津县高级中学2022-2023学年高一12月月考化学试题北京市第十一中学2021-2022学年高一上学期期中考试化学试题
名校
解题方法
3 . 常温下,在溶液中可发生以下反应:①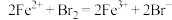 ②
② ③
③ 由此判断下列说法正确的是( )
由此判断下列说法正确的是( )
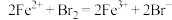 ②
② ③
③ 由此判断下列说法正确的是( )
由此判断下列说法正确的是( )| A.铁元素在反应①中被还原,在③中被氧化 |
| B.反应②中当有1molCl2被氧化时,有2molBr—被还原 |
C.氧化性强弱顺序为: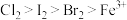 |
D.还原性强弱顺序为: |
您最近一年使用:0次
2020-02-17更新
|
200次组卷
|
10卷引用:【全国百强校】新疆维吾尔自治区第二师华山中学2018-2019学年高一上学期期末考试化学试题
【全国百强校】新疆维吾尔自治区第二师华山中学2018-2019学年高一上学期期末考试化学试题云南省大理市下关一中2017-2018学年高一上学期期中考试化学试题贵州省普定县一中2018-2019学年高一上学期期中考试化学试题【市级联考】云南省大理市2017-2018学年高一上学期期中考试化学试题云南省富宁县一中2019-2020学年高二上学期开学考试化学试题四川省泸县第五中学2019-2020学年高一上学期期中考试化学试题云南省丽江市玉龙县第一中学2019—2020学年高一上学期期末考试化学试题云南省大理市下关第一中学2019-2020学年高一上学期期中考试化学试题安徽省肥东县高级中学2020-2021学年高一上学期期中考试化学试题四川省遂宁市第二中学2020-2021学年高一上学期第二阶段测试化学试题
11-12高三·福建三明·阶段练习
名校
4 . 常温下,在溶液中可以发生反应:X+2Y3+=2Y2++X2+,对下列叙述的判断正确的是( )
①X被氧化 ②X是氧化剂 ③X具有还原性 ④Y2+是氧化产物
⑤Y2+具有还原性 ⑥Y3+的氧化性比X2+的氧化性强
①X被氧化 ②X是氧化剂 ③X具有还原性 ④Y2+是氧化产物
⑤Y2+具有还原性 ⑥Y3+的氧化性比X2+的氧化性强
| A.②③④⑥ | B.①③④⑤ | C.①③⑤⑥ | D.①②⑤⑥ |
您最近一年使用:0次
名校
5 . 铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
Ⅰ.(1)所含铁元素既有氧化性又有还原性的物质是________ (填字母)。
A.Fe B.FeCl3 C.FeSO4 D.Fe2O3
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是( )
A. NaNO2被氧化 B. 药品美蓝是还原剂
C. NaNO2是还原剂 D. 药品美蓝被还原
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:________________________________ 。
Ⅱ. 高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(4)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中Na2O2是________ (填“氧化剂”或“还原剂”)。
(5)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O。
、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3∶2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:__________________________________________ 。
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为________ mol。
Ⅰ.(1)所含铁元素既有氧化性又有还原性的物质是
A.Fe B.FeCl3 C.FeSO4 D.Fe2O3
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是
A. NaNO2被氧化 B. 药品美蓝是还原剂
C. NaNO2是还原剂 D. 药品美蓝被还原
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
Ⅱ. 高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(4)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中Na2O2是
(5)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O。
、Cl-、H2O。①碱性条件下,氧化剂和还原剂的物质的量的比为3∶2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为
您最近一年使用:0次
2020-01-16更新
|
221次组卷
|
3卷引用:新疆哈密市第十五中学2021-2022学年高一上学期期末考试化学试题
名校
解题方法
6 . 将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个反应:SO2+2Fe3++2H2O == SO42-+4H++2Fe2+,Cr2O72-+6Fe2++14H+ == 2Cr3++6Fe3++7H2O。下列说法正确的是
| A.Cr2O72-不能将SO2氧化 | B.还原性:Cr3+>Fe2+>SO2 |
| C.氧化性:Cr2O72->Fe3+>SO2 | D.两个反应中Fe3+均表现还原性 |
您最近一年使用:0次
2018-06-27更新
|
493次组卷
|
10卷引用:新疆乌鲁木齐市第二十三中学2023-2024学年高一上学期10月月考化学试题
新疆乌鲁木齐市第二十三中学2023-2024学年高一上学期10月月考化学试题【全国市级联考】贵州省毕节市2017-2018学年高一毕业学业达标模拟考试化学试题云南省玉溪市第一中学2017-2018学年高一下学期期末考试化学试题安徽省定远重点中学2018-2019学年高一下学期开学考试化学试题甘肃省天水市第一中学2019-2020学年高一上学期第二学段考试化学试题江西省南昌市安义中学2019-2020学年高一上学期期末考试化学试题云南省曲靖市沾益县炎方一中2019-2020学年高一上学期期末考试化学试题(已下线)【南昌新东方】2019-2020 安义中学 高一(上)期末 001广西象州县中学2020-2021学年高一上学期12月月考化学试题河南省信阳高级中学2020-2021学年高一6月月考化学试题
名校
解题方法
7 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究钠在氧气中燃烧所得固体成分 | 取少量加热后的固体粉末,加入少量蒸馏水 | 若有气泡产生,则证明燃烧后的固体粉末为Na2O2 |
| B | 比较KMnO4、Cl2 和Fe3+的氧化性 | 向酸性 KMnO4 溶液中滴入 FeCl2溶液,紫红色溶液变浅并伴有黄绿色气体产生 | 氧化性强弱:KMnO4>Cl2>Fe3+ |
| C | 制备 Fe(OH)3胶体 | 向沸水中滴加5~6滴FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。用红色激光笔照射液体 | 若产生一条光亮的“通路”,则得到Fe(OH)3 胶体 |
| D | 检验某溶液中是否存在K+ | 用玻璃棒蘸取待测液放在酒精灯外焰上灼烧,观察火焰的颜色 | 若看到火焰为黄色,则一定不存在 K+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-27更新
|
210次组卷
|
2卷引用:新疆乌鲁木齐八一中学2023-2024学年高一上学期1月月考化学试卷
名校
8 .  是一种食品添加剂,但食用过量可能致癌。酸性
是一种食品添加剂,但食用过量可能致癌。酸性 溶液与
溶液与 反应的化学方程式为
反应的化学方程式为 (未配平)。下列关于该反应叙述中
(未配平)。下列关于该反应叙述中不正确 的是
 是一种食品添加剂,但食用过量可能致癌。酸性
是一种食品添加剂,但食用过量可能致癌。酸性 溶液与
溶液与 反应的化学方程式为
反应的化学方程式为 (未配平)。下列关于该反应叙述中
(未配平)。下列关于该反应叙述中A. 是还原剂 是还原剂 | B.参加反应的 和 和 的个数比是 的个数比是 |
C. 是还原产物 是还原产物 | D.该反应条件下,氧化性 |
您最近一年使用:0次
2024-01-25更新
|
151次组卷
|
2卷引用:新疆维吾尔自治区乌鲁木齐市第101中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
9 . 实验室迅速制备少量氯气可利用如下反应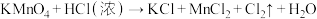 (未配平),此反应常温下就可以迅速进行.请回答下列问题:
(未配平),此反应常温下就可以迅速进行.请回答下列问题:
(1)上述反应中被氧化的元素是_________ ,盐酸在该反应中表现了___________ 性质,当生成6.72L(标准状况下) 时,转移电子的物质的量为
时,转移电子的物质的量为___________ 。
(2)实验室通常利用 与浓盐酸共热反应制得氯气,据此可知
与浓盐酸共热反应制得氯气,据此可知 、
、 、
、 三种物质的氧化性由强到弱的顺序为
三种物质的氧化性由强到弱的顺序为_______________________________ 。
(3)酸性 溶液与
溶液与 反应生成
反应生成 ,该反应的离子方程式是
,该反应的离子方程式是_______________________ 。
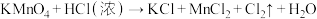 (未配平),此反应常温下就可以迅速进行.请回答下列问题:
(未配平),此反应常温下就可以迅速进行.请回答下列问题:(1)上述反应中被氧化的元素是
 时,转移电子的物质的量为
时,转移电子的物质的量为(2)实验室通常利用
 与浓盐酸共热反应制得氯气,据此可知
与浓盐酸共热反应制得氯气,据此可知 、
、 、
、 三种物质的氧化性由强到弱的顺序为
三种物质的氧化性由强到弱的顺序为(3)酸性
 溶液与
溶液与 反应生成
反应生成 ,该反应的离子方程式是
,该反应的离子方程式是
您最近一年使用:0次
10 . 由下列实验操作和现象得出的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向久置的FeCl2溶液中滴入几滴酸性KMnO4溶液 | 酸性KMnO4溶液褪色 | 久置的FeCl2溶液中一定含有Fe2+ |
| B | 铂丝蘸取某无色溶液后在火焰上灼烧 | 火焰呈黄色 | 该无色溶液中阳离子只含Na+ |
| C | 向某钾盐中滴加稀盐酸 | 产生的气体可以使澄清石灰水变浑浊 | 该钾盐为K2CO3或KHCO3或二者的混合物 |
| D | 向添有KIO3的食盐中加入淀粉溶液、稀盐酸和KI | 溶液变蓝 | 氧化性:IO >I- >I- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



